细胞外囊泡(EVs)因其良好的生物相容性和低免疫原性,被视为极具前景的药物递送载体。通过基因工程将治疗性分子装载到EVs中是关键,但现有方法存在效率低、支架蛋白结构复杂等问题。
近期,南京大学李维勤/张昊、香港中文大学夏江、东南大学王适之/余艺文团队合作在Nat Commun上发表题为“Extracellular vesicle engineering using a small scaffold protein”的论文,主要介绍了通过蛋白质组学筛选,发现并优化出一种仅含144个氨基酸的截短型支架蛋白EN144的研究工作。该蛋白能高效地将多种治疗性“货物”(如蛋白质、mRNA、基因编辑工具)装载到EVs中,并实现靶向递送。研究进一步构建了展示IL-6诱饵受体gp130的工程化EVs,在脓毒症和骨关节炎小鼠模型中展现出强大的抗炎和治疗效果。论文第一作者为东南大学颜文静(已经入职山东第二医科大学)、东南大学王适之、南京大学郝海滨。
1.发现高效EV支架蛋白EN144:研究团队使用三种独立的EV分离方法结合蛋白质组学分析,从Expi293F细胞来源的EVs中筛选膜蛋白。他们鉴定出ENPP1是一个高效的EV分选蛋白。进一步地,他们创造了一个仅包含ENPP1跨膜区和胞质域的144个氨基酸截短变体——EN144(图1f-h)。EN144是目前已知的最短、结构最简单的EV特异性支架蛋白,其装载EGFP等货物的效率比全长ENPP1高出3倍,并显著优于常用的PTGFRN和Lamp2b等支架蛋白(图1b-g)。
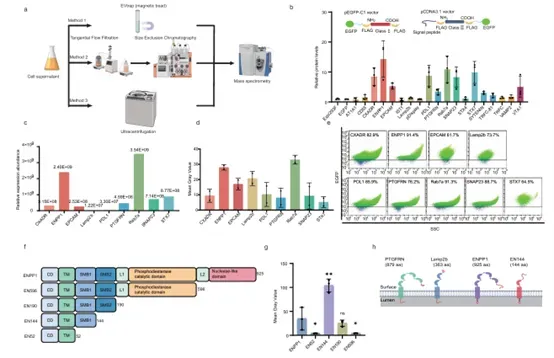
图1. 鉴定EN144作为最小的EV特异性支架蛋白
2. EN144-EVs具有良好的生物相容性和体内分布特性:EN144-EVs保持了天然EVs的典型形态、大小和标志物表达(图2a-d)。蛋白质组学分析显示,EN144的过表达未引起EVs蛋白谱的显著有害改变(图2e-f)。体内外毒性实验证明其安全性良好。静脉注射后,EN144-EVs主要分布在肝脏和脾脏,与天然EVs类似,但积累更多(图2g-h)。
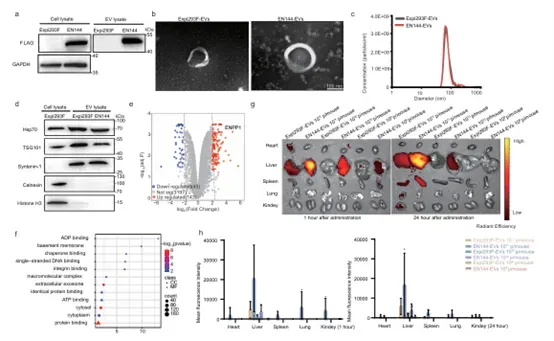
图2. EN144-EVs的蛋白质组分析及体内分布
3. EN144实现EVs表面和腔内“货物”的高效装载:
①表面修饰(靶向):将软骨细胞亲和肽(CAP)融合到EN144的C端,成功构建了靶向软骨细胞的EVs(EN144-EV-CAP),其被原代软骨细胞摄取的效率显著高于其他支架蛋白构建的EVs(图3a-c)。
②腔内装载mRNA:利用古菌核糖体蛋白L7Ae与其识别的C/D Box RNA基序配对系统,EN144能高效地将EGFP mRNA装载到EVs中,并递送至受体细胞进行翻译(图3d-g)。
③腔内装载CRISPR/Cas9复合物:测试了多种蛋白质异源二聚化策略(如GFP-纳米抗体、光控CIBN-CRY2等),发现GFP-纳米抗体系统能最有效地将CRISPR/Cas9基因编辑工具装载到EN144-EVs中。这些EVs能将功能性Cas9/sgRNA RNP复合物递送到细胞中,并成功实现基因编辑(图3h-n)。
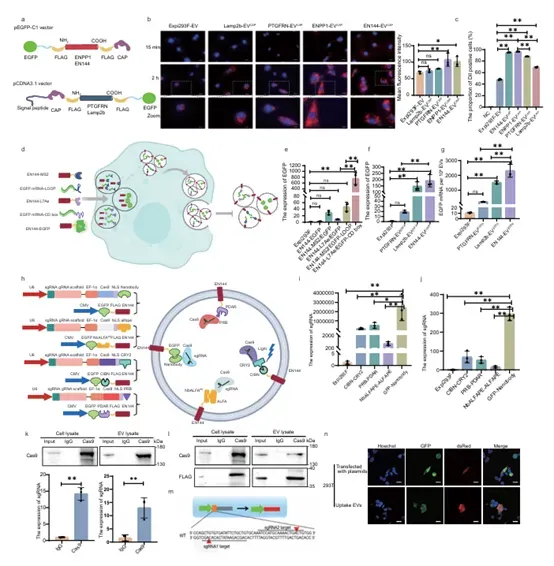
图3. EN144-EVs的表面和腔内货物装载
4. 工程化“诱饵EVs”治疗脓毒症:研究将EN144与人源IL-6信号转导受体gp130融合,构建了EN144-EVhgp130。在LPS诱导的脓毒症小鼠模型中,静脉注射EN144-EVhgp130能有效抑制IL-6的“反式信号”(trans-signaling),显著降低血清中IL-6、TNF-α等炎症因子水平,改善急性期蛋白反应,并提高小鼠生存率(图4)。
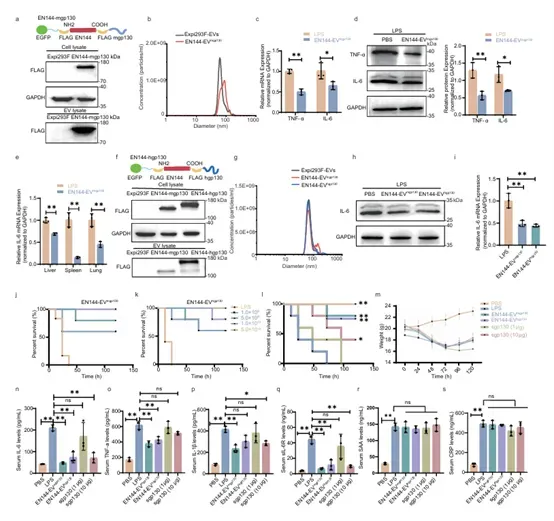
图4. EN144-EVhgp130在小鼠脓毒症模型中的抗炎作用。
5. 靶向性“诱饵EVs”治疗骨关节炎:进一步将EN144、gp130和CAP肽串联,构建了靶向软骨的EN144-EVhgp130-CAP。在大鼠前交叉韧带横断(ACLT)诱导的骨关节炎模型中,关节腔内注射EN144-EVhgp130-CAP能有效靶向软骨细胞和滑膜,抑制局部IL-6信号,减少软骨降解标志物MMP13的表达,增加软骨基质COL2A1,促进滑膜M2型巨噬细胞极化,从而显著减轻软骨损伤和炎症,效果优于临床常用的透明质酸(HA)治疗(图5)。
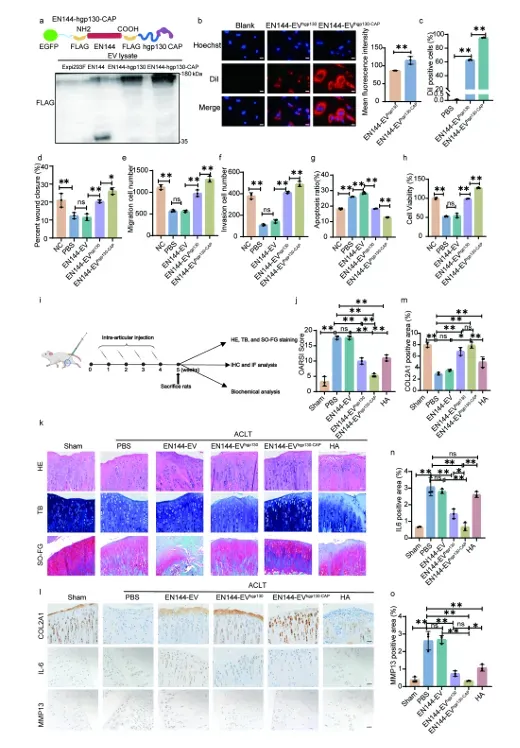
图5. 构建EN144-EVhgp130-CAP 用于靶向修复骨关节炎大鼠的软骨损伤。
总结:该研究确立EN144作为一个最小化、高性能的EV工程化平台支架蛋白。它能够灵活、高效地实现EVs的表面靶向修饰和腔内多种治疗性分子(蛋白、mRNA、基因编辑工具)的装载,并成功应用于构建针对IL-6信号通路的“诱饵EVs”,在脓毒症和骨关节炎两种重要的炎症性疾病模型中证明了其强大的治疗潜力。
参考文献:
Yan, W., Wang, S., Hao, H. et al. Extracellular vesicle engineering using a small scaffold protein. Nat Commun.2026 Mar 10. doi: 10.1038/s41467-026-70451-x