南京大学医学院附属金陵医院 | miR-218-5p+RGD 修饰:糖尿病肾病线粒体自噬调控新突破
- 2026-05-13 22:40:36

导读
本研究以糖尿病肾病(DKD)足细胞损伤伴线粒体自噬抑制为核心问题,首先发现调节性 T 细胞外泌体(Treg-Exos)可减轻高糖 / 糖基化终产物诱导的足细胞损伤,经测序筛选确定关键效应分子为 miR-218-5p;通过双荧光素酶等实验证实 miR-218-5p 靶向抑制 TNC,进而阻断 TLR4/SRC/FUNDC1 通路、恢复线粒体自噬;为提升靶向性,构建膜表面表达 RGD 肽的工程化外泌体(RGD-Treg-Exos),使其通过足细胞整合素实现精准递送;体内外结果一致表明,该工程化外泌体可显著恢复足细胞标志物表达、改善肾小球病理、降低尿白蛋白肌酐比,最终有效缓解 DKD 足细胞损伤,为 DKD 靶向无细胞治疗提供全新策略。
注:该文章发表于《Advanced Science》,该期刊最新影响因子为14.1,五年影响因子15.6,属于JCR Q1区及中科院综合性期刊1区。
研究亮点
首次揭示 Treg 外泌体通过 miR-218-5p 调控 TNC/TLR4/SRC/FUNDC1 通路恢复足细胞线粒体自噬;构建 RGD 修饰工程化外泌体实现足细胞精准靶向递送,为 DKD 提供安全高效的无细胞靶向治疗新方案。
研究背景
糖尿病肾病(DKD)是糖尿病最严重并发症之一,也是终末期肾病的主要诱因,足细胞损伤是 DKD 早期核心病理改变与进展关键驱动因素。足细胞富含线粒体且高度依赖线粒体供能,DKD 状态下高糖与糖基化终产物(AGEs)会显著抑制足细胞线粒体自噬,导致受损线粒体大量堆积、细胞凋亡增加、滤过屏障功能受损,最终引发蛋白尿与肾小球硬化。目前临床缺乏靶向足细胞、恢复线粒体自噬的特异性治疗手段。调节性 T 细胞(Tregs)具有免疫调节与组织保护作用,其外泌体(Treg-Exos)作为无细胞治疗载体,无表型转换风险且可穿透肾小球滤过屏障,但 Treg-Exos 对 DKD 足细胞的保护效应、核心分子机制及靶向递送策略尚未明确,亟待系统解析。
研究方法
本研究采用体外细胞与体内动物模型结合的策略:体外分离健康人外周血 CD4+CD25+Treg 细胞,超速离心提取外泌体并经 TEM、NTA、WB 鉴定;以高糖 + AGEs 诱导人足细胞损伤模型,通过共培养、外泌体孵育、GW4869 抑制外泌体分泌等明确 Treg-Exos 保护作用;经 miRNA 测序与交集分析筛选关键 miR-218-5p,利用双荧光素酶验证靶基因 TNC;构建 miR-218-5p 过表达 / 抑制、TNC 敲低 / 过表达、TLR4/SRC 干预等细胞体系;构建 DKD 小鼠模型(高脂饮食 + STZ),制备足细胞特异性 TNC/ITGAV 敲除小鼠;通过 RGD-CD63 质粒构建工程化 RGD-Treg-Exos,经 IVIS、免疫荧光、PAS、TEM、WB、qPCR 等进行体内外靶向性、疗效与机制验证。
研究结果
体外实验证实 Treg 与 Treg-Exos 可显著恢复 HG+AGEs 损伤足细胞的 SYNPO、WT1 表达,抑制凋亡、恢复线粒体膜电位与线粒体自噬,关键通过抑制 SRC/FUNDC1 通路实现;miRNA 测序确定 miR-218-5p 为核心效应分子,其在 DKD 患者、模型小鼠及损伤足细胞中显著下调,回补可逆转损伤;双荧光素酶证实 miR-218-5p 直接靶向 TNC,TNC 敲低可模拟外泌体保护效应,过表达则抵消其作用;TNC 通过 TLR4 激活 SRC 磷酸化,进而抑制 FUNDC1 介导的线粒体自噬;工程化 RGD-Treg-Exos 可通过整合素 αvβ3 精准靶向足细胞,较普通外泌体更显著改善足细胞损伤、肾小球系膜扩张、基底膜增厚、足突融合,降低尿白蛋白肌酐比,且安全性良好。
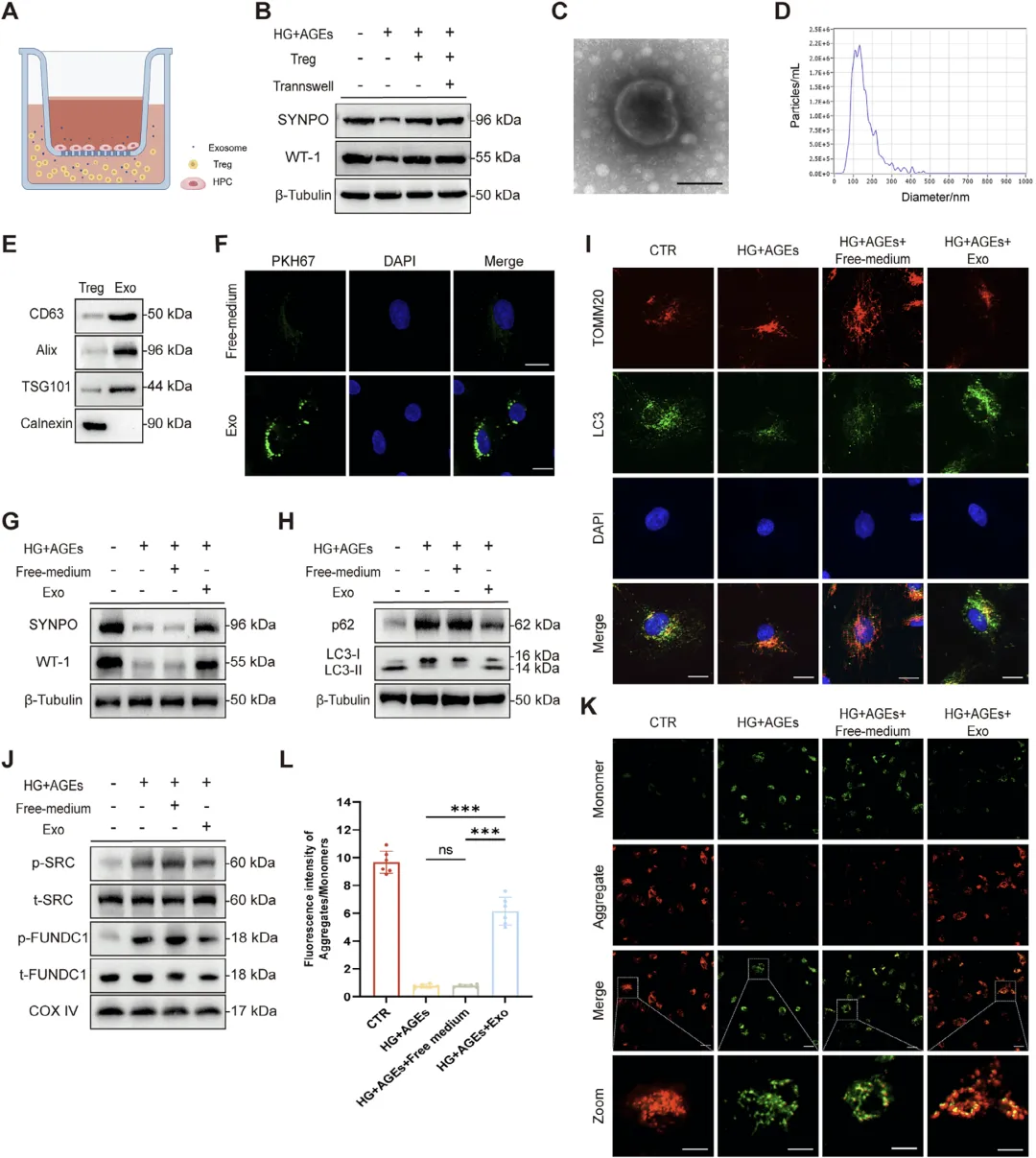
Figure 1:Treg 及 Treg 外泌体可缓解高糖 / 糖基化终产物诱导的足细胞损伤
这组图通过体外细胞实验系统证明调节性 T 细胞(Treg)及其外泌体(Treg‑Exos)对高糖联合糖基化终产物(HG+AGEs)造成的人足细胞损伤具有保护作用,首先利用共培养体系证实 Treg 能够恢复足细胞标志性蛋白 SYNPO 与 WT‑1 的表达并减少凋亡,随后对分离提取的 Treg‑Exos 进行形态、粒径、标志物鉴定,确认其符合外泌体典型特征,再通过荧光标记示踪观察到足细胞可有效摄取 Treg‑Exos,进一步实验发现 Treg‑Exos 能够逆转 HG+AGEs 导致的足细胞标志蛋白下降,降低自噬底物 p62 水平、促进 LC3‑Ⅱ 转化,增强线粒体自噬,同时抑制 SRC/FUNDC1 通路磷酸化,恢复线粒体膜电位,而抑制外泌体分泌后 Treg 的保护作用消失,直接说明 Treg 是通过释放外泌体发挥对足细胞的保护效应。
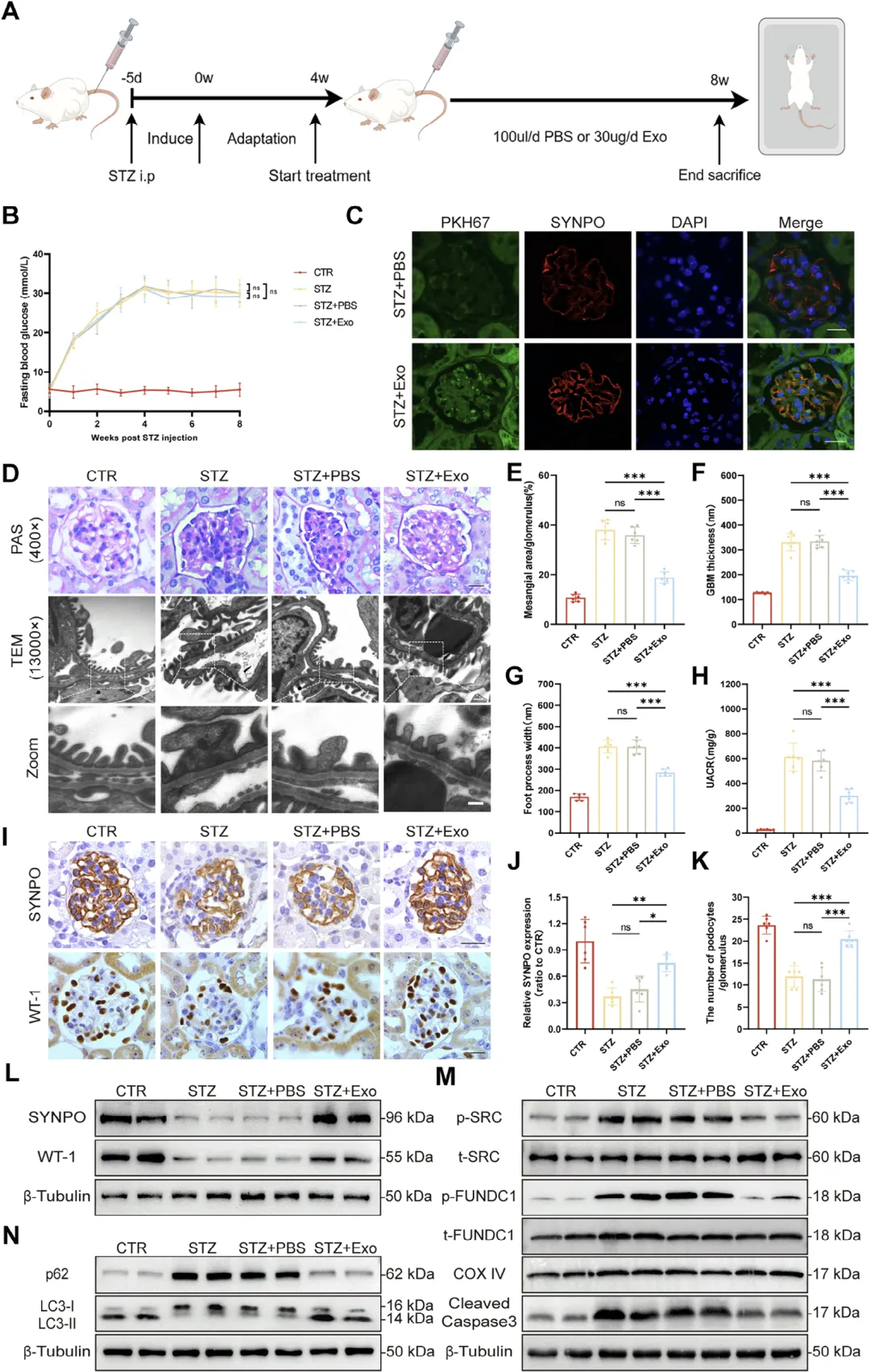
Figure 2:Treg 外泌体在糖尿病小鼠体内可减轻足细胞损伤并改善肾脏病理
这组图以糖尿病肾病小鼠模型为对象,验证 Treg‑Exos 在体内对足细胞及肾脏的保护效果,首先构建糖尿病小鼠模型并给予 Treg‑Exos 尾静脉注射处理,监测发现外泌体处理不影响小鼠血糖水平,通过荧光共定位观察到 Treg‑Exos 能够被小鼠肾脏足细胞摄取,随后 PAS 染色与透射电镜结果显示,Treg‑Exos 可明显改善糖尿病小鼠肾小球系膜增宽、基底膜增厚、足突融合等典型病理改变,同时检测发现外泌体处理后小鼠尿白蛋白肌酐比显著降低,足细胞标志蛋白 SYNPO、WT‑1 表达回升,肾脏组织线粒体自噬水平恢复,凋亡相关蛋白活化受抑,充分证实 Treg‑Exos 在体内可有效缓解糖尿病导致的足细胞损伤与肾脏病变进展。
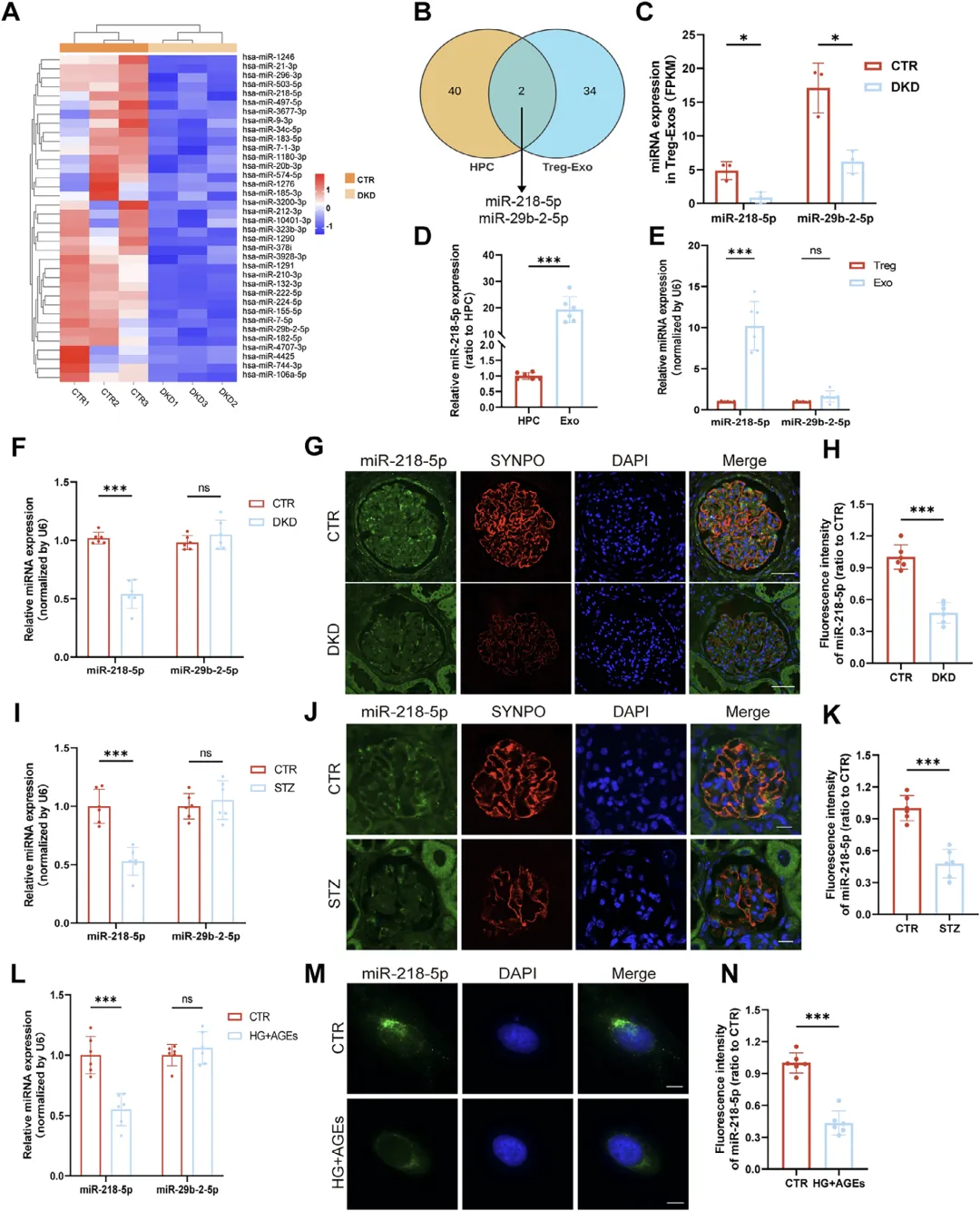
Figure 3:Treg 外泌体通过递送 miR‑218‑5p 发挥对足细胞的保护作用
这组图旨在筛选并确认 Treg‑Exos 发挥保护作用的关键 miRNA 分子,首先对健康人 Treg‑Exos 与 DKD 患者足细胞进行 miRNA 测序,通过交集分析筛选出在受损足细胞中下调、在 Treg‑Exos 中高表达的 miR‑218‑5p 与 miR‑29b2‑5p,经定量检测确定 miR‑218‑5p 在 Treg‑Exos 中显著富集,随后检测发现 miR‑218‑5p 在 DKD 患者肾组织、糖尿病小鼠肾组织及 HG+AGEs 诱导的足细胞中均明显降低,且其表达水平与细胞损伤程度密切相关,这些结果明确指向 miR‑218‑5p 是 Treg‑Exos 介导足细胞保护的核心功能分子,为后续机制探索奠定关键基础。
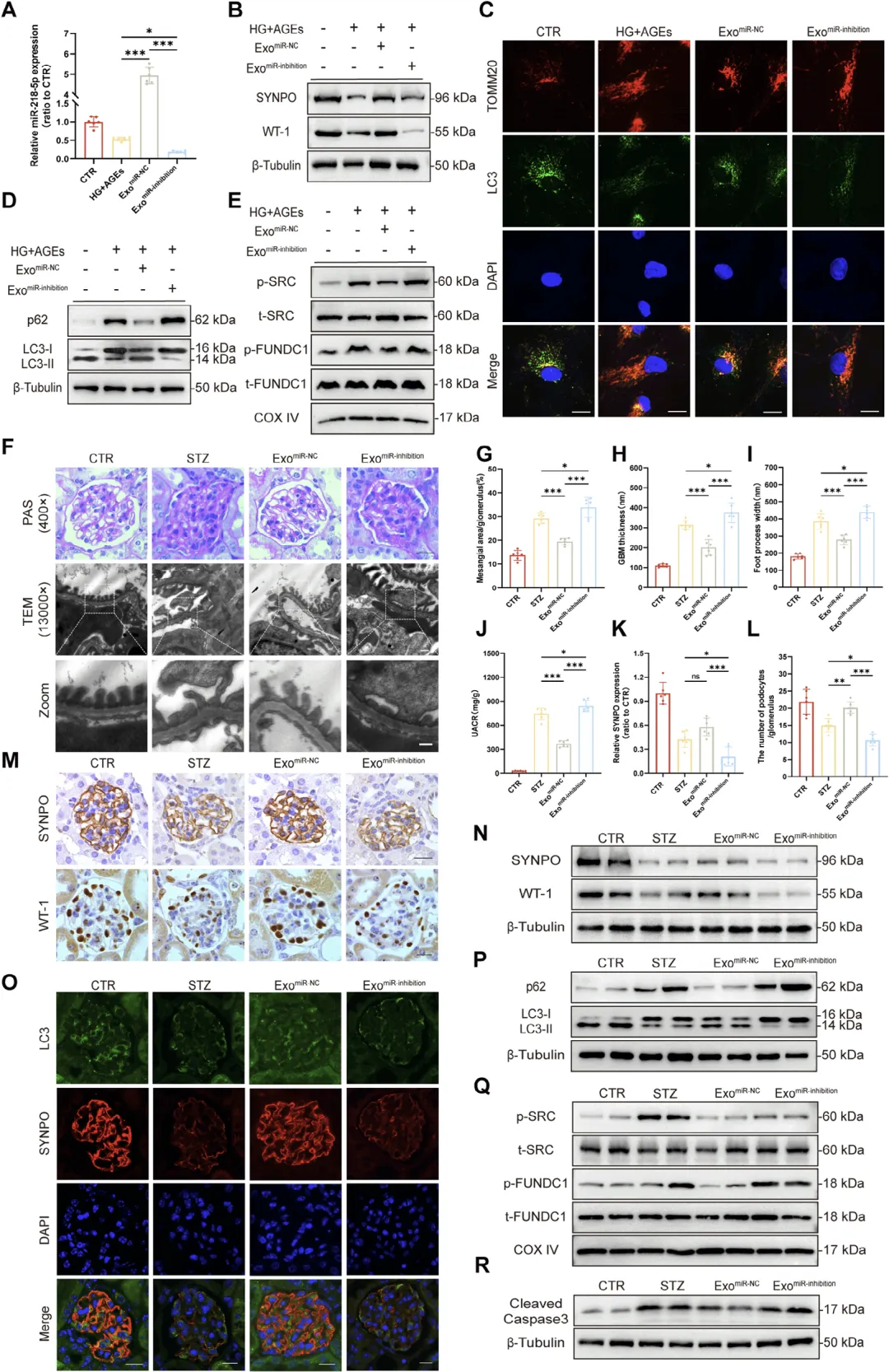
Figure 4:抑制 miR‑218‑5p 可消除 Treg 外泌体对足细胞的保护效应
这组图通过反向验证实验,证实 miR‑218‑5p 是 Treg‑Exos 发挥作用不可或缺的关键因子,体外实验中,使用 miR‑218‑5p 抑制剂沉默 Treg‑Exos 中的 miR‑218‑5p 后,原本 Treg‑Exos 能够恢复的足细胞标志蛋白表达、线粒体自噬水平、线粒体膜电位等保护作用均被完全抵消,足细胞凋亡重新增加;体内实验同样显示,注射低表达 miR‑218‑5p 的 Treg‑Exos 后,糖尿病小鼠的肾小球病理损伤、尿蛋白升高、足细胞标志蛋白下降等问题无法得到改善,线粒体自噬也未恢复,直接证明 miR‑218‑5p 是 Treg‑Exos 保护足细胞的必需元件。
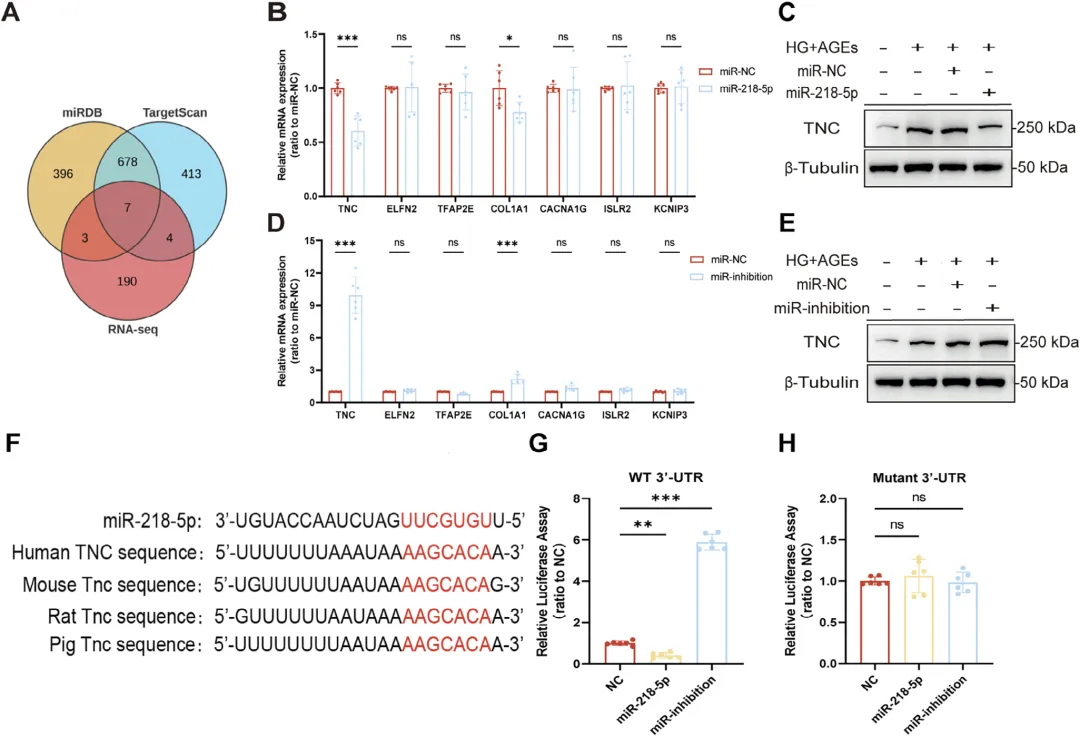
Figure 5:miR‑218‑5p 直接靶向调控 Tenascin‑C(TNC)基因
这组图明确了 miR‑218‑5p 发挥作用的直接靶基因,首先通过生信预测与转录组测序交集筛选出候选靶基因,经 qPCR 与 Western blot 验证,miR‑218‑5p 可显著抑制 TNC 的表达,抑制 miR‑218‑5p 则会使 TNC 水平上升,随后对 TNC 的 3’‑UTR 序列分析发现其存在与 miR‑218‑5p 结合的保守位点,双荧光素酶报告实验进一步证实,miR‑218‑5p 可直接结合野生型 TNC 的 3’‑UTR 并抑制荧光素酶活性,而对突变型结合位点无作用,最终确定 TNC 是 miR‑218‑5p 的直接靶基因,揭示了 Treg‑Exos 调控足细胞的核心分子靶点。
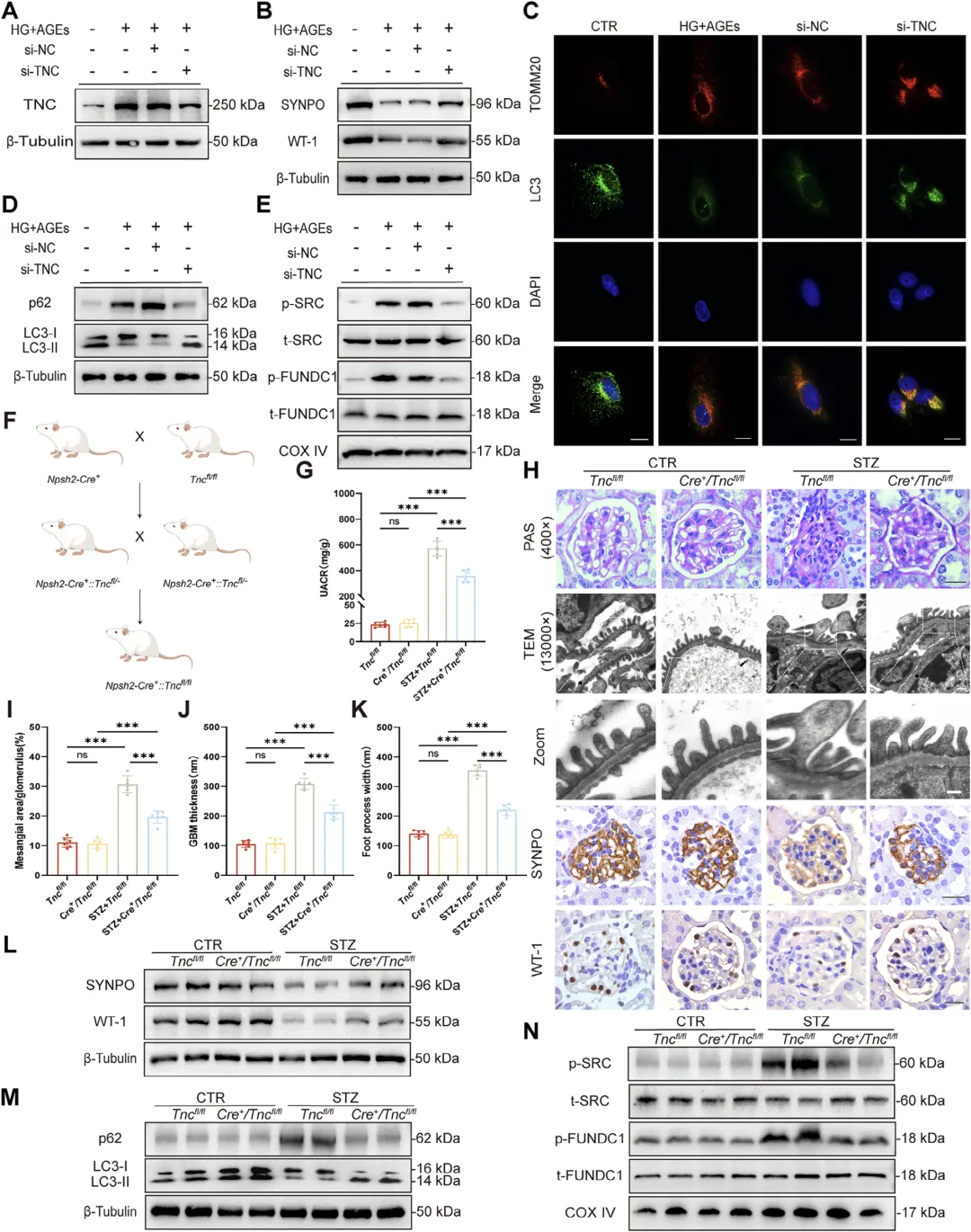
Figure 6:敲低 TNC 可在体内外模拟 Treg 外泌体对足细胞的保护作用
这组图通过功能回复实验验证 TNC 在足细胞损伤中的关键作用,体外实验中,使用 si‑TNC 敲低 HG+AGEs 诱导的足细胞内 TNC 表达后,足细胞标志蛋白 SYNPO、WT‑1 表达回升,线粒体自噬增强,SRC/FUNDC1 通路磷酸化受抑,细胞损伤明显缓解;体内构建足细胞特异性 TNC 敲除糖尿病小鼠,结果显示敲除 TNC 后小鼠尿白蛋白肌酐比降低,肾小球系膜扩张、基底膜增厚、足突融合等病理改变显著减轻,足细胞标志蛋白恢复,线粒体自噬水平提升,充分证明 TNC 是介导 DKD 足细胞损伤的关键分子,抑制 TNC 可直接起到保护足细胞的效果。
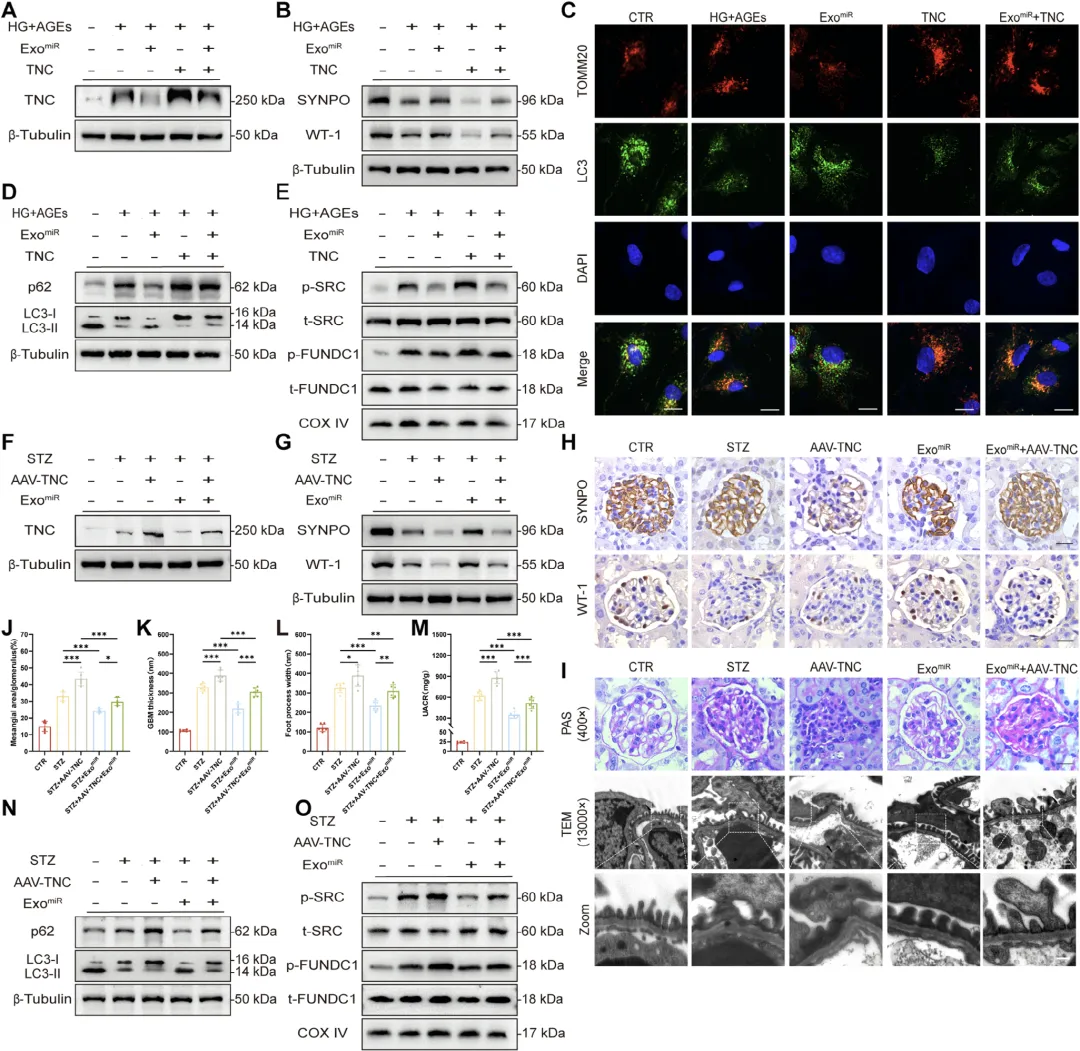
Figure 7:miR‑218‑5p 通过靶向 TNC 调控足细胞线粒体自噬
这组图通过回复实验完整验证 miR‑218‑5p‑TNC 调控轴的功能,体外实验中,过表达 TNC 可逆转高表达 miR‑218‑5p 的 Treg‑Exos 对足细胞的保护作用,导致足细胞标志蛋白下降、线粒体自噬受抑、细胞损伤加重;体内实验中,利用腺病毒在小鼠足细胞过表达 TNC 后,会抵消 Treg‑Exos 的治疗效果,加重肾小球病理损伤与尿蛋白升高,而给予高 miR‑218‑5p 外泌体可部分逆转损伤,同时实验证实 TNC 可结合并激活 TLR4,进而调控下游 SRC/FUNDC1 通路,完整阐明 miR‑218‑5p 通过靶向 TNC 调控 TLR4/SRC/FUNDC1 通路影响线粒体自噬的分子机制。
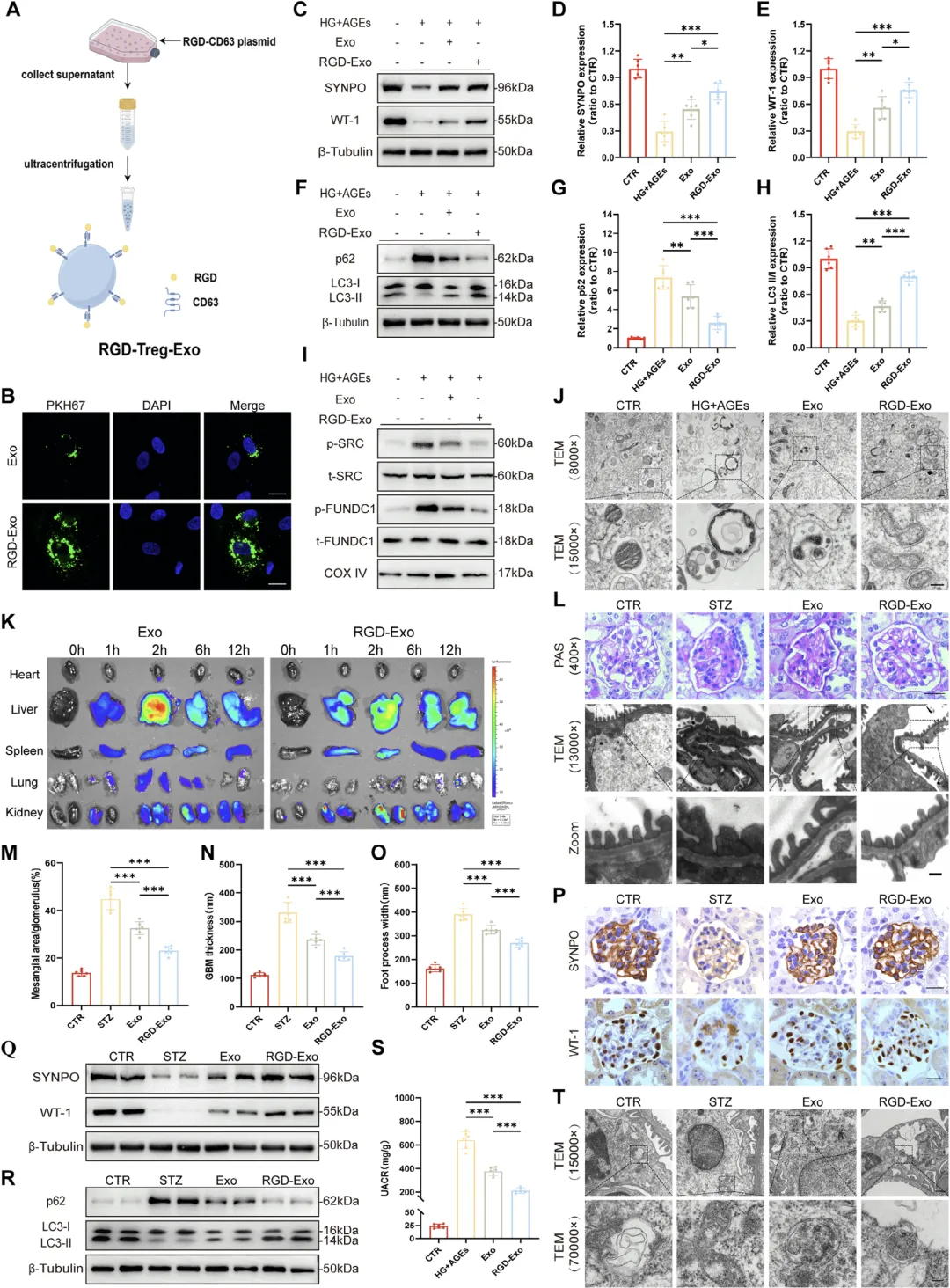
Figure 8:RGD 修饰工程化 Treg 外泌体可更高效靶向足细胞并增强保护效果
这组图展示工程化改造外泌体的优势与作用,通过在 Treg‑Exos 膜表面融合 RGD 肽构建靶向性工程外泌体(RGD‑Treg‑Exos),鉴定显示 RGD 修饰不改变外泌体基本结构,体外实验证实 RGD‑Treg‑Exos 可通过足细胞表面整合素 αvβ3 被更高效摄取,相比普通外泌体,其恢复足细胞标志蛋白、增强线粒体自噬、改善线粒体形态、抑制凋亡的效果更显著;体内活体成像显示 RGD‑Exos 更多富集于肾脏,荧光切片确认其靶向足细胞,进一步病理与功能检测表明,RGD 修饰可显著提升外泌体对糖尿病小鼠肾小球损伤、足突融合、尿蛋白升高等问题的改善效果,证明工程化改造能大幅增强外泌体的靶向性与治疗效能。
研究结论
本研究证实调节性 T 细胞外泌体可通过递送 miR-218-5p,靶向抑制 TNC/TLR4/SRC/FUNDC1 信号轴,恢复糖尿病肾病足细胞线粒体自噬水平,减少细胞凋亡与肾小球病理损伤;RGD 肽修饰的工程化外泌体可显著提升足细胞靶向递送效率,增强治疗效果。该研究阐明了 Treg-Exos 保护 DKD 足细胞的全新分子机制,建立了靶向足细胞的工程化外泌体无细胞治疗策略,为糖尿病肾病的精准治疗提供了实验依据与潜在转化方向。
局限性:仅在细胞与小鼠模型验证,未开展大动物与临床研究;外泌体制备工艺与质控标准待优化。展望:推进 RGD-Treg-Exos 临床前研究,优化工程化外泌体规模化生产;探索联合用药方案,拓展其在其他肾脏疾病中的应用。
参考文献
#糖尿病肾病#足细胞损伤#线粒体自噬#调节性T细胞外泌体#miR2185p#RGD修饰#TNC#靶向递送

国家杰青一对一答疑视频
医学省自然申请答疑,立项的关键条件是哪一些?从哪些方向可以杀出重围
临床型博士如何准备国青标书?没有预实验怎么办?专家一对一解答规划
中医药科研研究