PNAS |南京农大团队揭示菊花舌状花发育核心调控机制
- 2026-05-09 16:19:48
点击“蓝字” 关注我们
合瓣花(花瓣合生)是被子植物进化中多次出现的关键形态创新,其形成分为两种发育途径:晚期合瓣(花瓣原基初始分离,后期合生)与早期合瓣(直接由环状合生原基发育)。目前,早期合瓣类群中花冠筒形成的遗传基础仍不明确。菊花作为典型早期合瓣植物,其舌状花花冠筒的形成特异性依赖背瓣伸长。
2026年4月27日,南京农业大学陈发棣教授团队在国际学术期刊PNAS上发表了题为“An auxin-induced transcriptional cascade CmBES1-CmSAUR66 orchestrates the ray floret development in Chrysanthemum morifolium”的研究论文。该研究揭示了生长素介导的CmBES1-CmSAUR66转录级联调控菊花舌状花花冠筒形成的关键机制,解析了被子植物早期合瓣花花冠筒发育的分子调控通路,为深入理解合瓣花冠建成与生长素信号的调控机制提供了新见解。


材料方法
GWAS:200份菊花种质,GBS测序;
过表达验证:通过农杆菌介导的叶盘法,构建amiR-CmSAUR66沉默株系与CmBES1过表达株系;
基因表达分析:RT-qPCR与RNA原位杂交;
蛋白-DNA 互作:酵母单杂交、EMSA、ChIP-qPCR、双荧光素酶报告实验。

主要研究结果
1. CmSAUR66与菊花舌状花类型相关
本研究对200份切花菊种质的舌状花类型进行评估,发现花冠筒融合度呈连续变异。GWAS分析共鉴定到7个控制舌状花类型的QTN,在每个QTN的200 kb侧翼区间内共筛选到103个候选基因。结合6份不同瓣型菊花(3平瓣、3管瓣)的转录组数据,进一步筛选出8个差异表达基因,其中23号染色体上的生长素响应基因evm.TU.scaffold_1113.140位于最显著SNP(Chr23_209783790)侧翼,成为核心候选。
基因型分析显示,该位点A/C多态性与花冠筒融合度显著相关,管瓣种质更倾向携带A/C杂合基因型。RT-qPCR验证表明,该基因在平瓣舌状花中的表达量显著高于管瓣,提示其负调控菊花花冠筒融合,决定舌状花类型。
序列比对显示,该基因编码典型SAUR蛋白,含SAUR保守结构域;进化树分析表明其与拟南芥AtSAUR66同源性最高,故命名为CmSAUR66。菊花叶肉原生质体瞬时表达实验显示,CmSAUR66定位于细胞质膜,与多数拟南芥SAUR蛋白的亚细胞定位一致。
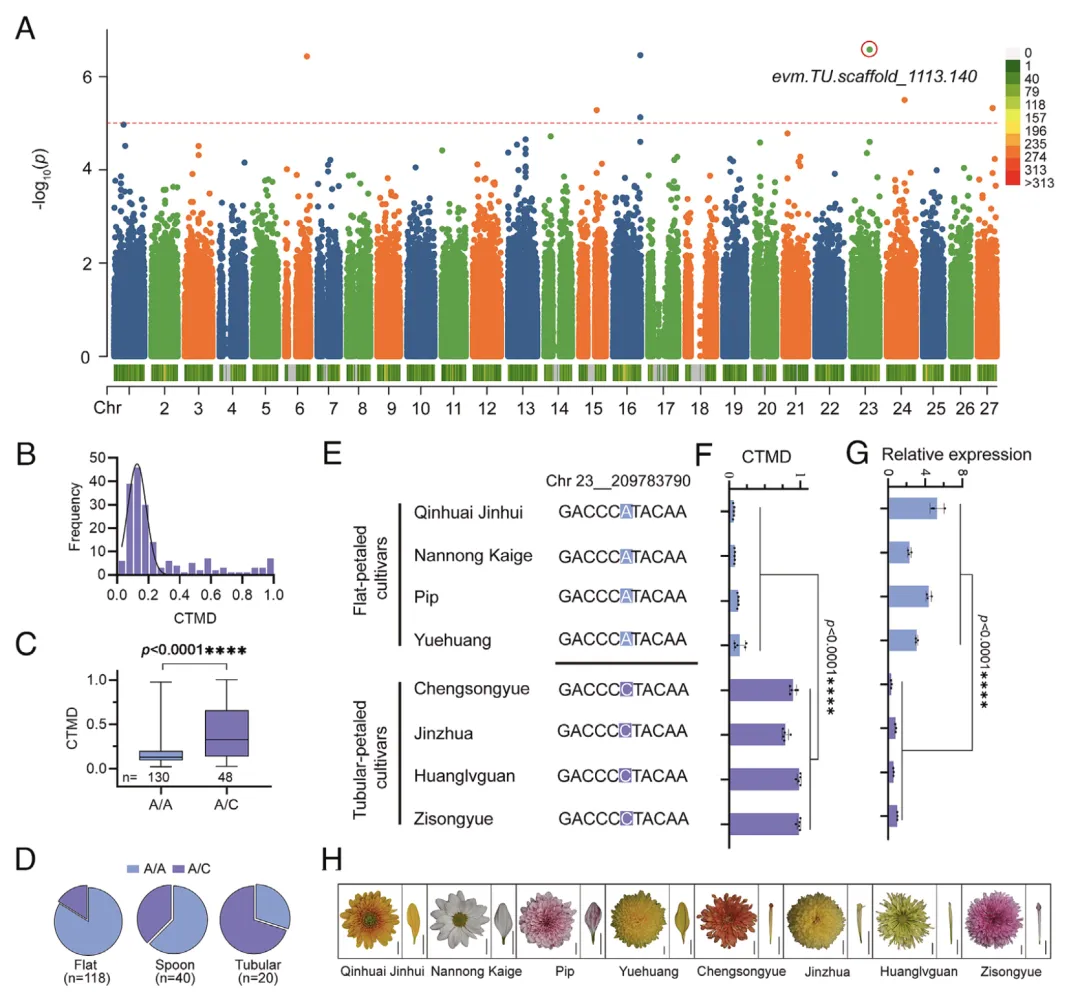
图1 evm.TU.scaffold_1113.140为菊花舌状花形态的候选调控因子
2. CmSAUR66通过抑制背瓣发育调控花冠筒融合
为解析CmSAUR66的功能,构建amiR-CmSAUR66沉默载体并转化。与野生型(WT)相比,沉默株系舌状花瓣中CmSAUR66表达量下调49.3%~69.1%,花冠筒融合度显著提升,外层轮舌状花的融合增强最为明显,且融合度仍保持由外至内递减的梯度特征。
沉默CmSAUR66还会抑制头状花序直径与舌状花大小,细胞学观察显示,决定舌状花长度的腹瓣细胞数量与平均长度均显著减少。对4 mm、6 mm直径的早期花序进行体视镜与扫描电镜观察发现:野生型4 mm花序的舌状花背瓣原基停止伸长,仅腹瓣原基正常发育;而amiR-5株系的背瓣原基持续发育,与腹瓣同步伸长,最终导致花冠筒融合度升高。
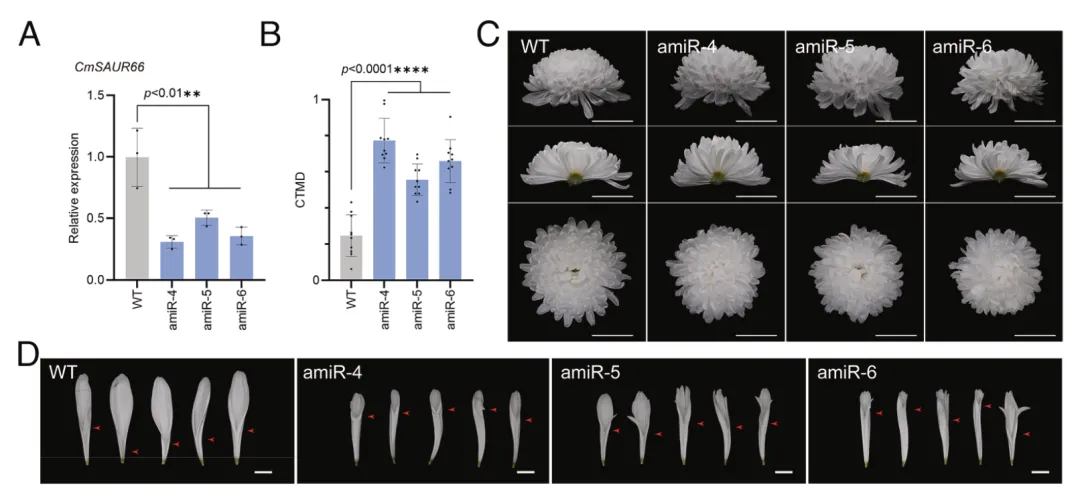
图2 CmSAUR66负调控菊花的花冠筒融合
3. CmSAUR66通过调控CmCYC2c的背腹不对称分布调控花冠筒发育
RNA原位杂交显示,CmSAUR66在花发育Ⅲ期均匀分布于背、腹瓣原基及雄蕊原基;Ⅳ~Ⅴ期腹瓣显著伸长、雌蕊起始后,CmSAUR66在雌蕊中表达增强,仍均匀分布于背、腹瓣,无明显表达差异。结合CmSAUR66沉默促进背瓣伸长、抑制腹瓣生长的表型,推测其通过在背、腹瓣中结合不同互作蛋白实现功能分化。
CYC2类TCP基因是菊科花冠形态建成的核心调控因子,异位表达可诱导管瓣花形成。RT-qPCR结果显示,CmSAUR66沉默显著上调CmCYC2c表达。原位杂交进一步验证:野生型中CmCYC2c在Ⅳ~Ⅴ期背瓣表达减弱、腹瓣持续表达,对应背腹瓣不对称形态;而amiR-5株系中,CmCYC2c在Ⅳ~Ⅴ 期背、腹瓣中持续表达,这种异位表达促使背、腹瓣同步伸长,最终形成管瓣花冠筒。
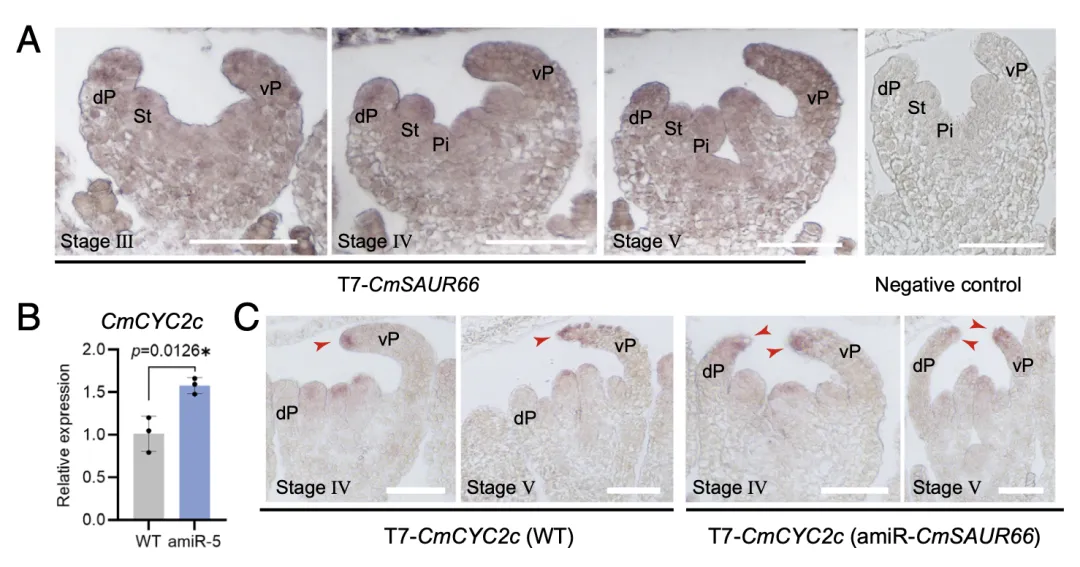
图3 CmSAUR66 通过CmCYC2c 调控花器官背腹不对称性
为明确遗传互作关系,在amiR-CmSAUR66转基因株系中瞬时沉默CmCYC2c,结果显示花冠筒融合度显著降低,CTMD值从0.72 降至0.45,证实CmSAUR66通过CmCYC2c部分调控舌状花花冠筒发育。
4. CmSAUR66调控生长素介导的花冠筒发育
SAUR基因为早期生长素响应基因,CmSAUR66启动子含经典生长素响应元件。对2 mm直径的菊花花序进行10 μM生长素(IAA)处理,发现CmSAUR66在处理2分钟后快速诱导表达,30分钟达到峰值,符合典型SAUR基因的生长素快速响应特征。
外源生长素处理实验显示,10 μM IAA持续处理可显著促进花冠筒融合,CTMD值从0.17 升至0.75;20 μM IAA处理效果减弱,同时诱导中心管状花向舌状花转化。生长素处理后,CmSAUR66表达显著被抑制,与其负调控花冠筒融合的功能一致。
对amiR-5株系进行10 μM IAA处理,发现沉默株系的花冠筒融合度无显著变化,生长素诱导的CTMD提升效应被大幅削弱,证实敲降CmSAUR66降低了植株对生长素的敏感性,CmSAUR66是生长素调控花冠筒发育的核心因子。
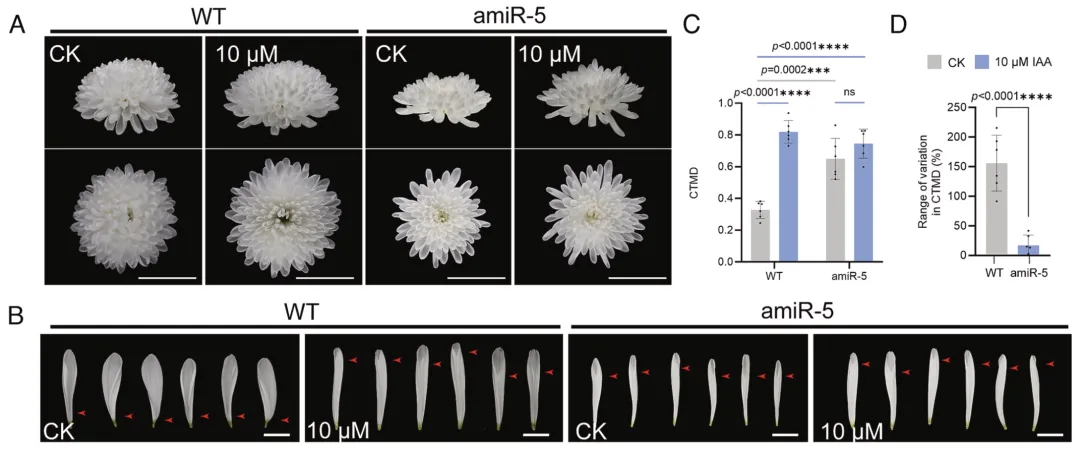
图4 敲除CmSAUR66会降低植株对生长素的敏感性
5.生长素诱导的CmBES1直接抑制CmSAUR66表达
CmSAUR66对瞬时与持续生长素处理的相反表达模式,提示持续生长素信号下存在其他调控因子。通过酵母单杂交(Y1H)文库筛选,从8 个候选上游转录因子中鉴定到CmBES1(已知正调控舌状花花冠筒发育)。Y1H、染色质免疫共沉淀(ChIP)、凝胶迁移实验(EMSA)共同证实:CmBES1可直接结合CmSAUR66启动子的E-box 元件(CATGTG)。
双荧光素酶报告实验与RT-qPCR 显示,CmBES1过表达显著抑制CmSAUR66的转录;持续生长素处理可显著上调CmBES1表达,表明生长素通过诱导CmBES1,直接抑制CmSAUR66表达。
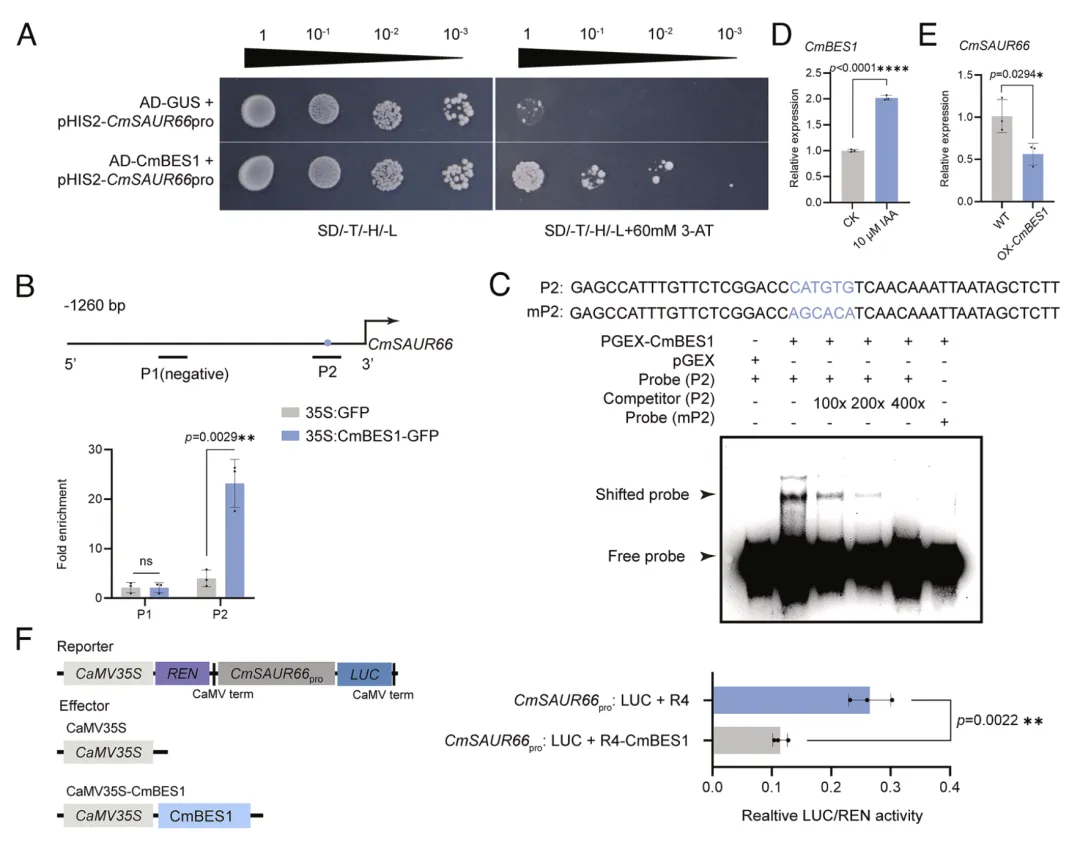
图5 CmBES1通过直接结合启动子,在转录水平上抑制CmSAUR66
6. CmSAUR66在CmBES1调控花冠筒形成中呈上位效应
为解析CmBES1与CmSAUR66的遗传互作,在CmBES1过表达株系中瞬时过表达CmSAUR66,结果显示花冠筒融合表型被显著回补,CTMD 值从0.91 降至0.43,证实CmBES1部分依赖CmSAUR66调控花冠筒发育,CmSAUR66对CmBES1呈上位效应。
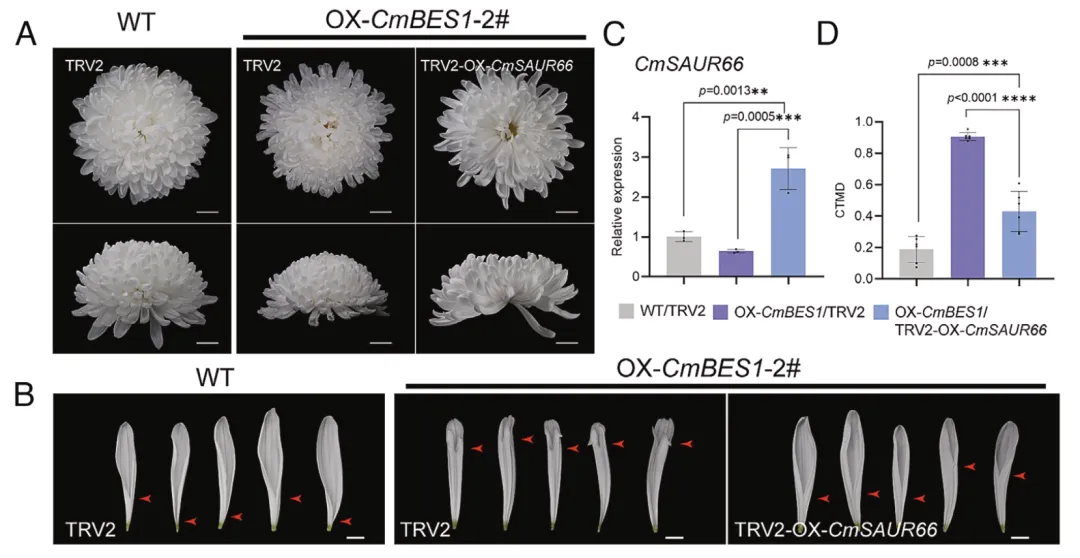
图6 在调控花冠筒融合的通路中,CmSAUR66位于CmBES1的下游发挥作用

小结
菊花作为重要经济作物,兼具观赏、药用、食用价值,基因组已解析、种质资源丰富,且花冠筒融合性状呈连续变异,是通过正向遗传学解析合瓣发育的理想材料。本研究以200份菊花自然种质为材料,通过GWAS与转录组联合分析,鉴定到调控舌状花花冠筒融合的关键基因CmSAUR66,并通过遗传转化、时空表达分析、外源生长素处理与生化实验,阐明了CmBES1–CmSAUR66模块通过调控CmCYC2c的背腹不对称分布,介导生长素调控早期合瓣花冠筒形成的分子机制。
参考文献
Jia D, Zhang Y, Su J, et al. An auxin-induced transcriptional cascade CmBES1-CmSAUR66 orchestrates the ray floret development in Chrysanthemum morifolium. Proc Natl Acad Sci U S A. 2026 May 5;123(18):e2527961123.
往期回顾

