IF 10.6,苏州市立医院 4 样本空转 + 6 个公共数据,斩获 10.6 分 KRAS 突变 CRC 研究
单细胞联合空间转录组,堪称顶刊“黄金组合”!不过随着技术普及,单纯依赖公共数据挖掘想冲击顶刊难度渐增(6分+期刊用公共数据依然稳妥)。这时,“公共数据+小样本自测序”的混搭模式就成了最优解——既保证创新高度,又能节省测序成本,性价比拉满!
之前给大家分享过不少“单细胞自测序+空间转录组公共数据”的案例,近期发现“单细胞公共数据+空间转录组自测序”的思路越来越火:样本量要求更低,创新点更突出,特别适合想冲刺顶刊的朋友~ 今天科信服给大家举个实操案例:一篇发表在1区顶刊《Journal for ImmunoTherapy of Cancer》(IF=10.6)的研究,聚焦KRAS突变结直肠癌的内部异质性,就用了这个混搭思路! 选题是单细胞领域经典的异质性分析,为了提升顶刊竞争力,设计了“单细胞公共数据整合+空间转录组自测序+小鼠模型单细胞验证”的闭环方案:整合6个公共数据库的单细胞数据,搭配4个结直肠癌样本的空间转录组自测序数据,再用小鼠模型的单细胞自测序做功能验证。这样的设计,既靠多源数据撑起了顶刊所需的研究体量,自测序样本量又可控,性价比超高!而且文中的单细胞和空间转录组分析做得全面扎实~ 最后通过小鼠模型测序和免疫组化验证,形成“数据分析-功能验证”的完整逻辑链,干湿结合的模式,直接给顶刊冲刺再加一层buff!如果您在方案设计或生信分析上遇到难题,不妨联系科信服!咱们团队拥有十余年技术沉淀,能提供从个性化思路设计到完整生信分析的一站式服务,助力您高效产出高分成果!中文题目:单细胞和空间转录组分析识别了KRAS突变结直肠癌中的免疫抑制空间生态位
发表期刊:J Immunother Cancer
发表时间:2026年12月
KRAS是结直肠癌(CRC)中最常突变的基因之一,在肿瘤发生、进展、免疫逃避和治疗耐药性中起着关键作用。KRAS突变CRC中显著的异质性凸显了对更精准和个性化治疗方法的紧迫需求。1. 样本与数据来源
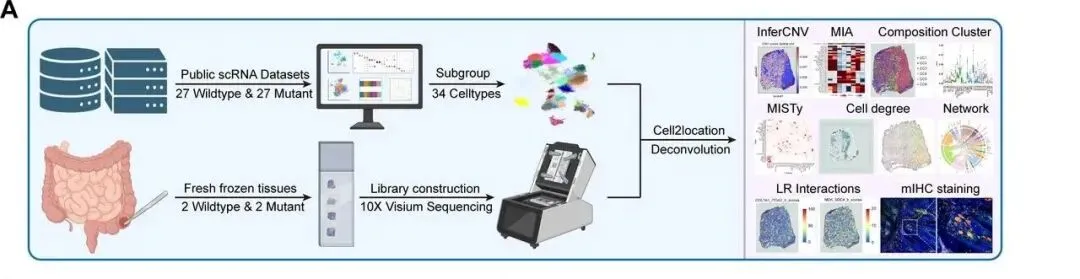
- 临床样本:收集 4 例结直肠癌患者手术切除组织(2 例 KRAS 突变、2 例野生型),整合 6 个公共数据库(GSE132465 等)的 27 例突变型、27 例野生型结直肠癌 scRNA-seq 数据。
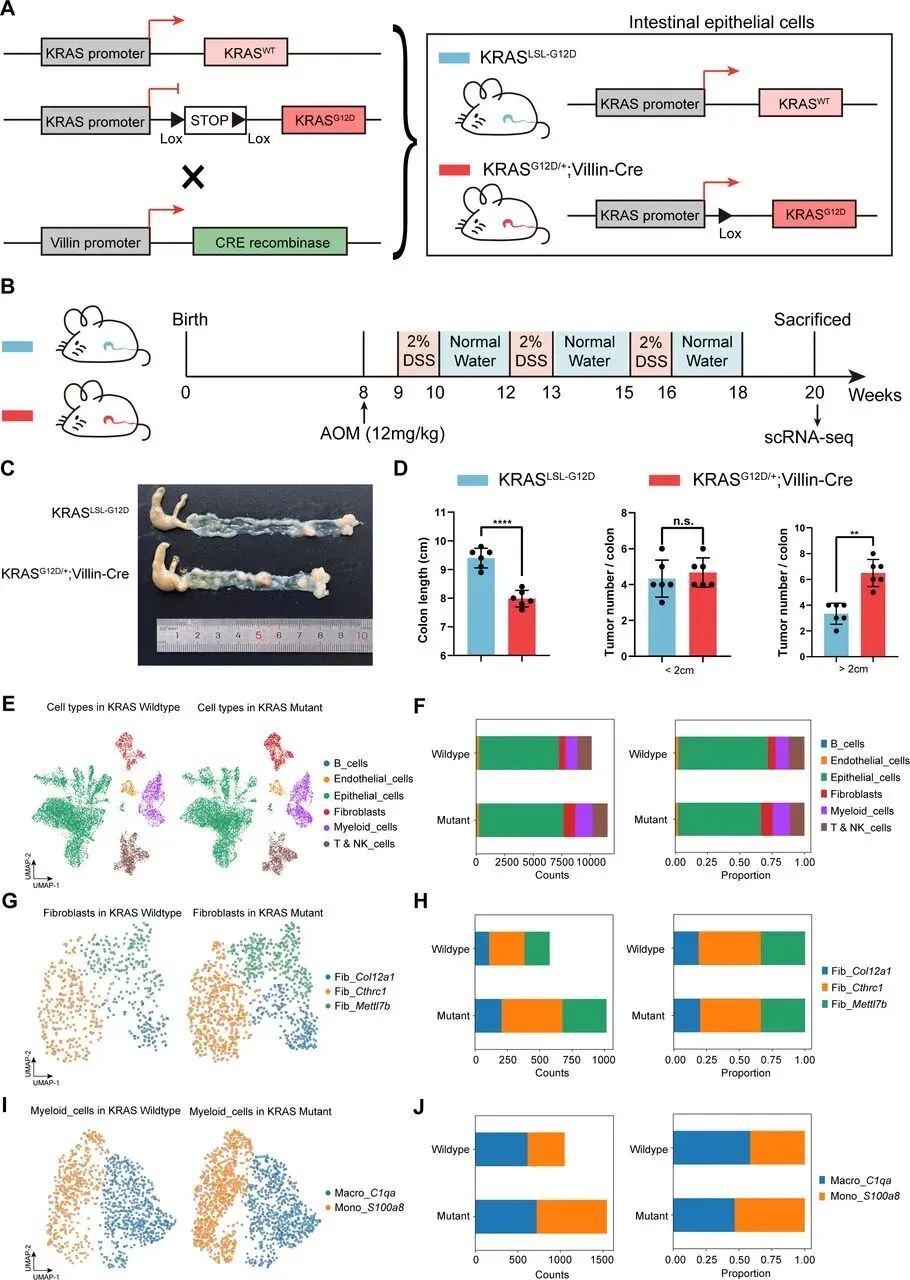
- 动物模型:构建 KRASG12D/+; Villin-Cre 条件性敲除小鼠,经 AOM/DSS 诱导建立结直肠癌模型,获取肿瘤组织进行 scRNA-seq。
2. 测序与实验技术
- 空间转录组:采用 10x Genomics Visium 平台对冷冻组织切片测序,结合 H&E 染色评估组织形态。
- 单细胞测序:对临床样本和小鼠肿瘤组织进行 scRNA-seq,捕获单细胞基因表达特征。
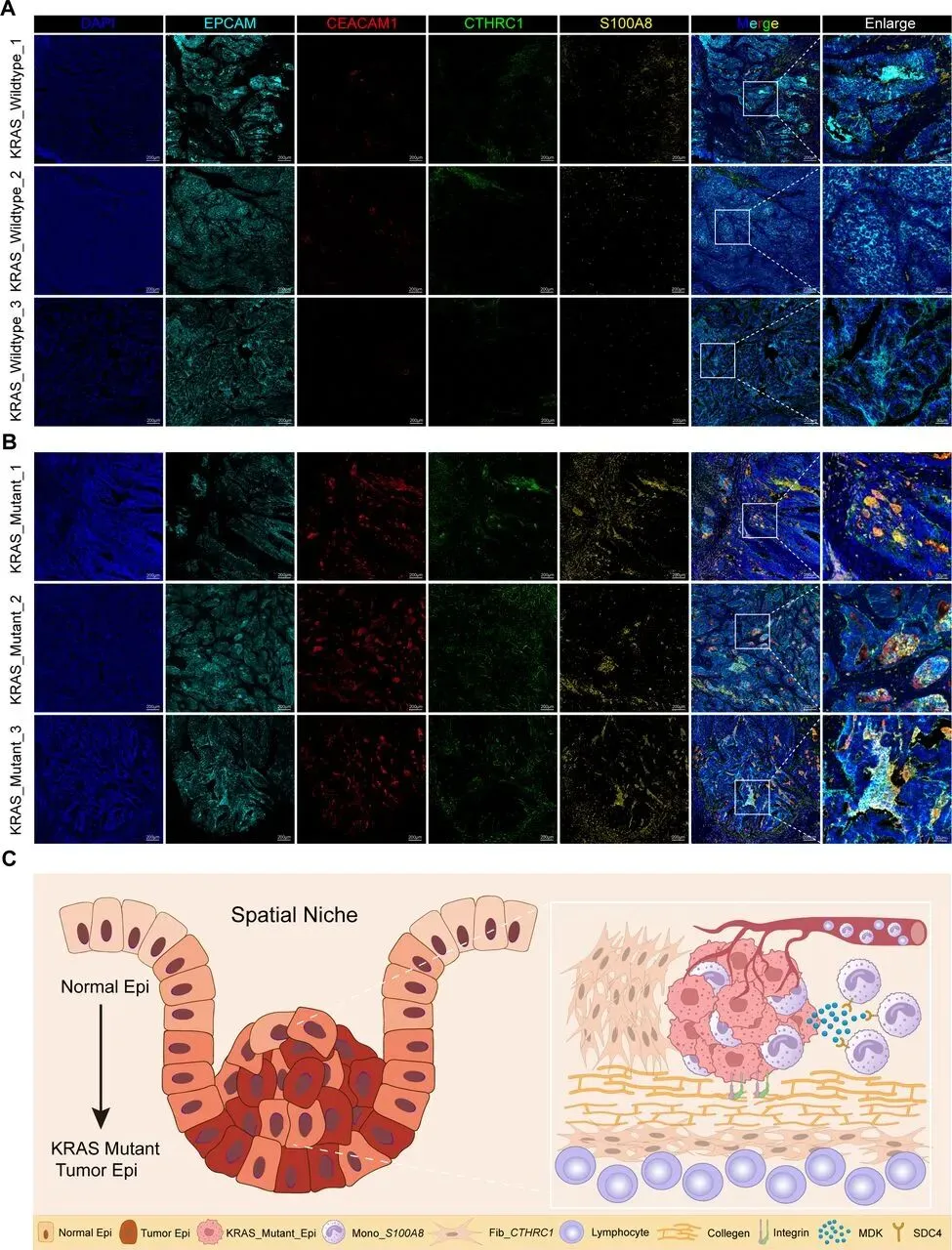
- 多重免疫组化(mIHC):针对 CEACAM1、CTHRC1、S100A8 等标志物进行 TSA 荧光染色,验证细胞共定位。
3. 数据分析工具与流程
- 数据预处理:使用 Scanpy、Seurat 进行质控、归一化和批次效应校正(Harmony),Scrublet 去除双细胞。
- 细胞聚类与注释:通过 Leiden 算法聚类,依据经典标志物注释 34 个细胞亚群,UMAP 可视化。
- 空间与细胞互作分析:用 Cell2location 进行细胞类型解卷积,CellChat、stLearn 分析配体 - 受体互作,MISTy、ISCHIA 解析空间依赖关系与细胞生态型。
- 功能与临床关联分析:通过 ssGSEA、InferCNV 分析基因富集与拷贝数变异,结合 TCGA-COADREAD 队列分析临床预后与化疗敏感性。
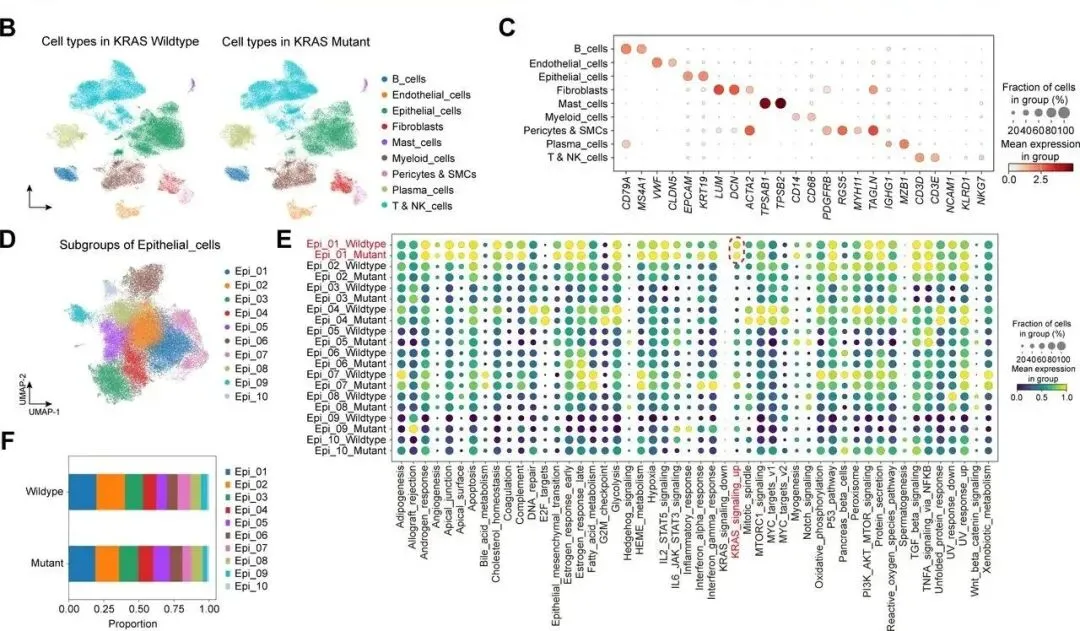
整合 27 例 KRAS 野生型与 27 例突变型 CRC 公开 scRNA-seq 数据,经质控(去双细胞、筛低质量细胞)获 136,890 个高质量细胞,聚类注释出 8 类主要细胞类型;上皮细胞细分 10 亚群,Epi_01 的 KRAS 信号评分最高(突变型 > 野生型),为 KRAS 突变相关上皮细胞(标志物 CEACAM1),其在两组中比例相近,提示 KRAS 突变可能通过重塑 TME 发挥作用。Fib_CTHRC1和Mono_S100A8在KRAS突变CRC中发挥关键作用
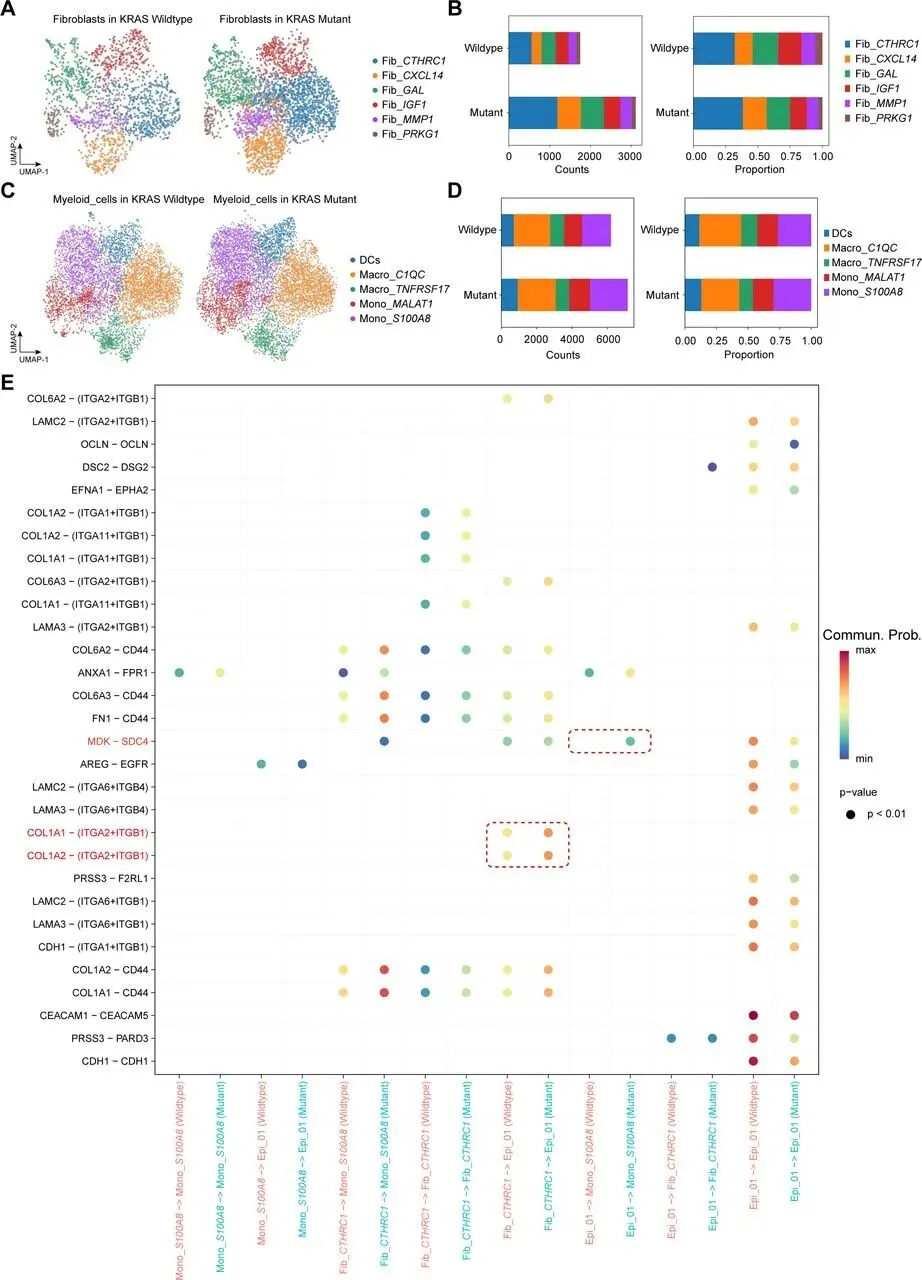
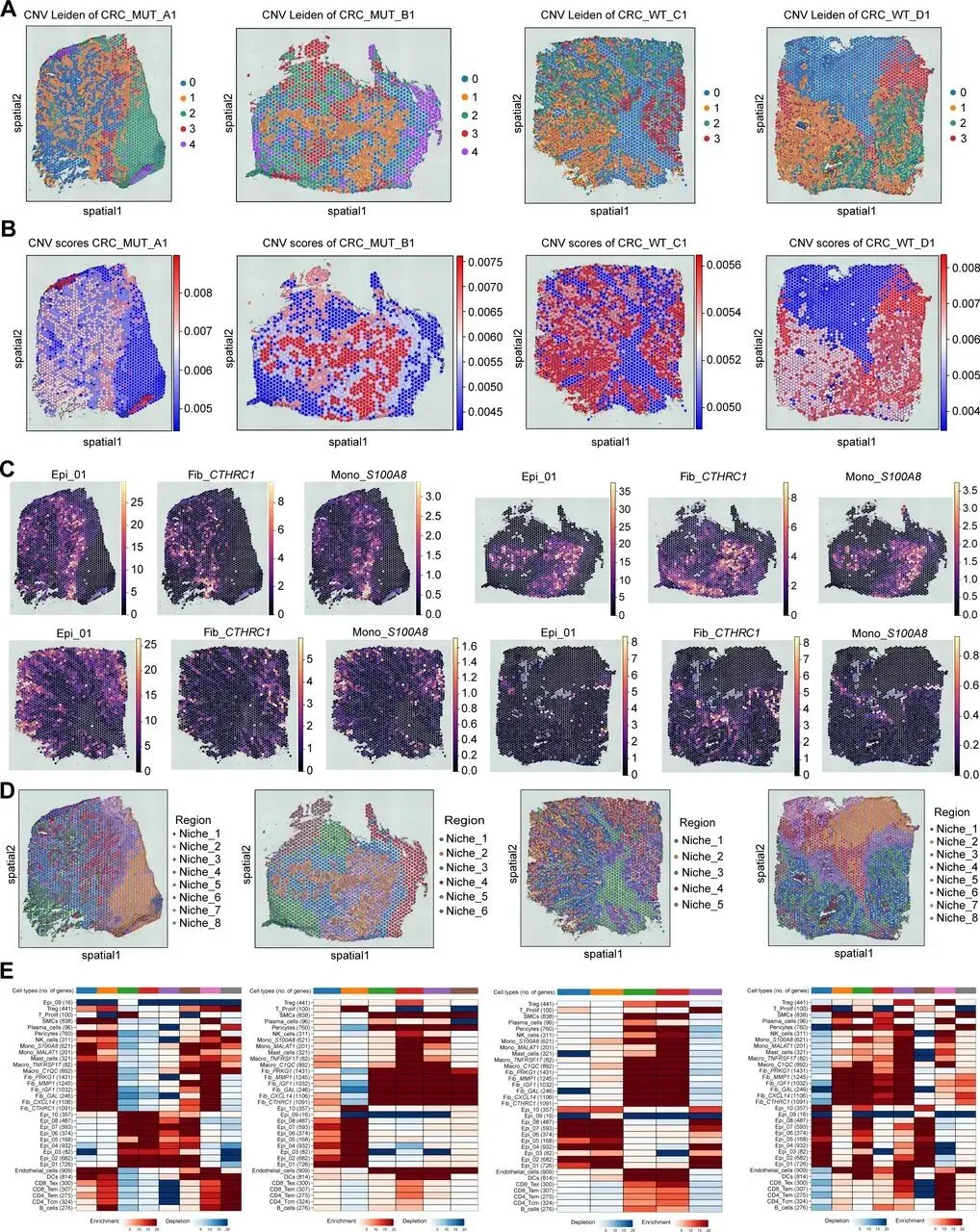
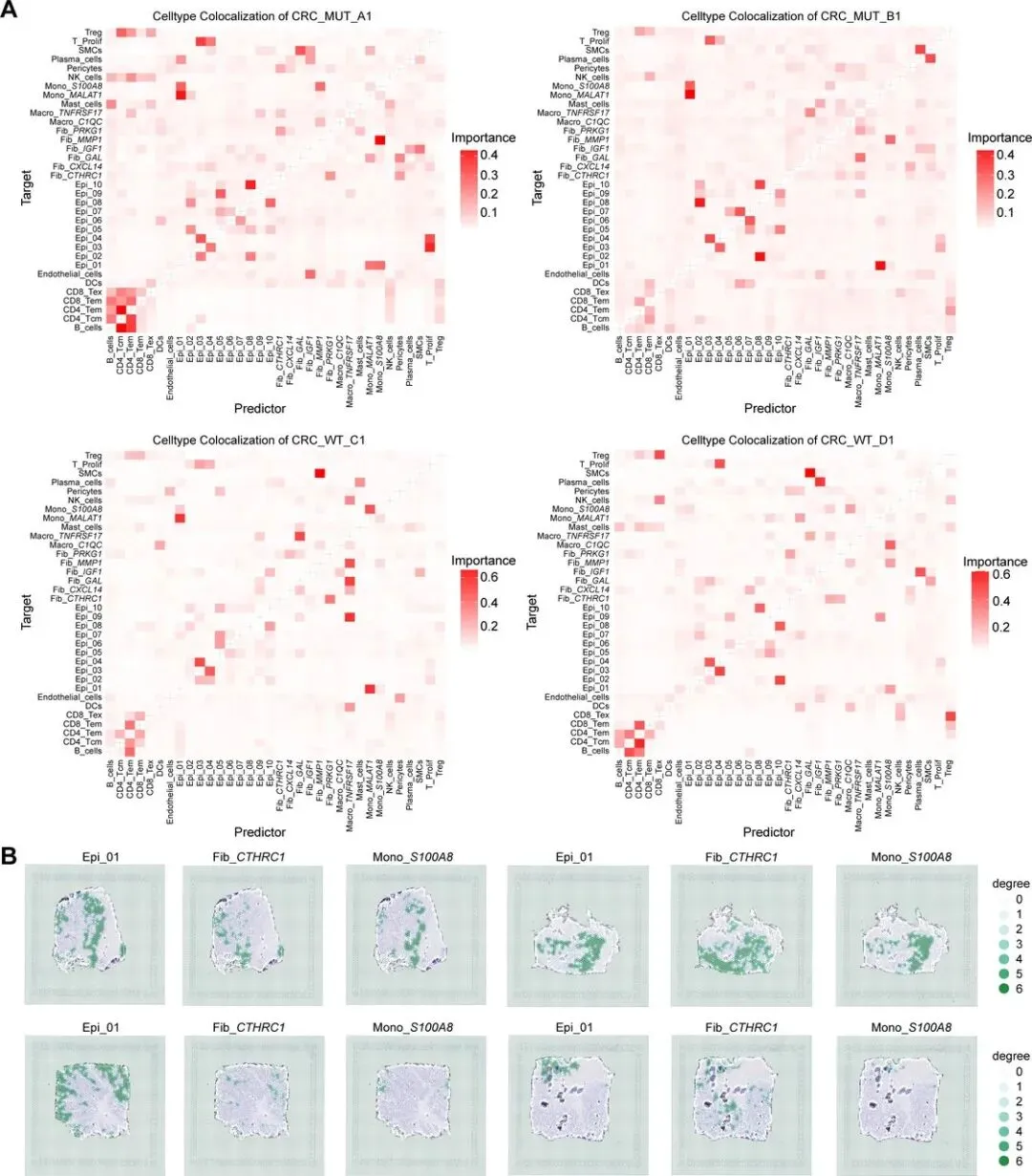
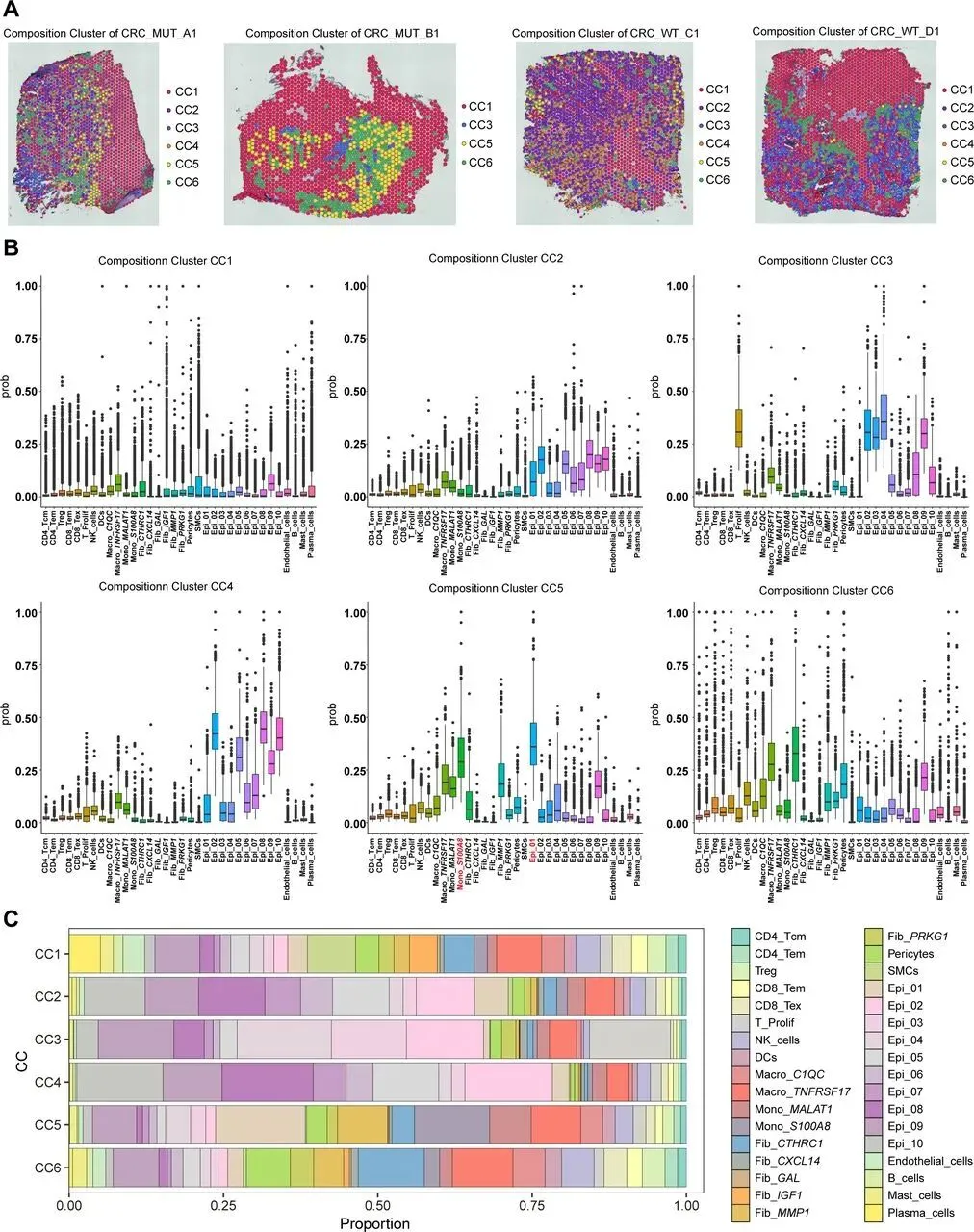
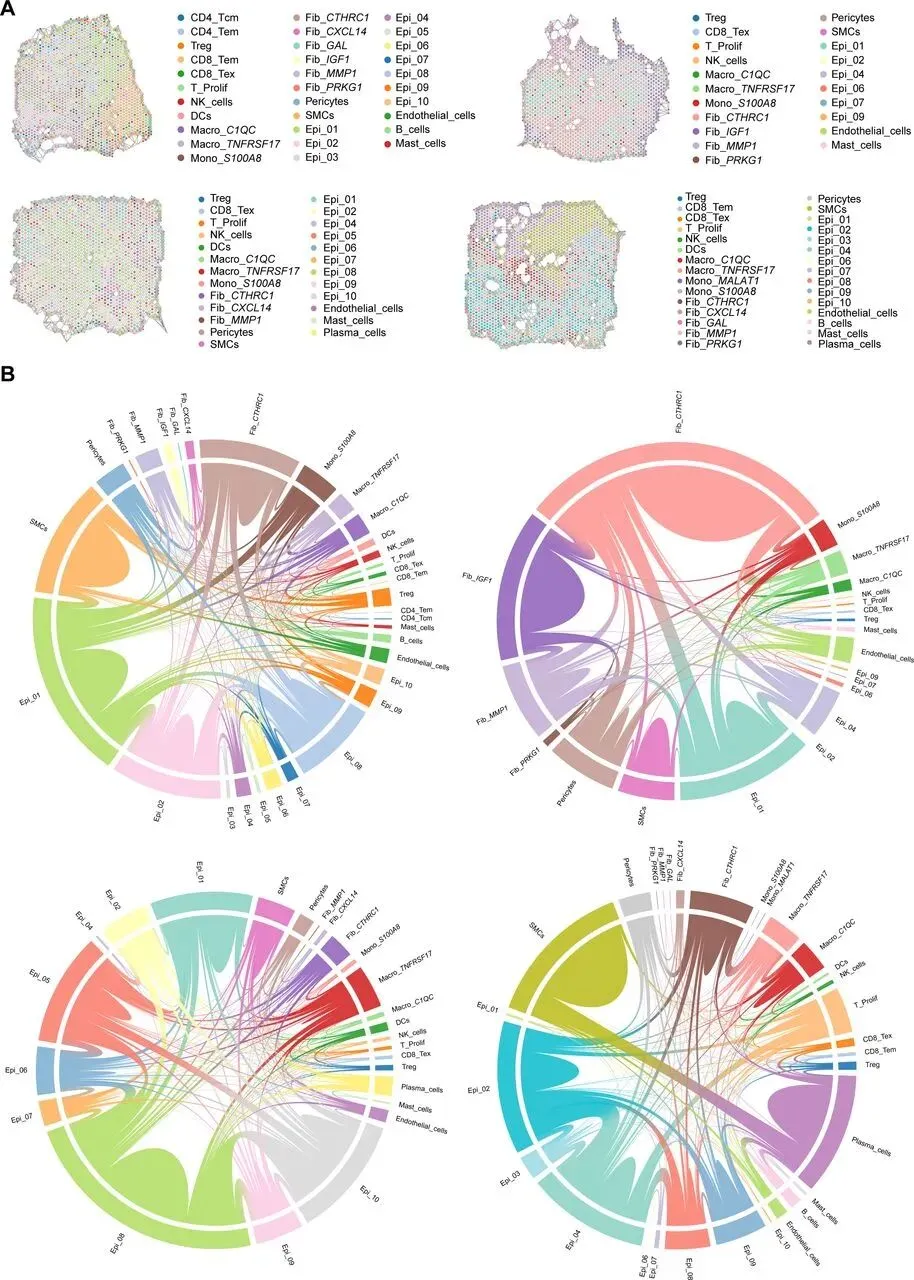
分析 KRAS 野生型与突变型 CRC 的 TME 差异,发现突变组成纤维细胞和髓系细胞比例显著更高,对二者进一步亚聚类:成纤维细胞分为 6 个亚群,其中 Fib_CTHRC1 比例差异最大且最丰富;髓系细胞分为 5 个亚群,Mono_S100A8 比例差异最显著,二者均为突变型 TME 关键细胞。通过 CellChat 分析,突变组中 Epi_01 释放 MDK 配体结合 Mono_S100A8 的 SDC4 受体,Fib_CTHRC1 分泌 COL1A1/COL1A2 结合 Epi_01 的 ITGA2/ITGB1 受体。临床关联显示,Epi_01、Fib_CTHRC1、Mono_S100A8 高表达均与患者不良预后相关,且在化疗不敏感肿瘤中丰度显著升高;Epi_01 和 Fib_CTHRC1 还与肿瘤晚期分期、淋巴结转移相关,Mono_S100A8 主要通过构建免疫抑制微环境促进治疗耐药和转移。为分析肿瘤异质性与治疗耐药的关联,本研究以高表达免疫标志物的位点为参考,通过 inferCNV 方法评估各位点 CNV 状态。Leiden 聚类显示,KRAS 突变组肿瘤有 5 个 CNV 状态亚组,多于野生型的 4 个,提示其异质性更高;空间转录组分析中,高 CNV 评分区域对应肿瘤区、低评分对应基质区,且突变型各微环境的平均 CNV 水平有特征差异,表明 KRAS 突变肿瘤恶性程度和治疗抵抗性更强。利用含 34 种细胞亚型的 scRNA-seq 数据集,通过 Cell2location 算法对 ST 数据去卷积,获得各位点细胞丰度评分,发现 KRAS 突变组 Epi_01、Fib_CTHRC1、Mono_S100A8 丰度高于野生型,印证微环境差异。提取两类数据的差异表达基因进行多模态交集分析(p<0.01,超几何检验),以热图展示 34 种细胞在不同微环境的富集水平,为后续细胞共定位及网络互作分析奠定基础。采用 MISTy 机器学习框架分析 KRAS 突变型 CRC 的细胞空间分布与互作,发现肿瘤区域内细胞共现类型可预测近景空间尺度的肿瘤相关区室。KRAS 突变组中 Epi_01 与 Mono_S100A8 共定位显著,野生型组较弱;Fib_CTHRC1 未与二者直接共定位,但同型细胞网络与二者部分重叠,推测其形成纤维屏障。野生型肿瘤缺乏该三类细胞构成的网络。使用 ISCHIA 方法基于细胞共现特征聚类,识别出 CRC 的 6 种空间生态型。其中 KRAS 突变组特有 CC5 和 CC6:CC5 集中在肿瘤核心区,高丰度共定位 Epi_01 与 Mono_S100A8,为突变型特征生态型;CC6 分布于 CC5 外周,富含 Fib_CTHRC1 和淋巴细胞,形成排斥淋巴细胞的纤维屏障。Mono_S100A8 通过招募抑制性细胞、Fib_CTHRC1 通过形成纤维屏障,共同构建 KRAS 突变型 CRC 的免疫抑制微环境,野生型肿瘤无此结构。对各位点 34 种细胞类型归一化后,通过 Squidpy 计算邻接矩阵、弦图可视化,发现 KRAS 突变组中 Epi_01、Fib_CTHRC1、Mono_S100A8 相邻关系更频繁,还与 Fib_MMP1 形成紧密网络;野生型组无此网络,主要由其他上皮细胞组成。这进一步验证了 Fib_CTHRC1 通过环绕肿瘤细胞形成保护,支撑 KRAS 突变型 CRC 的免疫抑制微环境。Fib_CTHRC1和Mono_S100A8在KRASG12D/+;Villin-Cre小鼠中发挥关键作用
构建 KRASG12D/+; Villin-Cre 小鼠模型并建立 AOM/DSS 诱导结直肠癌模型,发现该模型小鼠肿瘤负荷更高、结肠更短、大肿瘤更多,肠上皮细胞中 KRASG12D 激活可促进癌症进展。对小鼠肿瘤组织 scRNA-seq 分析显示,其 TME 中成纤维细胞和髓系细胞比例显著升高,与人类 KRAS 突变 CRC 特征一致;成纤维细胞亚聚类后,KRAS 突变模型小鼠 Fib_CTHRC1 更丰富,髓系细胞亚聚类后 Mono_S100A8 比例和数量均增加。CellChat 分析证实,模型小鼠中 Fib_CTHRC1、Mono_S100A8 与 KRAS 突变上皮细胞间配体 - 受体信号显著增强,且存在与人类一致的 MDK-SDC4、COL1A1/COL1A2-ITGA2/ITGB1 信号轴,表明二者是促肿瘤生态位的关键功能成分,并非仅为生物标志物。对 3 例 KRAS 野生型和 3 例突变型 CRC 组织进行 mIHC 检测,以 CEACAM1(Epi_01 特异标志物)、EPCAM、CTHRC1、S100A8 为靶点,发现突变型肿瘤中三者荧光强度更高且存在空间共定位(CEACAM1 与 S100A8 共分布,CTHRC1 部分共存或分布于边缘),ST 数据与 mIHC 结果一致。研究证实,KRAS 突变上皮细胞通过 MDK_SDC4 信号招募 Mono_S100A8,Fib_CTHRC1 分泌胶原蛋白既促进肿瘤侵袭,又形成物理屏障,三者协同构建突变型 CRC 特有的免疫抑制微环境。本研究通过单细胞与空间转录组的跨技术整合,首次揭开了 KRAS 突变结直肠癌免疫抑制微环境的空间架构和分子机制,定义了全新的 “细胞三联体” 生态位模式。这一发现不仅深化了我们对 KRAS 突变驱动肿瘤进展的理解,更提供了可转化的生物标志物和治疗靶点,为突破 KRAS 突变结直肠癌的治疗瓶颈开辟了新路径。
别让繁琐的数据分析拖慢科研进度!西安科信服生物的专业团队,懂你所需、解你所难:转录组、单细胞、肠道菌群…… 无论哪个领域,机器学习、孟德尔随机化等工具信手拈来。从数据到结论,从思路到成果,一站式服务让你专注科学本身。现在就联系我们,让你的科研之路少走弯路,快速产出高质量成果,离顶刊更近一步!单细胞、孟德尔、机器学习…技术更新太快学不动?自己摸索耗时易错?🔥 我们为你铺好最后一公里路!从方案设计、数据清洗到结果解析,核心技能一站配齐。不止教技术,更教你如何用在课题上。👉 专属福利:现在报名,享一对一导师全程答疑,真正“学会为止”!⏰ 限时叠加:三人拼团立减288元,转发海报再领神秘科研好礼!扫码咨询,让你的科研效率翻倍!