IF10.1!南京医科大学团队GEO+机器学习轻松拿下一区!
- 2026-05-09 07:47:06

📍为什么同样的化疗方案,有的胰腺癌患者有效,有的却迅速耐药?答案可能藏在一群名为‘应激颗粒’的细胞器中。
💡南京医科大学这项发表于《International Journal of Surgery》上的首次系统性地揭示了应激颗粒相关基因在胰腺导管腺癌中的多维度预后价值及其在肿瘤微环境中的动态调控网络。
💥这篇研究首次构建了基于应激颗粒基因(LAMA3、ITGA6、COL17A1、TOP2A)的胰腺癌预后模型。突破在于:通过机器学习与单细胞测序,揭示上述基因主导导管细胞分化、重塑免疫微环境(如巨噬细胞/CD8⁺ T细胞失衡),并关联特定靶向药物敏感性,为“癌王”的精准诊疗提供新框架。
如果你也想使用机器学习和GEO数据库的方法进行生信分析,快关注科研圈与GBD吧!
°首次构建基于 SG 相关基因的 PDAC 预后模型
°首次揭示 SG 相关基因与 PDAC 免疫微环境的关联规律
°首次通过单细胞测序解析 SG 相关基因的细胞特异性机制
°首次明确不同风险组的药物敏感性差异与分子特征

胰腺导管腺癌(PDAC)恶性程度高、预后差,5 年生存率不足 10%,现有治疗受诊断延迟、耐药等因素限制。其纤维化微环境和代谢失调为应激颗粒(SGs)研究提供理想模型,但 SGs 在 PDAC 中的预后价值与相关机制尚未明确。本研究结合机器学习与单细胞测序,探究 SG 相关基因的作用,旨在挖掘预后标志物与治疗靶点。
①数据获取
从 TCGA、GEO 数据库获取 PDAC 转录组及单细胞测序数据,作为训练集和验证集。从 GeneCards 数据库提取 844 个应激颗粒相关基因(SGRGs)。
②核心基因筛选与模型构建
筛选 PDAC 与正常组织的差异表达基因,与 SGRGs 取交集得到差异表达 SGRGs。经单变量 Cox 回归分析筛选候选预后基因,结合 10 种机器学习算法的 101 种组合,最终确定 4 个核心预后 SGRGs(LAMA3、ITGA6、COL17A1、TOP2A),构建风险评分模型。
③模型验证与临床关联
用 Kaplan-Meier 曲线、ROC 曲线验证模型预后预测能力,结合年龄、N 分期构建诺模图。分析高低风险组的免疫细胞浸润、药物敏感性及基因突变差异。
④单细胞与机制分析
对单细胞数据进行质控、聚类和细胞注释,确定导管细胞为关键细胞类型。
通过伪时间分析探究导管细胞分化与核心基因的关联,用 CellChat 分析细胞间通信。
差异表达 SGRGs 筛选与功能特征
从 TCGA 训练集中鉴定出 3456 个差异表达基因(DEGs),与 844 个 SGRGs 取交集,得到 90 个差异表达 SGRGs(DE-SGRGs)。
功能富集分析显示,DE-SGRGs 富集于 “活性氧代谢过程”“白细胞迁移” 等生物学过程,以及 “AGER-AGE 信号通路”“ECM - 受体相互作用” 等关键通路,提示其参与 PDAC 的病理进程调控。
蛋白质 - 蛋白质相互作用(PPI)网络分析发现,APOE、ITGB2、REN 等基因在网络中存在广泛相互作用,可能是 DE-SGRGs 发挥功能的核心节点。
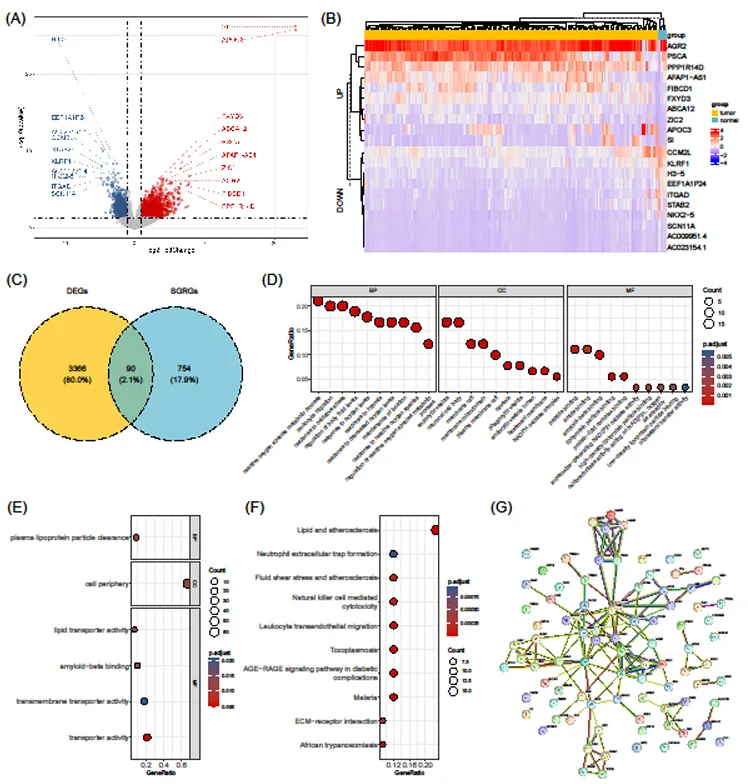
图1:差异表达 SGRGs 筛选与功能特征
预后风险模型构建与验证
通过单变量 Cox 回归分析和比例风险假设检验,筛选出 12 个候选预后 SGRGs,再结合 10 种机器学习算法的 101 种组合,最终确定 4 个核心预后 SGRGs(LAMA3、ITGA6、COL17A1、TOP2A)
模型预测性能优异:训练集 1、2、3 年生存率 AUC 值分别为 0.70、0.73、0.75;验证集 GSE28735 对应 AUC 值达 0.64、0.78、0.83,高低风险组患者生存率差异显著(p<0.0001)。
整合风险评分、年龄、N 分期构建诺模图,校准曲线显示预测生存率与实际观察结果高度一致,且风险评分为独立预后因素。
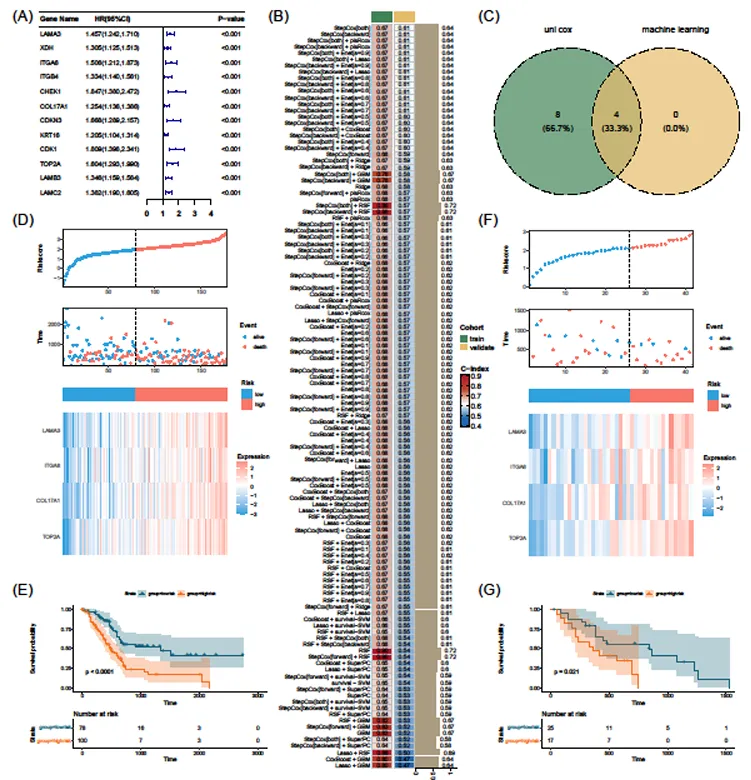
图2:预后风险模型构建
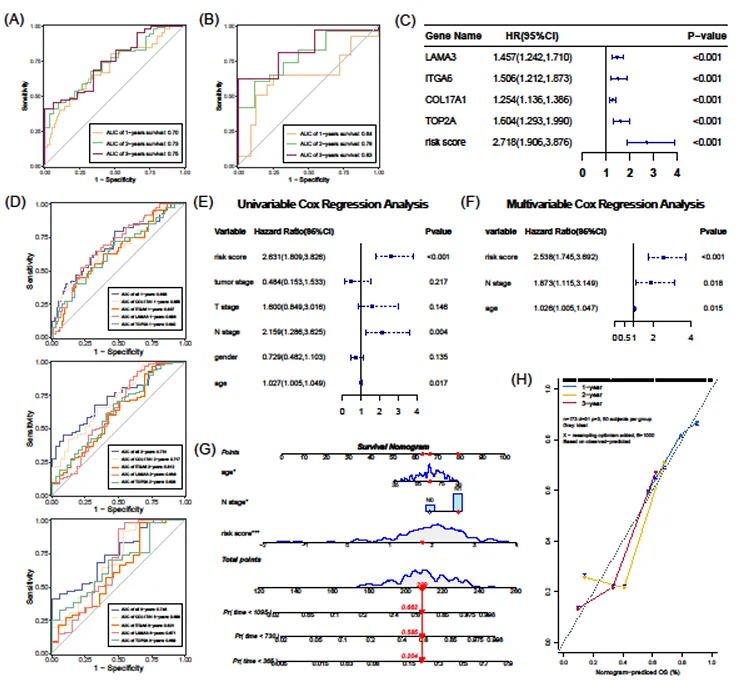
图3:模型验证与临床关联
免疫微环境与免疫 checkpoint 差异
高低风险组免疫细胞浸润存在显著差异:高风险组 M0 巨噬细胞、嗜酸性粒细胞浸润增加,CD8 T 细胞、单核细胞浸润减少;M0 巨噬细胞与 COL17A1 呈强正相关(cor=0.33,p<0.001),CD8 T 细胞与 ITGA6 呈强负相关(cor=-0.30,p<0.001)。
高风险组 ESTIMATE 评分、免疫评分及基质评分均显著更低,且 13 个免疫检查点基因表达异常,其中 LGALS9、TNFSF9 等 9 个基因上调,CD200、BTLA 等 4 个基因下调,提示高风险患者存在更明显的免疫逃逸。
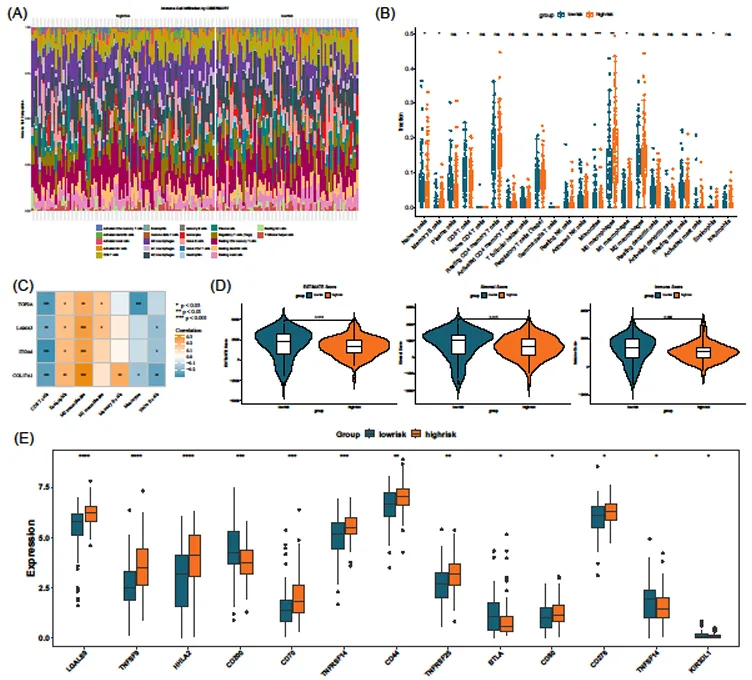
图4:高/低风险组胰腺癌患者中22种免疫细胞的浸润丰度比例图和(B)免疫浸润景观图
药物敏感性与基因突变特征
药物敏感性分析显示,低风险组对 JAK1_8709、sabutoclax 等药物敏感性更高(p<0.0001);高风险组对 ERK 抑制剂、trametinib 等药物敏感性更强,为精准治疗提供方向。
基因突变分析表明,高风险组 KRAS(77%)、TP53(71%)、SMAD4 突变率显著高于低风险组(KRAS 33%、TP53 37%);低风险组基因突变总数更少,单核苷酸多态性(SNP)比例更低,C-T 突变比例更高,提示不同风险组的分子变异模式存在差异。
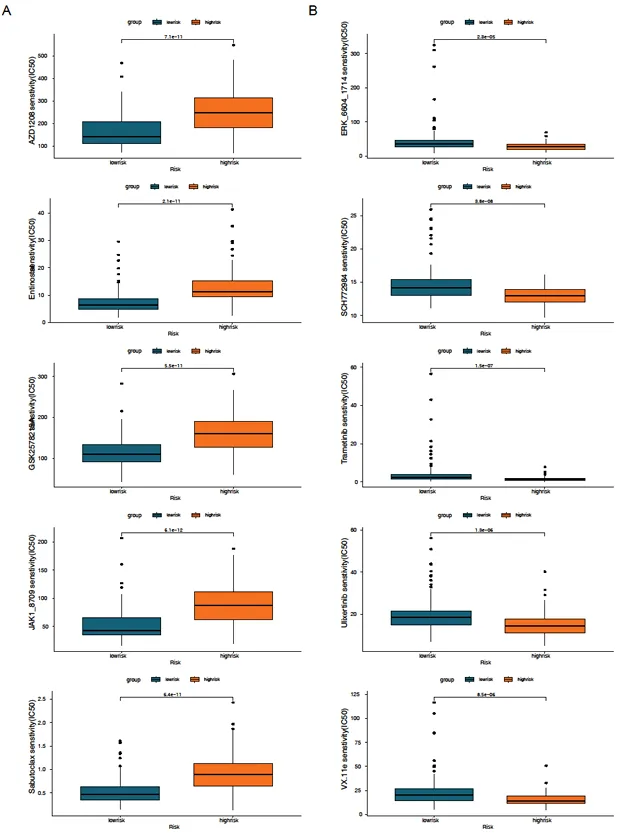
图5:胰腺癌患者低风险组或高风险组对常见抗肿瘤药物的敏感性评分图
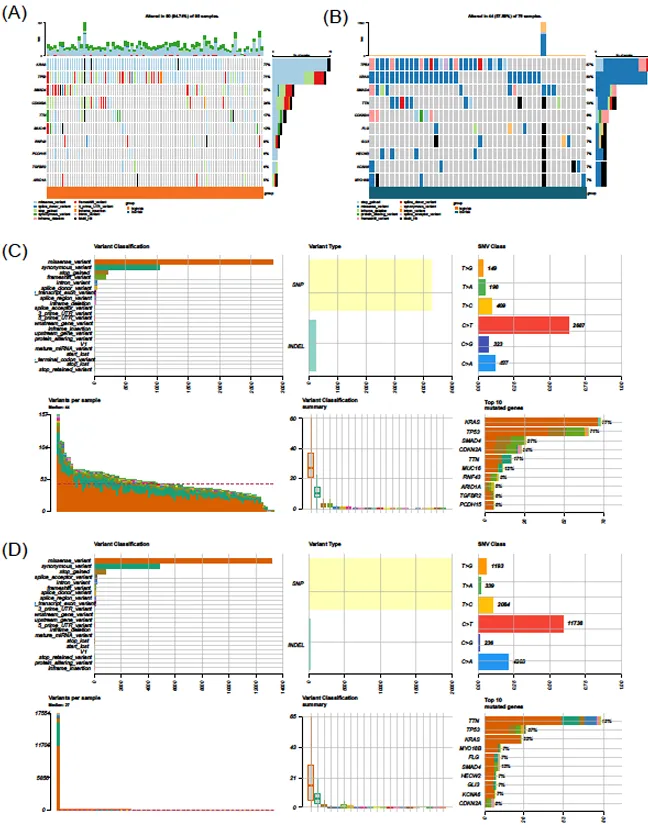
图6:高风险组(A)和低风险组(B)的肿瘤突变负荷分析瀑布图
核心 SGRGs 生物学机制
基因集富集分析(GSEA)显示,核心 SGRGs 参与多个关键通路:LAMA3 富集于 “硫酸化” 通路,ITGA6 关联 “糖酵解过程调控”“葡萄糖摄取”,COL17A1 涉及 “白细胞介素 27 介导的信号通路”,TOP2A 参与 “肝素生物合成”“脱氧核苷三磷酸生物合成”,这些通路均与 PDAC 发生发展密切相关。
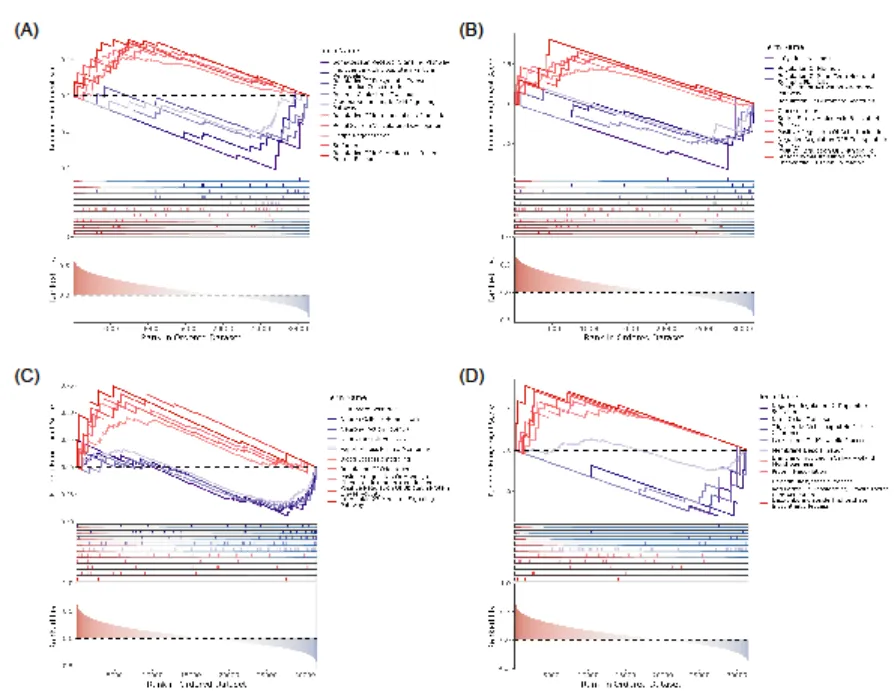
图7:核心 SGRGs 生物学机制
单细胞测序解析肿瘤微环境
对 GSE197177 和 GSE212966 单细胞数据集分析,鉴定出 11 种细胞类型(导管细胞、成纤维细胞、巨噬细胞等),其中导管细胞为关键细胞类型,且核心 SGRGs 在导管细胞中表达差异显著(p<0.01)。
伪时间分析显示,导管细胞分为 6 种亚型,分化过程经历 3 个状态,COL17A1、ITGA6 表达随分化进展升高,LAMA3 先升后降,TOP2A 呈 “降 - 停 - 升” 趋势,提示核心 SGRGs 与导管细胞分化状态密切相关。细胞通信分析发现,PDAC 组细胞间相互作用数量和强度显著高于正常组,导管细胞与成纤维细胞间存在强相互作用,可能共同促进肿瘤进展。
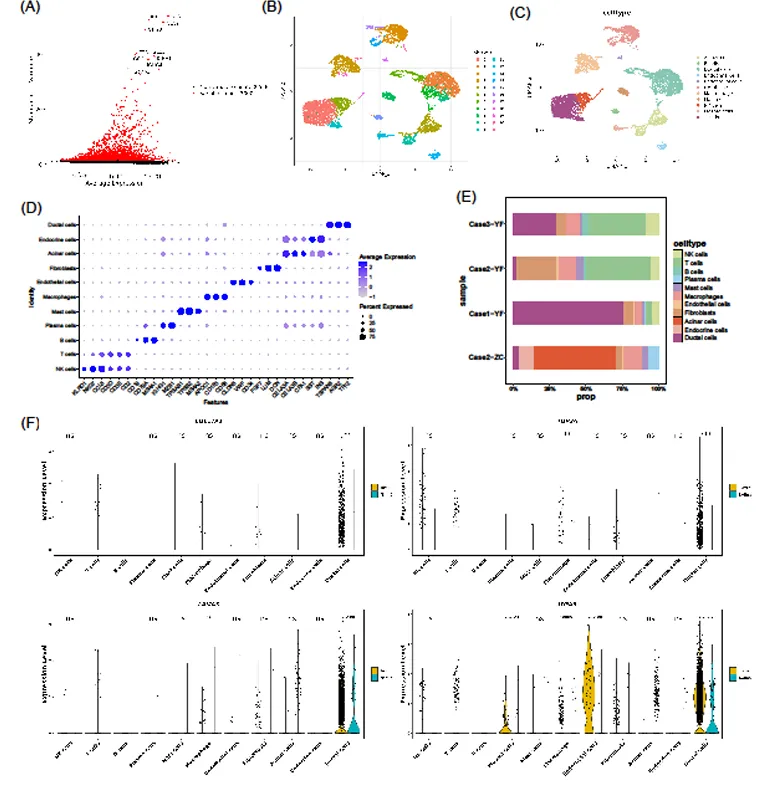
图8:单细胞景观分析
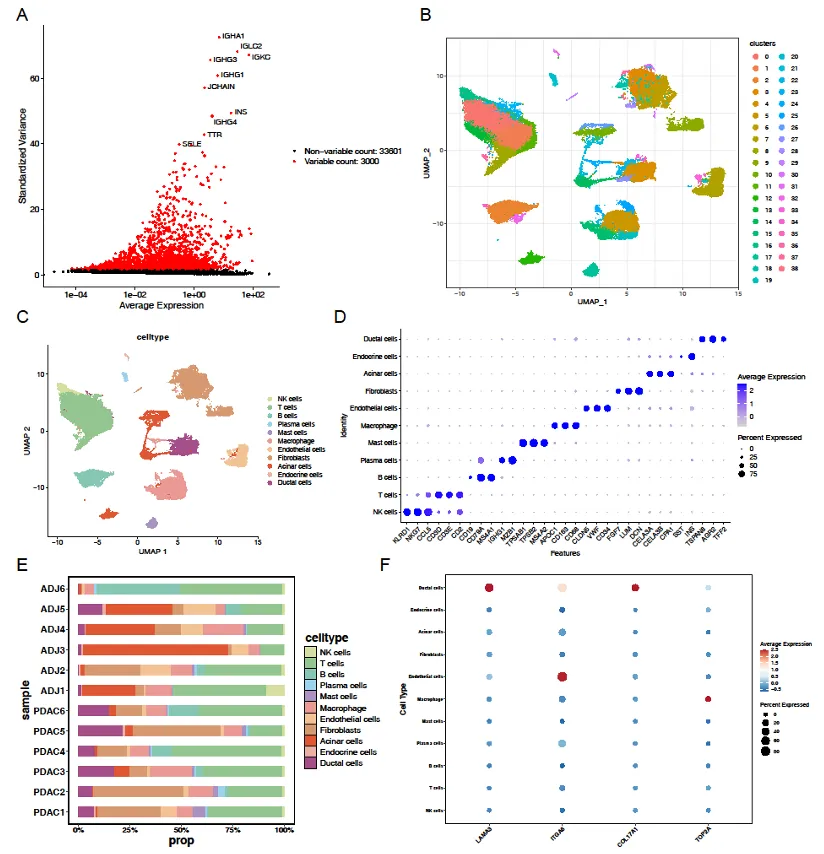
图9:导管细胞动态与细胞通信
核心 SGRGs 表达验证
在 TCGA 训练集和 GSE28735 验证集中,LAMA3、ITGA6、COL17A1、TOP2A 在 PDAC 肿瘤组织中的表达均显著高于癌旁正常组织(p<0.05),进一步证实其与 PDAC 的关联性。
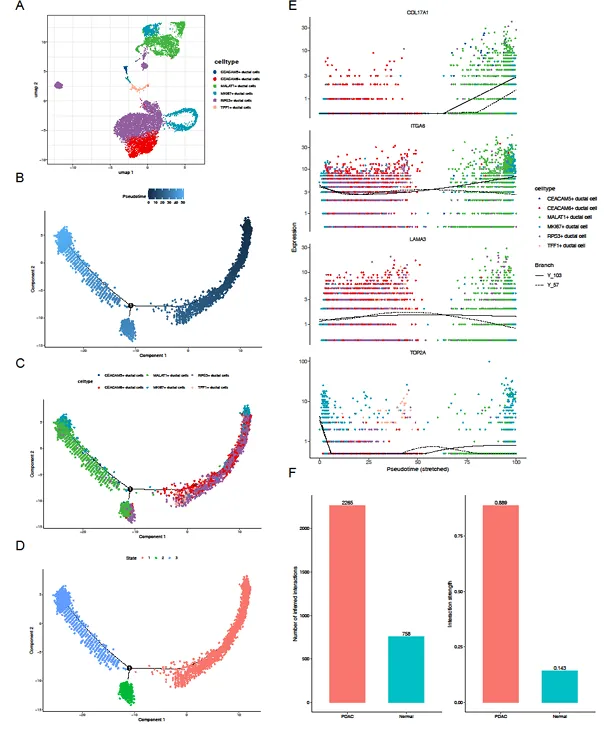
图10:核心 SGRGs 表达验证
该研究整合 TCGA、GEO 等数据库数据,通过差异表达分析、10 种机器学习的 101 种算法组合及单细胞测序技术开展研究。应激颗粒相关基因(SGRGs)在胰腺导管腺癌(PDAC)中的作用机制、免疫微环境特征、药物敏感性及细胞间通信。旨在筛选核心预后 SGRGs,构建并验证 PDAC 风险模型,明确不同风险组分子特征,为 PDAC 预后预测与个性化治疗提供依据。
如果你也想使用机器学习和GEO数据库的方法高分发文,欢迎私信咨询!

就找科研圈与GBD
