南京大学医学院附属鼓楼医院丨Syndecan-4 缺失加重巨噬细胞促炎能力,加速动脉粥样硬化发生发展
- 2026-05-02 23:20:58

前言
本研究以动脉粥样硬化分子机制不明为切入点,先检测小鼠重度动脉粥样硬化模型中 SDC4 的表达,发现其表达降低;随后构建 SDC4 与 ApoE 双敲除小鼠,给予高胆固醇饮食诱导动脉粥样硬化,结合组织染色、ELISA 检测明确 SDC4 缺失对斑块、脂质及炎症因子的影响;再分离原代巨噬细胞进行体外培养,经 oxLDL 刺激后检测细胞脂质沉积和炎症因子分泌,并通过蛋白印迹探究相关信号通路;最后利用慢病毒回补 SDC4、PKCα 激动剂干预验证通路作用,证实 SDC4 缺失通过抑制 PKCα-ABCA1/ABCG1 通路,增强巨噬细胞促炎能力、降低脂质转运能力,进而促进动脉粥样硬化,而补充 SDC4 或激活 PKCα 可逆转该效应,最终明确巨噬细胞中 SDC4 是防治动脉粥样硬化的潜在治疗靶点。
研究要点解析
研究方法
首先检测动脉粥样硬化小鼠血管组织中 SDC4 的表达水平,明确其与疾病的关联;再构建 SDC4⁻/⁻ApoE⁻/⁻双敲除小鼠,通过高胆固醇饮食诱导动脉粥样硬化,结合组织学染色、ELISA 等技术,从体内层面探究 SDC4 缺失对斑块形成、脂质代谢及炎症反应的影响;随后分离小鼠原代巨噬细胞进行体外培养,经 oxLDL 刺激后,检测细胞脂质沉积和炎症因子分泌情况,明确 SDC4 对巨噬细胞功能的调控;最后通过蛋白印迹、慢病毒回补 SDC4、PKCα 激动剂干预等手段,探究 SDC4 调控巨噬细胞功能及动脉粥样硬化的分子通路,并验证通路的特异性。
研究结果
动脉粥样硬化小鼠血管组织中巨噬细胞的 SDC4 表达显著降低;SDC4⁻/⁻ApoE⁻/⁻双敲除小鼠经高胆固醇饮食诱导后,主动脉弓脂质沉积更多、主动脉根部斑块负荷更重,血液中总胆固醇等脂质指标及血管组织促炎因子水平显著升高,且斑块胶原含量无明显变化;体外实验中,SDC4 缺失的巨噬细胞经 oxLDL 刺激后,脂质沉积增加、促炎因子分泌增多,PKCα 活性及 ABCA1、ABCG1 表达显著降低;慢病毒回补 SDC4 可恢复 PKCα-ABCA1/ABCG1 通路活性,PKCα 激动剂 PDBu 可逆转 SDC4 缺失导致的巨噬细胞脂质沉积增加和促炎能力增强的表型。
研究结论
本研究首次发现动脉粥样硬化小鼠中 SDC4 表达显著下调,且 SDC4 缺失不仅是动脉粥样硬化的病理结果,更是疾病发展的促进因素,其通过 PKCα-ABCA1/ABCG1 通路增强巨噬细胞促炎能力、降低脂质外流,进而加剧慢性炎症和脂质沉积,推动动脉粥样硬化进展,同时 SDC4 作为跨膜受体,其对炎症的调控存在细胞和场景特异性,在慢性血管炎症中主要发挥抗炎、保护血管的作用。但本研究存在局限性:采用全身 SDC4 敲除小鼠而非巨噬细胞特异性敲除模型,无法更精准地验证巨噬细胞中 SDC4 的作用;未探究 SDC4 对动脉粥样硬化中淋巴细胞、树突状细胞等其他免疫细胞的调控作用;仅使用雄性小鼠构建模型,未考虑性别差异对研究结果的影响,结论的适用性有待进一步验证。
图文结果解读
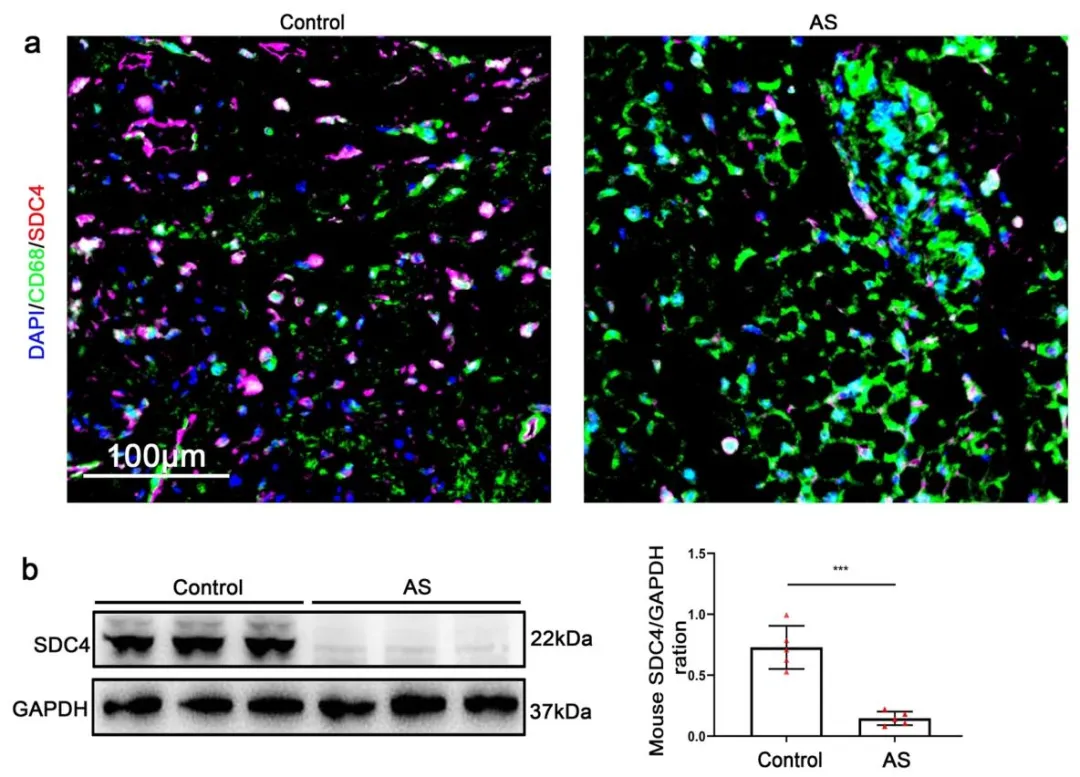
Fig1:通过免疫荧光和蛋白印迹实验,证实动脉粥样硬化(AS)小鼠血管组织中 SDC4 的表达水平相较于正常对照小鼠显著降低,明确 SDC4 下调与动脉粥样硬化发展相关。
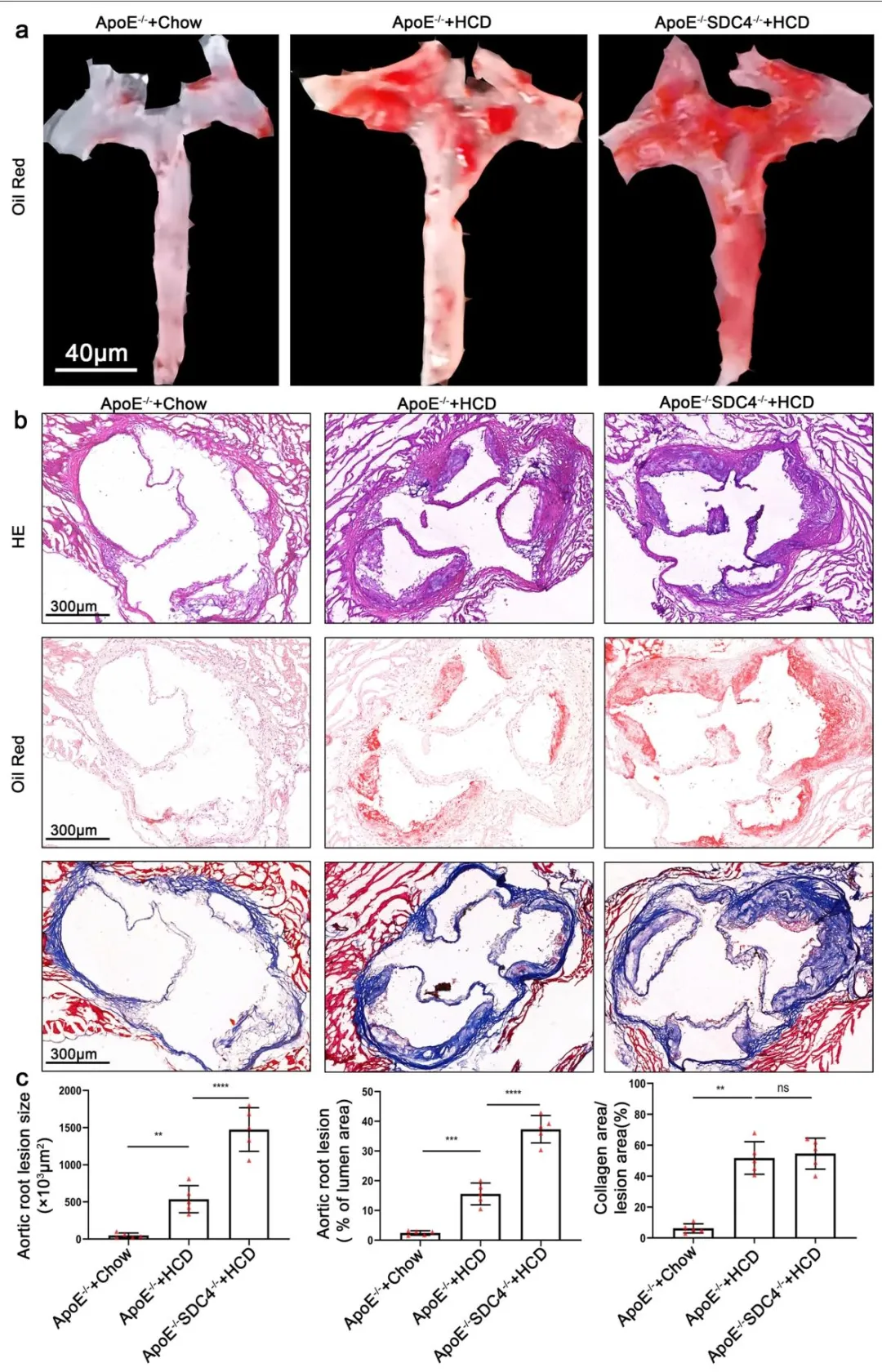
Fig2:利用油红 O、HE、Masson 染色及统计学分析,显示 SDC4⁻/⁻ApoE⁻/⁻双敲除小鼠经高胆固醇饮食诱导后,主动脉弓脂质沉积、主动脉根部斑块面积和脂质含量均显著高于 ApoE⁻/⁻小鼠,而胶原含量无显著差异,证明 SDC4 缺失会加速动脉粥样硬化斑块形成,且对斑块稳定性无明显影响。
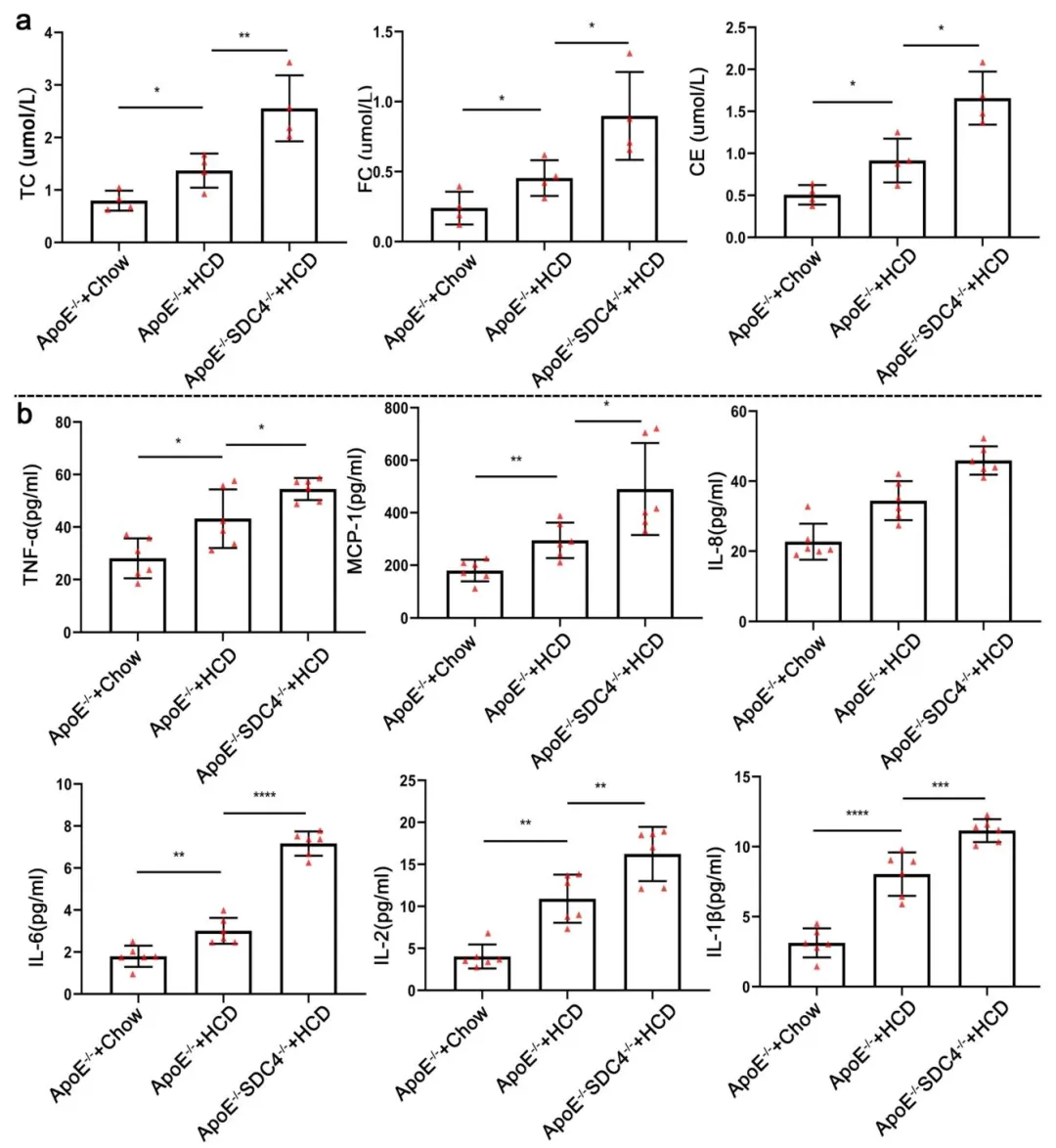
Fig3:通过 ELISA 检测,发现 SDC4⁻/⁻ApoE⁻/⁻小鼠血液中胆固醇酯、游离胆固醇、总胆固醇等脂质指标,以及血管组织中 TNF-α、MCP-1 等促炎因子水平,均显著高于 ApoE⁻/⁻小鼠,证实 SDC4 缺失与动脉粥样硬化中脂质代谢紊乱和炎症反应增强相关。
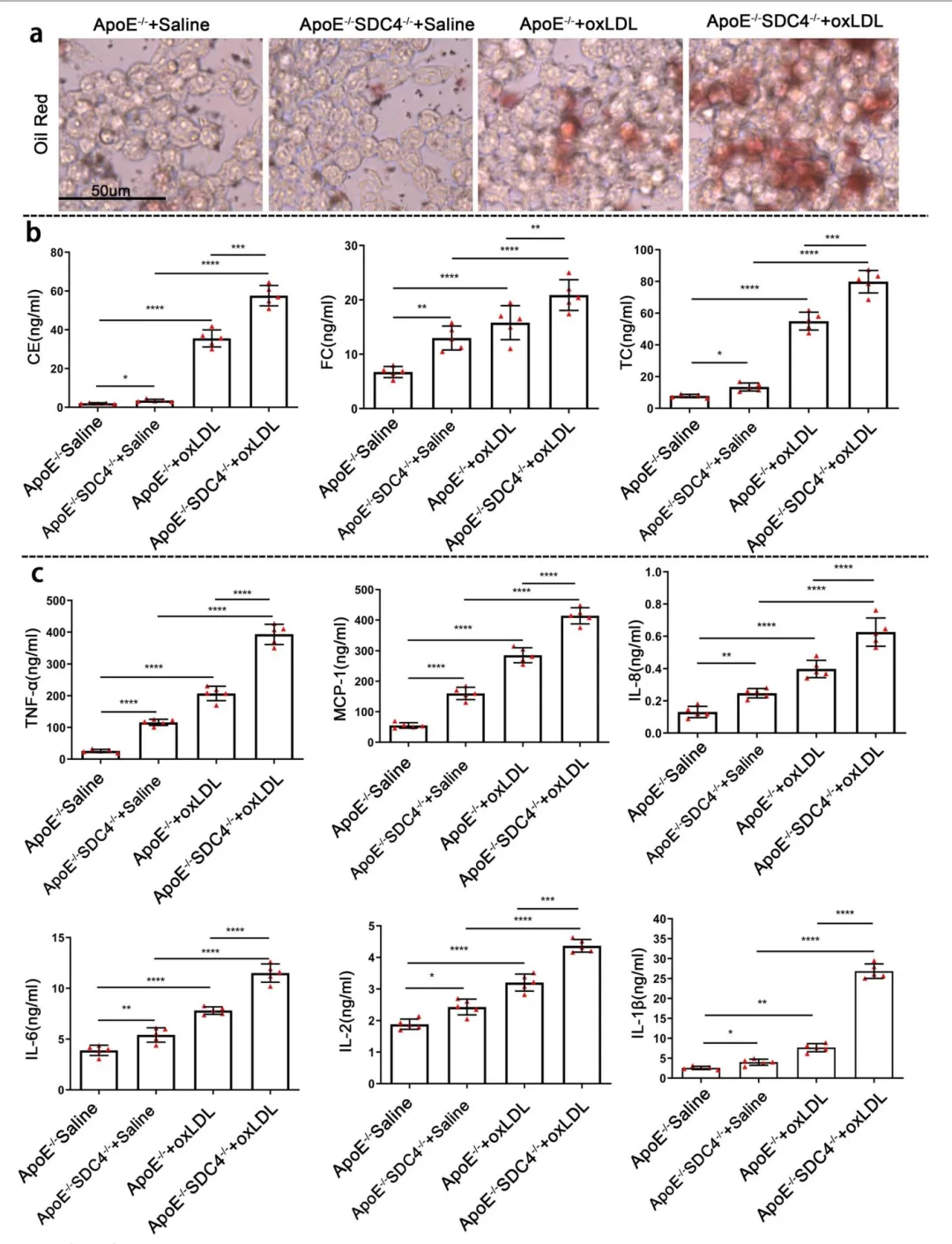
Fig4:体外巨噬细胞经 oxLDL 刺激后,油红 O 染色显示 SDC4 缺失的巨噬细胞脂质沉积更多,ELISA 检测发现其培养液中脂质指标和促炎因子水平均显著升高,证明 SDC4 缺失会增强巨噬细胞的促炎能力、降低其脂质转运能力。
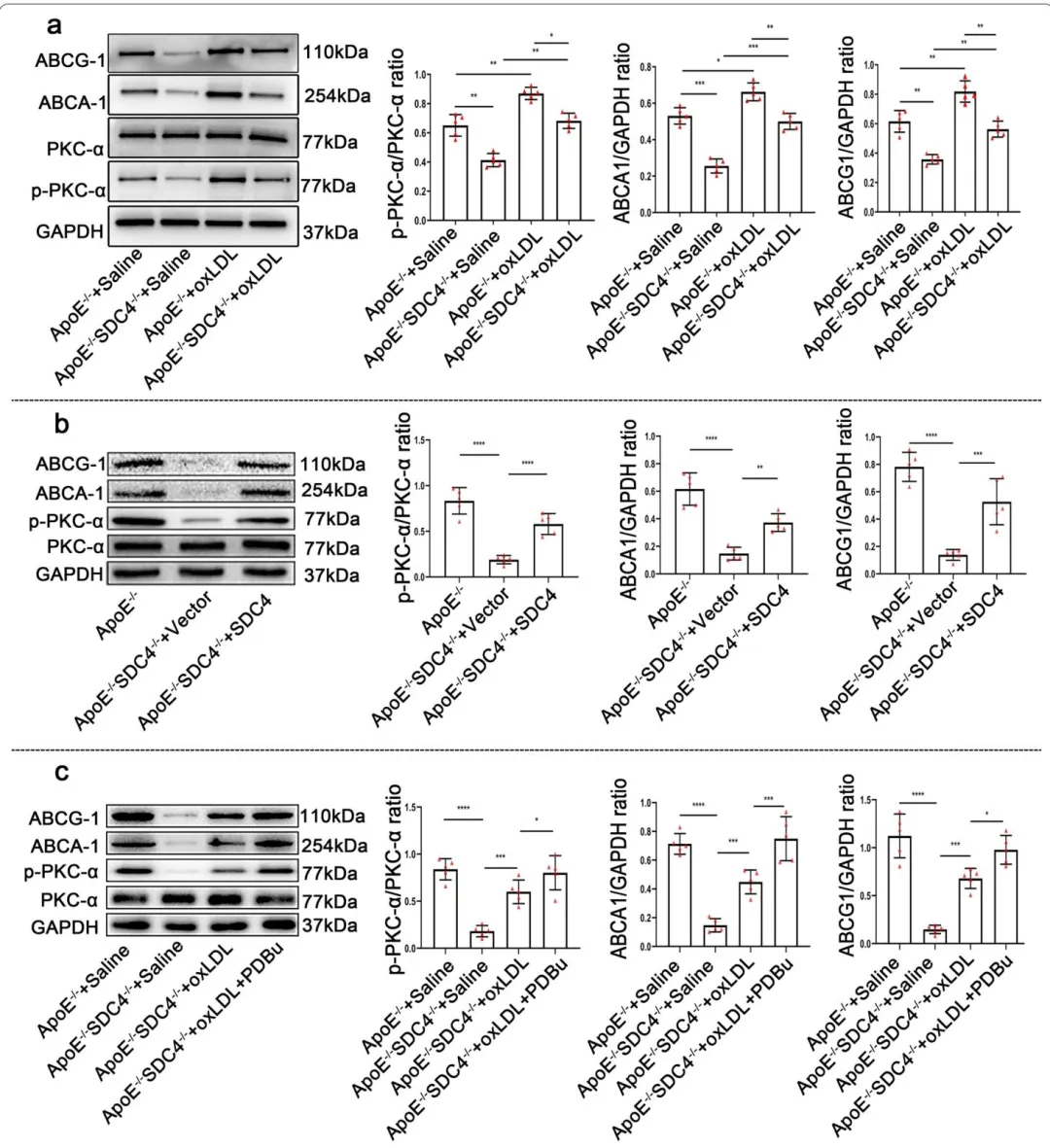
Fig5:蛋白印迹实验结果显示,SDC4 缺失的巨噬细胞中 PKCα 活性及 ABCA1、ABCG1 表达显著降低;慢病毒回补 SDC4 可恢复该通路相关蛋白的表达和活性;PKCα 激动剂 PDBu 可逆转 SDC4 缺失导致的通路抑制,证实 SDC4 调控巨噬细胞的作用依赖于 PKCα-ABCA1/ABCG1 通路。
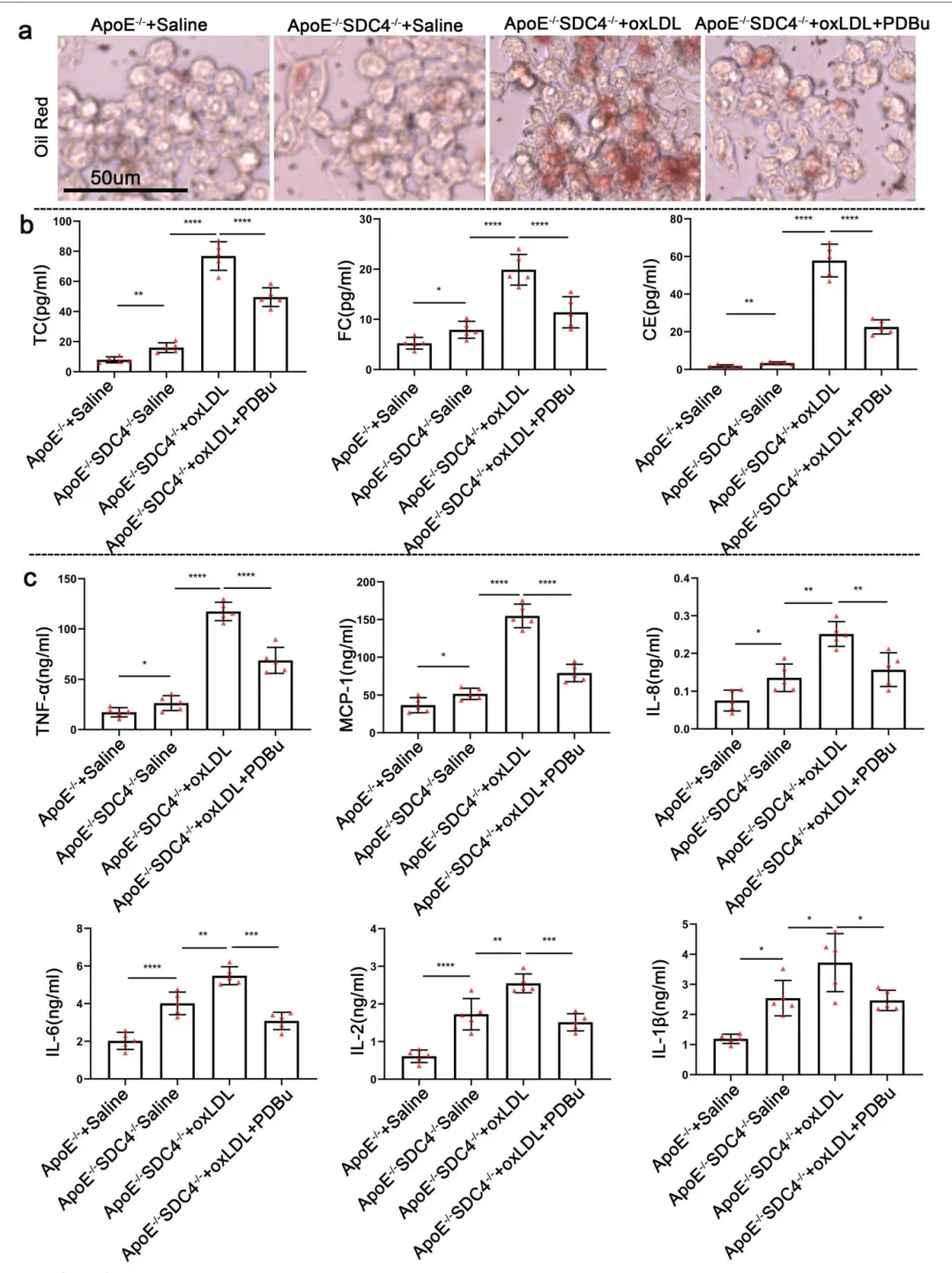
Fig6:油红 O 染色显示 PKCα 激动剂 PDBu 可减少 SDC4 缺失巨噬细胞的脂质沉积,ELISA 检测发现 PDBu 可降低其培养液中脂质指标和促炎因子水平,进一步验证 PKCα-ABCA1/ABCG1 通路是 SDC4 调控巨噬细胞脂质代谢和炎症反应的关键通路。
参考文献:Hu J, Zhang Y, Hu L, Chen H, Wu H, Chen J, Xie J, Xu B, Wei Z. A reduction of Syndecan-4 in macrophages promotes atherosclerosis by aggravating the proinflammatory capacity of macrophages. J Transl Med. 2022 Jul 16;20(1):319. doi: 10.1186/s12967-022-03505-5. PMID: 35842658; PMCID: PMC9287986.
本文中使用的图片来Pubmed,因客观原因未能与权利人取得联系。本平台出于学术交流目的引用,无意侵犯原作者权益。如权利人认为不妥,请及时联系公众号后台,我们将立即删除或协商解决。
医学国自然,省自然,博士课题设计,医学实验外包,医学SCI,实验方案设计,免费的线上博导一对一沟通,确认实力后再谈合作,科研合作可以加微信:SCI971SCI

生物信息学课题设计及指导实录,目前生信是否还适用于课题及文章?看专家给你解答
临床型博士如何准备国青标书?没有预实验怎么办?专家一对一解答规划
科研信息合集
整形外科方向最新研究分享
国自然课题设计思路
各大学校及医院国自然立项信息
骨科科研最新分享
泌尿外科科研最新分享
消化领域科研最新分享