南京大学鼓楼医院郭保生/蒋青团队最新《Nature Aging》揭示运动改善阿尔茨海默病认知障碍的新机制:骨骼肌分泌的 “小泡” 是关键
题目:Exercise alleviates cognitive dysfunction in Alzheimer's disease mice via skeletal muscle-derived extracellular vesicles that enhance plaque clearance by microglia通讯作者:郭保生 南京大学医学院附属鼓楼医院运动医学与成人重建外科行政主任,南京大学医学院副院长,国家重点研发计划首席科学家,入选江苏省“333高层次人才培养工程”第一层次;国内培养的第一个运动医学临床博士,“国之名医“获得者。担任国际关节炎协会(OARSI)任职理事,国际软骨损伤修复学会(ICRS)中国分会副主委、中华医学会运动医疗分会副主委、中国医师协会运动医学分会副会长、江苏省运动医疗分会创始主任委员。在Cell Metabolism,Nature Metabolism,Science Translational Medicine有影响力学术期刊上发表论文260余篇,他引9000余次,Annals of Joint创刊主编,《骨科专家评论》等两部专著的主编,以第一完成人获省部级一等奖1项、二等奖3项,多次获政府和行业表彰及荣誉称号。蒋青,主任医师、教授,博士生导师,南京大学医学院附属鼓楼医院运动医学与成人重建外科主任,从事运动医学疾病临床诊疗及科室管理与建设和运动系统疾病基础与临床研究工作;是国内培养的第一个运动医学临床博士、运动医学领域的首位国家杰青、科技部重点研发项目首席科学家。担任中华医学会运动医疗分会副主任委员、中国医师协会运动医学分会副会长、国际软骨损伤修复学会中国分会副主任委员、中国生物材料学会理事、江苏省医学会骨科学分会主任委员、江苏省医师协会运动医学医师分会会长。导语
阿尔茨海默病(AD)作为最常见的痴呆类型,其引发的认知衰退和功能障碍已成为全球重大医疗与社会问题,目前仍缺乏高效的治疗手段。而适度运动对 AD 认知功能的改善作用早已被证实,但背后的深层机制一直是科研界的未解之谜。近期,南京大学鼓楼医院郭保生/蒋青团队发表于《Nature Aging》的一项重磅研究,首次揭示了骨骼肌与大脑之间的 “跨界通讯” 机制-运动诱导骨骼肌分泌的细胞外囊泡,可通过调控小胶质细胞功能清除脑内淀粉样斑块,为AD的治疗提供了全新的运动模拟疗法思路,也为骨科与神经科学的交叉研究打开了新视野。
研究亮点
- 一、首次揭示骨骼肌 - 大脑的跨器官通讯新通路,填补运动改善 AD 机制的关键空白 既往研究仅证实运动对 AD 认知有改善作用,且知晓骨骼肌具备内分泌功能,但未明确骨骼肌向大脑传递调控信号的具体载体和途径。本研究首次证实,游泳运动可诱导骨骼肌分泌骨骼肌来源细胞外囊泡(SKM-EVs),该囊泡能突破血脑屏障的生理屏障,且被脑内小胶质细胞特异性摄取,明确了 SKM-EVs 是介导骨骼肌向大脑传递运动有益信号的核心介质,构建了 “骨骼肌 - SKM-EVs - 大脑小胶质细胞” 的跨器官通讯轴,填补了运动改善 AD 分子机制中 “外周 - 中枢” 信号传递的关键空白。
- 二、精准锁定 SKM-EVs 中调控 AD 的核心功能分子,明确 miR-378a-3p 的关键作用 细胞外囊泡包含多种 RNA、蛋白质、脂质等生物活性物质,本研究通过骨骼肌特异性 Dicer1 敲除小鼠模型,先证实 SKM-EVs 中的 miRNA 是发挥认知保护作用的核心组分;再通过 miRNA 深度测序、组织表达谱分析,从 20 个运动后上调的 miRNA 中,筛选出miR-378a-3p为关键功能分子 —— 该分子是唯一在骨骼肌和 SKM-EVs 中均被运动显著激活、且高度富集于骨骼肌的 miRNA,同时证实其在脑内的成熟体并非大脑自身合成,而是由 SKM-EVs 外周递送,精准锁定了运动改善 AD 的核心分子靶点。
- 三、阐明 miR-378a-3p 调控小胶质细胞功能的全新分子机制,关联脂质代谢与 Aβ 斑块清除 本研究首次揭示 miR-378a-3p 通过靶向抑制 p110α发挥作用,进而调控下游 AKT-GSK3β-FoxO1-LPL 信号轴,实现对疾病相关小胶质细胞(DAM)脂质代谢的精准调控。机制上,miR-378a-3p 抑制 p110α 后,可下调 AKT/GSK3β 磷酸化、上调 FoxO1 表达,进而促进脂蛋白脂酶(LPL)合成,增强小胶质细胞的脂质代谢水平和 ATP 生成,最终推动 DAM 的极化活化,提升其对 Aβ 斑块的吞噬和清除能力。该发现首次将骨骼肌来源 miRNA、脂质代谢与小胶质细胞的 Aβ 清除功能关联,揭示了 AD 中 microglia 功能调控的新机制。
- 四、通过功能获得 / 缺失实验层层验证,证实 SKM-EVs 及 miR-378a-3p 的核心效应 研究采用多维度的功能验证策略,层层递进证实核心靶点的作用:功能获得实验中,尾静脉注射运动诱导的 SKM-EVs、海马注射 miR-378a-3p 激动剂、骨骼肌特异性过表达 miR-378a-3p,均能显著改善 AD 小鼠认知、促进 DAM 活化和 Aβ 清除;功能缺失实验中,特异性阻断骨骼肌 EVs 分泌、敲除骨骼肌 Dicer1、骨骼肌特异性沉默 miR-378a-3p,均会完全消除运动对 AD 小鼠的认知保护作用。同时,体外细胞模型与体内动物模型相互印证,确保了研究结果的可靠性和严谨性。
- 五、开发出基于 SKM-EVs 的 AD 新型 “运动模拟” 治疗策略,具备潜在临床转化价值 考虑到 AD 患者常伴随肌萎缩、运动能力下降,难以通过自主运动获得获益,本研究构建了miR-378a-3p 过表达的 C2C12 肌管来源 EVs,证实尾静脉注射该工程化 EVs,可完美复刻运动的治疗效果 —— 显著减少 AD 小鼠脑内 Aβ 斑块、激活 DAM、改善突触可塑性和认知功能,且该效应依赖于小胶质细胞的存在。该策略将骨骼肌来源 EVs 作为天然的药物递送载体,兼具生物安全性、低免疫原性和血脑屏障穿透性,为 AD 的临床治疗提供了全新的、可替代运动的靶向生物治疗方案,具有重要的临床转化潜力。
- 六、实现骨科与神经科学的深度交叉,建立骨骼肌生理与神经退行性疾病的直接关联 本研究突破了骨科研究聚焦骨骼肌 “运动、支撑、损伤修复” 的经典范畴,将骨骼肌的内分泌功能与神经退行性疾病的发病机制紧密结合,首次证实骨骼肌可通过分泌 EVs 远程调控中枢神经系统的免疫功能(小胶质细胞活化),建立了骨骼肌生理状态与 AD 发生发展的直接联系。该研究为骨科领域开辟了 “骨骼肌 - 大脑轴” 的全新研究方向,推动了骨科与神经科学、老年病学、代谢病学的跨学科融合。
主要研究结果
本研究以 6 月龄 APP/PS1 AD 模型小鼠为研究对象,通过 4 周游泳运动干预、体内外功能实验、分子机制验证等一系列研究,取得了以下核心结果:
- 一、运动通过激活小胶质细胞改善 AD 小鼠认知 游泳运动显著减少 AD 小鼠大脑皮层和海马区的 Aβ 斑块沉积,提升其空间记忆和物体识别能力;而特异性清除小胶质细胞后,运动的认知改善作用完全消失,证实 DAM 的激活是运动改善 AD 的必要条件。
- 图1:运动锻炼通过激活小胶质细胞改善APP/PS1小鼠认知功能。a,APP/PS1小鼠有氧游泳训练示意图。b,每只小鼠选取20-25个淀粉样斑块进行三维结构重建分析。比例尺,5微米(每组分析6只小鼠)。c,对邻近淀粉样斑块但未直接接触斑块的小胶质细胞进行三维结构重建与Sholl分析;每只小鼠选取5-10个小胶质细胞生成一个生物学重复值用于Sholl分析。比例尺,10微米(每组分析6只小鼠)。d,流式细胞术分析小胶质细胞及CD11c阳性、甲氧基-X04阳性疾病相关小胶质细胞(每组分析6只小鼠)。e,Trem2、DAP12和p-SYK蛋白免疫印迹分析。样品源自同一实验,p-SYK凝胶平行处理(每组分析6只小鼠)。f,两阶段疾病相关小胶质细胞激活的PCR分析(每组分析6只小鼠)。g,APP/PS1小鼠小胶质细胞清除策略示意图。使用BioRender创建。Lin, J. (2026) https://biorender.com/7f9auln。h–k,水迷宫和新物体识别行为学分析(每组分析12只小鼠)。l,6×10^10阳性淀粉样斑块免疫荧光分析。比例尺,100微米(每组分析6只小鼠)。a–f采用两批独立APP/PS1小鼠:第一批(每组12只)用于行为学测试后的免疫荧光/免疫组化染色;第二批(每组18只)用于蛋白质印迹、PCR和流式细胞术分析。g–j采用单批独立APP/PS1小鼠(每组12只)。组间统计学显著性通过双尾非配对t检验(b、d、e、f)、单因素方差分析结合Tukey多重比较检验(i、k、l)、重复测量双因素方差分析结合Tukey多重比较检验(j)及双因素方差分析结合Bonferroni事后检验(c)进行计算。a.u.,任意单位;NS,无显著性差异。
- 二、运动促进 SKM-EVs 分泌并靶向脑内小胶质细胞
运动可显著上调骨骼肌中细胞外囊泡合成与分泌相关基因表达,体外肌组织运动模型也证实骨骼肌分泌 EVs 增多;通过骨骼肌特异性 CD63-GFP 报告小鼠,首次直观证实 SKM-EVs 可跨越血脑屏障,且优先被脑内小胶质细胞摄取。图2:运动促进骨骼肌来源细胞外囊泡分泌及其进入小胶质细胞。a,有氧游泳运动APP/PS1小鼠比目鱼肌中Rab27a表达的免疫荧光分析(每组分析6只小鼠)。b,离体肌肉训练模型及细胞外囊泡纯化分离示意图。c,离体训练肌肉中Rab27a、CD9和CD63的蛋白质印迹分析(每组分析6只小鼠)。d,离体训练组与对照组细胞外囊泡透射电镜分析。比例尺,100微米(每组分析6个实验样本)。f,离体训练组与对照组细胞外囊泡纳米颗粒追踪分析(每组分析6个实验样本)。g,HSAcre; CD63-GFPki小鼠构建示意图。使用BioRender创建。Lin, J. (2026) https://biorender.com/7f9auln。h,有氧游泳运动HSAcre; CD63-GFPki小鼠比目鱼肌中GFP的免疫荧光分析。比例尺,20微米(每组分析6只小鼠)。i,HSAcre; CD63-GFPki小鼠脑组织中GFP的免疫荧光分析。比例尺,50微米(每组分析6只小鼠)。a–f采用单批独立野生型小鼠(每组6只)。g–i采用单批独立HSAcre-CD63-GFPki小鼠(每组6只)。组间统计学显著性通过双尾非配对t检验(a、c、f、h、i)进行计算。- 三、SKM-EVs 是运动改善 AD 的核心效应因子 尾静脉注射运动诱导的 SKM-EVs,可复刻运动的效果,显著改善 AD 小鼠认知、促进 DAM 极化和 Aβ 斑块清除;而特异性阻断骨骼肌 EVs 的分泌,则会完全消除运动对 AD 小鼠的认知保护作用。
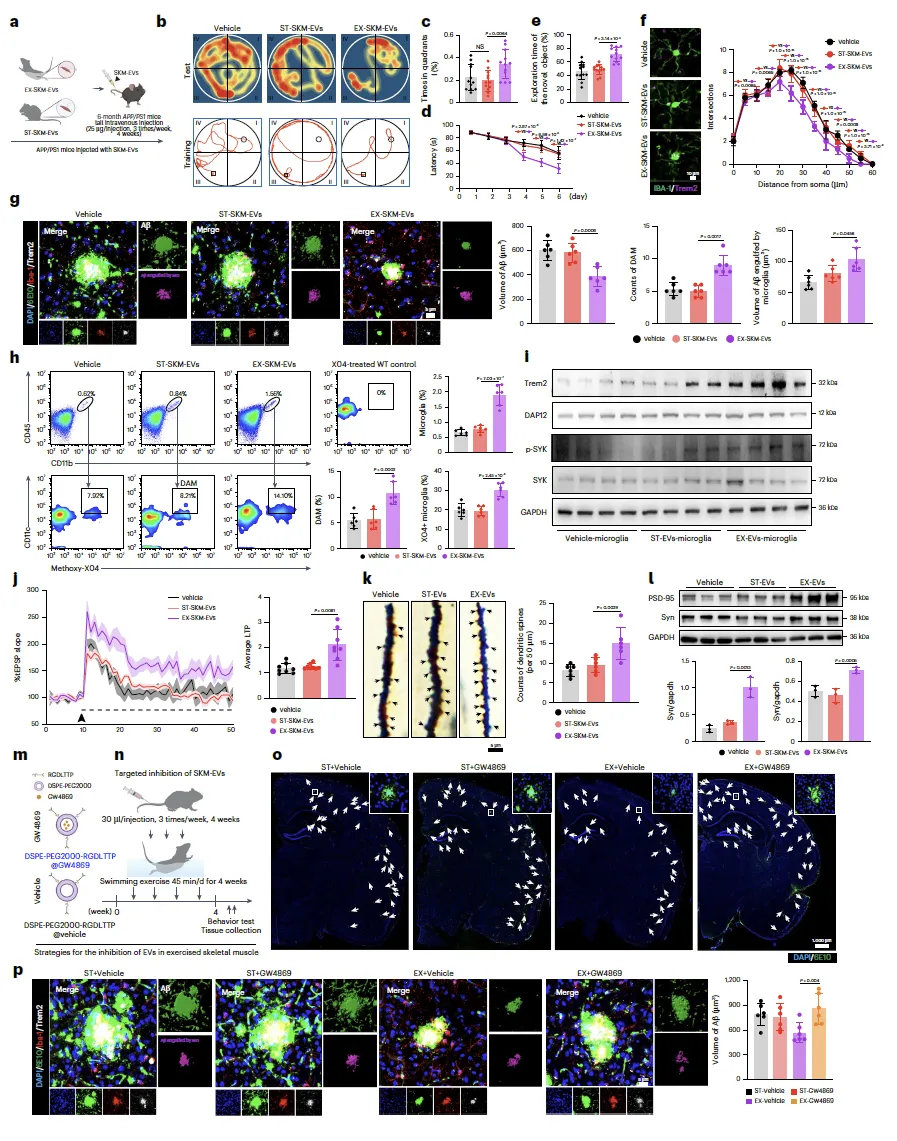 图3:功能获得与缺失实验表明,运动诱导的骨骼肌来源细胞外囊泡可通过激活小胶质细胞改善APP/PS1小鼠认知功能。a,骨骼肌来源细胞外囊泡给药示意图。使用BioRender创建。Lin, J. (2026) https://biorender.com/7f9auln。b,水迷宫实验热图。c,骨骼肌来源细胞外囊泡处理的APP/PS1小鼠水迷宫实验阶段行为学分析(每组分析12只小鼠)。d,骨骼肌来源细胞外囊泡处理的APP/PS1小鼠水迷宫训练阶段行为学分析(每组分析12只小鼠)。e,骨骼肌来源细胞外囊泡处理的APP/PS1小鼠新物体识别实验行为学分析(每组分析12只小鼠)。f,对邻近淀粉样斑块但未直接接触斑块的小胶质细胞进行三维结构重建与Sholl分析;每只小鼠选取5-10个小胶质细胞生成一个生物学重复值用于Sholl分析。比例尺,20微米(每组分析6只小鼠)。g,每只小鼠选取20-25个淀粉样斑块进行三维结构重建分析。比例尺,5微米(每组分析6只小鼠)。h,小胶质细胞、X04+小胶质细胞及X04+CD11c+疾病相关小胶质细胞的流式细胞术分析(每组分析6只小鼠)。i,脑组织小胶质细胞TREM2-DAP12-SYK蛋白表达免疫印迹分析。样品源自同一实验,p-SYK凝胶平行处理(每组分析4只小鼠)。j,骨骼肌来源细胞外囊泡处理的APP/PS1小鼠长时程增强测定(每组分析8只小鼠)。k,骨骼肌来源细胞外囊泡处理的APP/PS1小鼠高尔基染色分析(每组分析6只小鼠)。l,骨骼肌来源细胞外囊泡处理的APP/PS1小鼠脑组织PSD-95和Syn蛋白表达免疫印迹分析(每组分析3只小鼠)。m,DSPE-PEG2000-RGDLTTP@GW4869构建示意图。使用BioRender创建。Lin, J. (2026) https://biorender.com/7f9auln。n,DSPE-PEG2000-RGDLTTP@GW4869给药示意图。使用BioRender创建。Lin, J. (2026) https://biorender.com/7f9auln。o,淀粉样斑块免疫荧光染色。比例尺,1000微米(每组分析6只小鼠)。p,淀粉样斑块三维结构重建分析。比例尺,5微米(每组分析6只小鼠)。a–l采用三批独立APP/PS1小鼠:第一批AD小鼠(每组12只)在完成水迷宫、旷场和新物体识别任务后用于免疫荧光分析(每组6只)和流式细胞术分析(h,每组6只);第二批AD小鼠(每组12只)用于长时程增强测定(每组8只)和免疫印迹分析(每组4只);第三批AD小鼠(每组9只)用于高尔基染色(每组6只)和免疫印迹分析(每组3只)。m–o采用单批独立APP/PS1小鼠。组间统计学显著性通过单因素方差分析结合Tukey多重比较检验(c、e、g、h、j、k、l、p)、重复测量双因素方差分析结合Tukey多重比较检验(d)及双因素方差分析结合Bonferroni事后检验(f)进行计算。数据以平均值±标准误表示
图3:功能获得与缺失实验表明,运动诱导的骨骼肌来源细胞外囊泡可通过激活小胶质细胞改善APP/PS1小鼠认知功能。a,骨骼肌来源细胞外囊泡给药示意图。使用BioRender创建。Lin, J. (2026) https://biorender.com/7f9auln。b,水迷宫实验热图。c,骨骼肌来源细胞外囊泡处理的APP/PS1小鼠水迷宫实验阶段行为学分析(每组分析12只小鼠)。d,骨骼肌来源细胞外囊泡处理的APP/PS1小鼠水迷宫训练阶段行为学分析(每组分析12只小鼠)。e,骨骼肌来源细胞外囊泡处理的APP/PS1小鼠新物体识别实验行为学分析(每组分析12只小鼠)。f,对邻近淀粉样斑块但未直接接触斑块的小胶质细胞进行三维结构重建与Sholl分析;每只小鼠选取5-10个小胶质细胞生成一个生物学重复值用于Sholl分析。比例尺,20微米(每组分析6只小鼠)。g,每只小鼠选取20-25个淀粉样斑块进行三维结构重建分析。比例尺,5微米(每组分析6只小鼠)。h,小胶质细胞、X04+小胶质细胞及X04+CD11c+疾病相关小胶质细胞的流式细胞术分析(每组分析6只小鼠)。i,脑组织小胶质细胞TREM2-DAP12-SYK蛋白表达免疫印迹分析。样品源自同一实验,p-SYK凝胶平行处理(每组分析4只小鼠)。j,骨骼肌来源细胞外囊泡处理的APP/PS1小鼠长时程增强测定(每组分析8只小鼠)。k,骨骼肌来源细胞外囊泡处理的APP/PS1小鼠高尔基染色分析(每组分析6只小鼠)。l,骨骼肌来源细胞外囊泡处理的APP/PS1小鼠脑组织PSD-95和Syn蛋白表达免疫印迹分析(每组分析3只小鼠)。m,DSPE-PEG2000-RGDLTTP@GW4869构建示意图。使用BioRender创建。Lin, J. (2026) https://biorender.com/7f9auln。n,DSPE-PEG2000-RGDLTTP@GW4869给药示意图。使用BioRender创建。Lin, J. (2026) https://biorender.com/7f9auln。o,淀粉样斑块免疫荧光染色。比例尺,1000微米(每组分析6只小鼠)。p,淀粉样斑块三维结构重建分析。比例尺,5微米(每组分析6只小鼠)。a–l采用三批独立APP/PS1小鼠:第一批AD小鼠(每组12只)在完成水迷宫、旷场和新物体识别任务后用于免疫荧光分析(每组6只)和流式细胞术分析(h,每组6只);第二批AD小鼠(每组12只)用于长时程增强测定(每组8只)和免疫印迹分析(每组4只);第三批AD小鼠(每组9只)用于高尔基染色(每组6只)和免疫印迹分析(每组3只)。m–o采用单批独立APP/PS1小鼠。组间统计学显著性通过单因素方差分析结合Tukey多重比较检验(c、e、g、h、j、k、l、p)、重复测量双因素方差分析结合Tukey多重比较检验(d)及双因素方差分析结合Bonferroni事后检验(f)进行计算。数据以平均值±标准误表示- 四、miR-378a-3p 是 SKM-EVs 中的关键功能分子 骨骼肌特异性敲除 miRNA 加工关键基因 Dicer1 后,运动的认知改善作用消失;通过 miRNA 测序筛选,发现 miR-378a-3p 在运动诱导的 SKM-EVs 中显著上调,且是唯一在骨骼肌和 SKM-EVs 中均被运动激活的骨骼肌富集 miRNA。
- 图4:运动诱导的骨骼肌来源细胞外囊泡中的miR-378a-3p是介导游泳运动改善AD认知功能获益的主要分子。a,骨骼肌来源细胞外囊泡处理APP/PS1小鼠示意图。使用BioRender创建。Lin, J. (2026) https://biorender.com/7f9auln。b,接受野生型静息状态骨骼肌来源细胞外囊泡、条件性敲除静息状态骨骼肌来源细胞外囊泡、野生型运动状态骨骼肌来源细胞外囊泡和条件性敲除运动状态骨骼肌来源细胞外囊泡处理的APP/PS1小鼠水迷宫实验行为学分析(每组分析12只小鼠)。c,运动状态与静息状态骨骼肌来源细胞外囊泡的miRNA测序分析。d,候选miRNA的韦恩图分析。e,候选miR-378a-3p、miR-378c和miR-22-3p的PCR分析(每组分析6个实验样本)。f,比目鱼肌和骨骼肌来源细胞外囊泡中候选miRNA的PCR分析(每组分析6个实验样本)。g,皮层和海马中候选miRNA的PCR分析(每组分析6个实验样本)。h,比目鱼肌、皮层和海马中pri-miR-378a的PCR分析(每组分析6个实验样本)。a和b采用单批独立APP/PS1小鼠(每组12只)。e–h采用另一批独立APP/PS1小鼠(每组6只)。组间统计学显著性通过双尾非配对t检验(f–h)进行计算。
- 五、miR-378a-3p 通过调控脂质代谢激活小胶质细胞 海马注射 miR-378a-3p 激动剂、骨骼肌特异性过表达 miR-378a-3p,均可促进 DAM 极化和 Aβ 清除,改善 AD 小鼠认知;机制上,miR-378a-3p 靶向抑制 p110α,上调脂蛋白脂酶(LPL)表达,增强小胶质细胞脂质代谢和 ATP 生成,进而提升其吞噬功能。
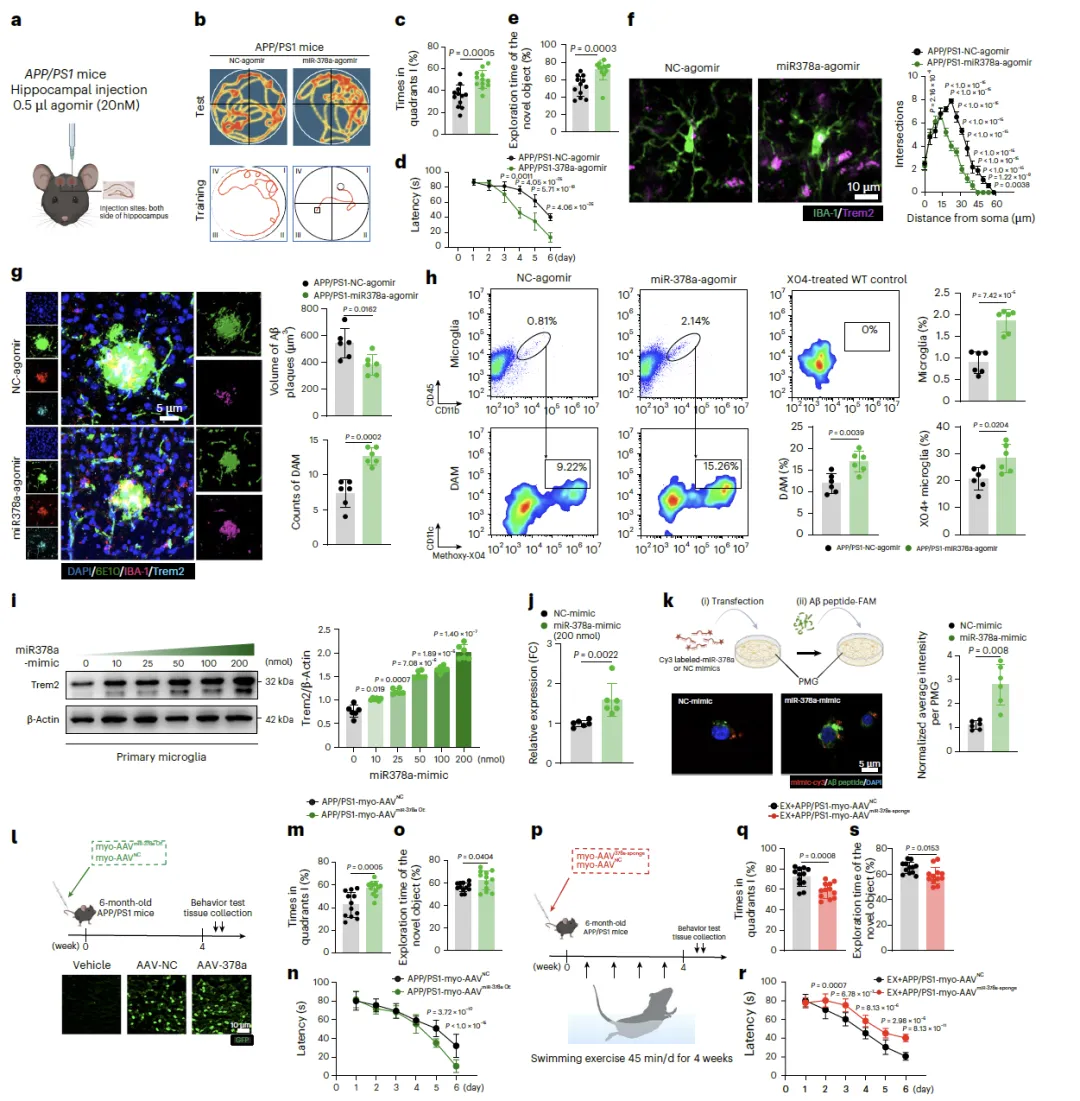 图5:miR-378a-3p改善小鼠认知功能并促进疾病相关小胶质细胞激活。a,agomir注射示意图。使用BioRender创建。Lin, J. (2026) https://biorender.com/7f9auln。b,水迷宫实验热图。c,注射agomir的APP/PS1小鼠水迷宫实验阶段行为学分析(每组分析12只小鼠)。d,注射agomir的APP/PS1小鼠水迷宫训练阶段行为学分析(每组分析12只小鼠)。e,注射agomir的APP/PS1小鼠新物体识别实验行为学分析(每组分析12只小鼠)。f,对邻近淀粉样斑块但未直接接触斑块的小胶质细胞进行三维结构重建与Sholl分析;每只小鼠选取5-10个小胶质细胞生成一个生物学重复值用于Sholl分析。比例尺,10微米(每组分析6只小鼠)。g,每只小鼠选取20-25个淀粉样斑块进行三维结构重建分析。比例尺,5微米(每组分析6只小鼠)。h,小胶质细胞、甲氧基-X04+小胶质细胞及X04+CD11c+疾病相关小胶质细胞的流式细胞术分析(每组分析6只小鼠)。i,Trem2蛋白水平免疫印迹分析(每组分析6个实验样本)。j,Trem2转录水平PCR分析(每组分析6个实验样本)。k,与mimic和Aβ肽-FAM共培养的小胶质细胞免疫荧光分析。比例尺,5微米(每组分析6个实验样本)。l,AAV-378a-OE和AAV-NC给药示意图。使用BioRender创建。Lin, J. (2026) https://biorender.com/7f9auln。比例尺,10微米。m,注射AAV的APP/PS1小鼠水迷宫实验阶段行为学分析(每组分析12只小鼠)。n,注射AAV的APP/PS1小鼠水迷宫训练阶段行为学分析(每组分析12只小鼠)。o,注射AAV的APP/PS1小鼠新物体识别实验行为学分析(每组分析12只小鼠)。p,AAV-378a-sponge和AAV-NC给药及有氧运动训练策略示意图。使用BioRender创建。Lin, J. (2026) https://biorender.com/7f9auln。q,注射AAV-Sponge的运动APP/PS1小鼠水迷宫实验阶段行为学分析(每组分析12只小鼠)。r,注射AAV-Sponge的运动APP/PS1小鼠水迷宫训练阶段行为学分析(每组分析12只小鼠)。s,注射AAV-Sponge的运动APP/PS1小鼠新物体识别实验行为学分析(每组分析12只小鼠)。a–h采用单批独立APP/PS1小鼠:认知行为测试后,每组6只用于免疫荧光分析,每组6只用于流式细胞术分析(每组共12只)。l–s采用两批独立APP/PS1小鼠(每组12只)。组间统计学显著性通过重复测量双因素方差分析结合Tukey多重比较检验(d、n、r)、双尾非配对t检验(c、e、g、h、k、m、o、q、s)、单因素方差分析结合Tukey多重比较检验(i)及双因素方差分析结合Bonferroni多重比较检验(f)进行计算。
图5:miR-378a-3p改善小鼠认知功能并促进疾病相关小胶质细胞激活。a,agomir注射示意图。使用BioRender创建。Lin, J. (2026) https://biorender.com/7f9auln。b,水迷宫实验热图。c,注射agomir的APP/PS1小鼠水迷宫实验阶段行为学分析(每组分析12只小鼠)。d,注射agomir的APP/PS1小鼠水迷宫训练阶段行为学分析(每组分析12只小鼠)。e,注射agomir的APP/PS1小鼠新物体识别实验行为学分析(每组分析12只小鼠)。f,对邻近淀粉样斑块但未直接接触斑块的小胶质细胞进行三维结构重建与Sholl分析;每只小鼠选取5-10个小胶质细胞生成一个生物学重复值用于Sholl分析。比例尺,10微米(每组分析6只小鼠)。g,每只小鼠选取20-25个淀粉样斑块进行三维结构重建分析。比例尺,5微米(每组分析6只小鼠)。h,小胶质细胞、甲氧基-X04+小胶质细胞及X04+CD11c+疾病相关小胶质细胞的流式细胞术分析(每组分析6只小鼠)。i,Trem2蛋白水平免疫印迹分析(每组分析6个实验样本)。j,Trem2转录水平PCR分析(每组分析6个实验样本)。k,与mimic和Aβ肽-FAM共培养的小胶质细胞免疫荧光分析。比例尺,5微米(每组分析6个实验样本)。l,AAV-378a-OE和AAV-NC给药示意图。使用BioRender创建。Lin, J. (2026) https://biorender.com/7f9auln。比例尺,10微米。m,注射AAV的APP/PS1小鼠水迷宫实验阶段行为学分析(每组分析12只小鼠)。n,注射AAV的APP/PS1小鼠水迷宫训练阶段行为学分析(每组分析12只小鼠)。o,注射AAV的APP/PS1小鼠新物体识别实验行为学分析(每组分析12只小鼠)。p,AAV-378a-sponge和AAV-NC给药及有氧运动训练策略示意图。使用BioRender创建。Lin, J. (2026) https://biorender.com/7f9auln。q,注射AAV-Sponge的运动APP/PS1小鼠水迷宫实验阶段行为学分析(每组分析12只小鼠)。r,注射AAV-Sponge的运动APP/PS1小鼠水迷宫训练阶段行为学分析(每组分析12只小鼠)。s,注射AAV-Sponge的运动APP/PS1小鼠新物体识别实验行为学分析(每组分析12只小鼠)。a–h采用单批独立APP/PS1小鼠:认知行为测试后,每组6只用于免疫荧光分析,每组6只用于流式细胞术分析(每组共12只)。l–s采用两批独立APP/PS1小鼠(每组12只)。组间统计学显著性通过重复测量双因素方差分析结合Tukey多重比较检验(d、n、r)、双尾非配对t检验(c、e、g、h、k、m、o、q、s)、单因素方差分析结合Tukey多重比较检验(i)及双因素方差分析结合Bonferroni多重比较检验(f)进行计算。- 图6:miR-378a-3p通过靶向p110α增强脂质代谢并促进小胶质细胞激活。a,经Aβ和miR-378a-3p模拟物处理的原代小胶质细胞的KEGG通路富集分析。b,模拟物处理的小胶质细胞中脂肪酸、甘油三酯和花生四烯酸含量测定(每组分析6个实验样本)。c,模拟物和抑制剂处理的原代小胶质细胞及小胶质细胞中ATP水平测定(每组分析6个实验样本)。d,模拟物处理的小胶质细胞中脂质代谢相关基因转录水平PCR分析(每组分析6个实验样本)。e,模拟物和抑制剂处理的小胶质细胞中LPL蛋白水平免疫印迹与分析(每组分析4个实验样本)。f,不同浓度模拟物处理的小胶质细胞中LPL蛋白水平免疫印迹与分析(0–200 nmol;每组分析3个实验样本)。g,不同浓度模拟物处理的原代小胶质细胞中ATP水平测定(0–200 nmol;每组分析6个实验样本)。h,模拟物和抑制剂处理的原代小胶质细胞中p110α蛋白水平免疫印迹与分析(每组分析3个实验样本)及p110α转录水平PCR分析(每组分析6个实验样本)。i,miR-378a-3p模拟物处理的原代小胶质细胞中p110α–AKT–GSK3β–Foxo1信号通路免疫印迹分析(每组分析6个实验样本)。j,图i中p110α–AKT–GSK3β–Foxo1信号通路的定量分析。k,AS1842856给药示意图。使用BioRender创建。Lin, J. (2026) https://biorender.com/7f9auln。AS1842856处理的原代小胶质细胞中LPL蛋白免疫印迹(每组分析6个实验样本)。l,图l中LPL蛋白的定量分析。m,AS1842856处理的原代小胶质细胞中LPL转录水平PCR分析(每组分析6个实验样本)。n,AS1842856处理的原代小胶质细胞中ATP水平测定(每组分析6个实验样本)。数据以平均值±标准误表示。组间统计学显著性通过双尾非配对t检验(b、d、j、m、n、o)、单因素方差分析结合Tukey多重比较检验(c、e、h)及单因素方差分析结合Dunnett多重比较检验(f、g)进行计算。
- 六、过表达 miR-378a-3p 的肌管 EVs 具有治疗潜力
体外构建 miR-378a-3p 过表达的 C2C12 肌管细胞,其分泌的 EVs 经尾静脉注射后,可有效减少 AD 小鼠脑内 Aβ 斑块、激活 DAM、改善突触可塑性和认知功能,且该效应依赖于小胶质细胞的存在。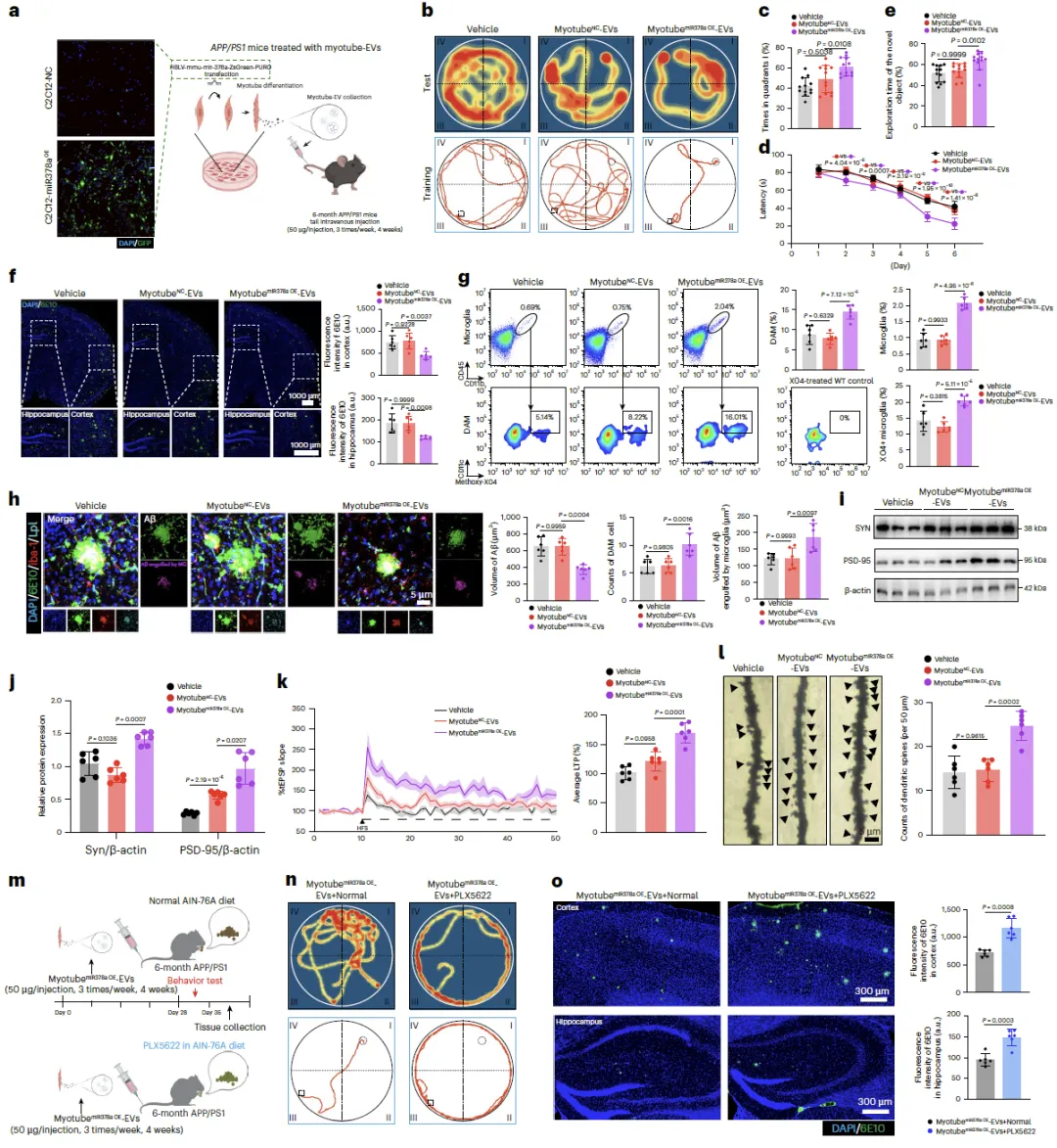
图7:过表达miR-378a-3p的肌管来源细胞外囊泡治疗性给药可缓解AD小鼠认知功能障碍。a,过表达miR-378a-3p的肌管来源细胞外囊泡处理APP/PS1小鼠示意图。使用BioRender创建。Lin, J. (2026) https://biorender.com/7f9auln。b,水迷宫实验热图。c,注射溶媒对照、过表达miR-378a-3p肌管来源细胞外囊泡或对照肌管来源细胞外囊泡的APP/PS1小鼠水迷宫实验阶段行为学分析(每组分析12只小鼠)。d,注射溶媒对照、过表达miR-378a-3p肌管来源细胞外囊泡或对照肌管来源细胞外囊泡的APP/PS1小鼠水迷宫训练阶段行为学分析(每组分析12只小鼠)。e,注射溶媒对照、过表达miR-378a-3p肌管来源细胞外囊泡或对照肌管来源细胞外囊泡的APP/PS1小鼠新物体识别实验行为学分析(每组分析12只小鼠)。f,注射溶媒对照、过表达miR-378a-3p肌管来源细胞外囊泡或对照肌管来源细胞外囊泡的APP/PS1小鼠脑组织Aβ免疫荧光分析(每组分析6只小鼠)。g,注射溶媒对照、过表达miR-378a-3p肌管来源细胞外囊泡或对照肌管来源细胞外囊泡的APP/PS1小鼠脑组织小胶质细胞、X04+小胶质细胞及X04+CD11c+疾病相关小胶质细胞流式细胞术分析(每组分析6只小鼠)。h,每只小鼠选取20-25个淀粉样斑块进行三维结构重建分析。比例尺,5微米(每组分析6只小鼠)。i,注射溶媒对照、过表达miR-378a-3p肌管来源细胞外囊泡或对照肌管来源细胞外囊泡的APP/PS1小鼠脑组织SYN和PSD-95蛋白水平免疫印迹分析(每组分析6只小鼠)。j,图i中SYN和PSD-95蛋白免疫印迹的定量分析。k,注射溶媒对照、过表达miR-378a-3p肌管来源细胞外囊泡或对照肌管来源细胞外囊泡的APP/PS1小鼠长时程增强测定(每组分析6只小鼠)。l,注射溶媒对照、过表达miR-378a-3p肌管来源细胞外囊泡或对照肌管来源细胞外囊泡的APP/PS1小鼠高尔基染色及分析(每组分析6只小鼠)。m,注射过表达miR-378a-3p肌管来源细胞外囊泡的APP/PS1小鼠分别饲喂正常饮食和PLX5622饮食示意图。使用BioRender创建。Lin, J. (2026) https://biorender.com/7f9auln。n,注射过表达miR-378a-3p肌管来源细胞外囊泡的APP/PS1小鼠在正常饮食和PLX5622饮食下的水迷宫实验热图。o,脑组织皮层和海马区域淀粉样斑块分析(每组分析6只小鼠)。a–l采用两批独立APP/PS1小鼠:第一批AD小鼠(每组12只)在认知功能行为测试后用于免疫荧光分析(每组6只)和流式细胞术分析(每组6只);第二批AD小鼠(每组15只)用于免疫印迹分析、长时程增强测定和高尔基染色。m–o采用单批独立APP/PS1小鼠(每组12只)。数据以平均值±标准误表示。组间统计学显著性通过单因素方差分析结合Tukey多重比较检验(c、e、f–l)、双尾非配对t检验结合Welch校正(o)及重复测量双因素方差分析结合Tukey多重比较检验(d)进行计算。
全文总结
本研究首次系统阐明了运动介导的SKM-EVs-miR-378a-3p-p110α轴在改善阿尔茨海默病认知障碍中的核心作用及分子机制:游泳运动作为适度有氧运动,可激活骨骼肌的内分泌功能,促进富含 miR-378a-3p 的 SKM-EVs 分泌;该囊泡跨越血脑屏障后被小胶质细胞摄取,通过 miR-378a-3p 靶向抑制 p110α,调控 AKT-GSK3β-FoxO1-LPL 信号轴增强小胶质细胞脂质代谢,进而促进 DAM 极化和 Aβ 斑块清除,最终改善 AD 小鼠的认知功能。同时,研究证实过表达 miR-378a-3p 的肌管来源 EVs 可模拟运动的治疗效果,为 AD 提供了全新的 “运动模拟” 靶向治疗策略。此外,该研究还揭示了骨骼肌作为内分泌器官,在调节中枢神经系统功能中的重要作用,建立了骨骼肌生理与神经退行性疾病之间的直接联系。
编者的话
这项研究将骨骼肌的内分泌功能与神经退行性疾病紧密结合,为骨科领域的研究提供了全新的视角和方向,对未来骨科研究者具有多方面重要启示:
- 1、拓展骨骼肌生理功能的研究边界 骨科研究长期聚焦于骨骼肌的运动、支撑、损伤修复等经典功能,本研究证实骨骼肌的内分泌功能可远程调控中枢神经系统,提示骨科研究者应进一步关注骨骼肌作为 “内分泌器官” 的潜在价值,探索骨骼肌分泌的囊泡、细胞因子等在全身多器官调控中的作用。
- 2、推动骨科与神经科学的交叉研究 AD 等神经退行性疾病常伴随骨骼肌萎缩、运动能力下降,而本研究证实骨骼肌可反向调控大脑功能,为骨科研究开辟了 “骨骼肌 - 大脑轴” 的新方向。未来骨科研究者可围绕运动干预、骨骼肌损伤修复、肌萎缩等问题,探索其对神经系统疾病的影响及机制,实现骨科与神经科学的深度融合。
- 3、挖掘运动疗法在骨科相关合并症中的应用潜力 运动是骨科临床中重要的康复手段,本研究为运动疗法的 “跨界效益” 提供了分子依据。未来骨科研究者可探索不同运动方式、运动强度对骨骼肌分泌谱的调控规律,结合骨科患者常合并的认知障碍、神经损伤等问题,开发个性化的运动康复方案,实现 “治骨” 与 “治脑”、“康复” 与 “防病” 的双重目标。
- 4、探索骨骼肌来源生物制剂的研发方向 本研究证实骨骼肌来源 EVs 可作为治疗 AD 的新型生物制剂,提示骨科研究者可基于骨骼肌的分泌特性,开发针对骨科疾病及合并症的生物治疗手段。例如,探索骨骼肌 EVs 在骨损伤修复、骨质疏松、肌骨疼痛中的作用,或利用骨骼肌细胞工程改造分泌特定功能分子的 EVs,为骨科疾病提供新型靶向治疗策略。
- 5、关注肌骨代谢与神经代谢的协同调控 本研究发现脂质代谢是连接骨骼肌 EVs 与小胶质细胞功能的关键环节,而骨科领域的骨质疏松、肌萎缩等疾病也与代谢紊乱密切相关。未来骨科研究者可关注肌骨代谢与神经代谢的共同调控靶点,探索代谢干预在改善肌骨健康和神经系统功能中的双重作用,为代谢相关肌骨疾病和神经疾病的联合治疗提供新思路。