艰难梭菌感染治疗新靶点!南京中医药大学/温州医科大学2026年2月发表新研究:FBA-K280 乙酰化介导的糖酵解调控
- 2026-05-17 17:58:19
导 读
Introduction

一、研究背景解读
Background
二、研究思路解析
Train of Though
该研究采用细胞模型 + 体外细菌实验结合全蛋白质组学 + 赖氨酸乙酰化修饰组学的技术路线,从宿主保护和直接抗细菌两个维度,系统解析黄腐酚和丁酸梭菌上清液的抗 CDI 机制,整体研究思路分为 5 个核心步骤:
1. 构建细胞模型,验证黄腐酚的宿主保护作用
建立 DSS 诱导的 Caco-2 肠上皮细胞炎症模型,叠加艰难梭菌感染模拟临床 IBD 合并 CDI 的病理状态,通过细胞活力检测、炎症信号通路表达分析、宿主蛋白质组学检测,明确黄腐酚对肠上皮细胞的保护效应及对宿主蛋白组的调控作用。
2. 体外细菌实验,验证黄腐酚和 CBs 的直接抗艰难梭菌作用
通过细菌定植实验、生长动力学检测、毒素基因(tcdA、tcdB、tcdR)qRT-PCR 检测,评估黄腐酚和 CBs 对艰难梭菌定植、增殖及毒素产生的抑制效果。
3. 全蛋白质组学分析,解析二者对艰难梭菌蛋白组的重塑作用
分别对黄腐酚、CBs 处理后的艰难梭菌进行 TMT 标记的定量蛋白质组学检测,筛选差异表达蛋白(DEPs),通过 KEGG 富集、PPI 网络分析,明确二者调控的核心生物学通路。
4. 赖氨酸乙酰化修饰组学,挖掘核心调控的 PTMs 靶点
采用亲和富集结合 LC-MS/MS 的技术,绘制黄腐酚和 CBs 处理后艰难梭菌的赖氨酸乙酰化修饰图谱,筛选差异乙酰化位点和蛋白,定位修饰调控的核心代谢通路。
5. 功能验证,明确关键靶点的生物学作用
针对糖酵解通路的关键酶 ** 果糖 - 1,6 - 二磷酸醛缩酶(FBA)** 的 K280 乙酰化位点,通过定点突变、蛋白纯化、酶活检测,验证该乙酰化位点对酶催化活性及细菌糖酵解的调控作用,阐明分子机制。
实验技术与方法要点
菌株与细胞培养:严格厌氧培养艰难梭菌 ATCC BAA-1382 和丁酸梭菌 ATCC 19398,制备 CBs;常规培养 Caco-2 细胞,DSS 诱导建立炎症模型。
组学检测:TMT 标记定量蛋白质组学、赖氨酸乙酰化肽段亲和富集、LC-MS/MS 质谱分析,MaxQuant 进行数据处理,STRING/Cytoscape 进行生物信息学分析。
功能验证:质粒构建与蛋白纯化、定点突变(FBA-K280A)、酶活检测、qRT-PCR、CCK-8、CFSE 荧光标记定植实验等。
统计分析:GraphPad Prism 9.5,独立样本 t 检验、单因素方差分析,p<0.05 为差异显著。
三、研究主要结果展示
ResultDemonstraion
该研究首次从蛋白质组学和赖氨酸乙酰化修饰组学层面,阐明了黄腐酚和丁酸梭菌上清液抗艰难梭菌的共同分子机制:二者均通过调控艰难梭菌的赖氨酸乙酰化水平,靶向干扰糖酵解代谢通路,抑制细菌的定植、增殖和毒素产生,从而降低其致病性;同时,黄腐酚还能通过保护肠上皮细胞完整性、抑制 NF-κB/JNK 等炎症信号通路激活,发挥宿主肠道保护作用,适用于 IBD 合并 CDI 的病理状态。其中,果糖 - 1,6 - 二磷酸醛缩酶(FBA)的 K280 位点乙酰化是关键调控靶点,该位点的乙酰化状态直接决定 FBA 的催化活性,进而调控艰难梭菌糖酵解代谢和毒力表型。主要研究结果如下:
结果1: 黄腐酚缓解艰难梭菌叠加 DSS 诱导的 Caco-2 细胞损伤,抑制炎症信号通路
DSS 单独处理显著降低 Caco-2 细胞活力,叠加艰难梭菌感染后细胞损伤进一步加剧,而黄腐酚可显著恢复细胞活力,缓解协同损伤。
艰难梭菌感染显著上调 Caco-2 细胞中 NF-κB1、TAK1、TRAF6、JNK 等炎症信号通路关键基因的表达,黄腐酚可显著下调上述基因表达,发挥抗炎作用。
宿主蛋白质组学显示,艰难梭菌感染导致 Caco-2 细胞 156 个蛋白下调、226 个蛋白上调,核心影响类固醇生物合成等肠屏障相关通路;黄腐酚可逆转 32 个被艰难梭菌下调的蛋白和 33 个被上调的蛋白,重塑宿主蛋白组至正常水平。
结果2:黄腐酚和 CBs 均能体外抑制艰难梭菌的定植、增殖及毒素产生
定植抑制:CFSE 荧光标记实验显示,黄腐酚和 CBs 均可显著降低艰难梭菌对 Caco-2 细胞的黏附 / 内化能力。
生长抑制:细菌生长动力学检测表明,黄腐酚(50μM)和 CBs(1:100 比例)能显著抑制艰难梭菌的体外增殖。
毒素抑制:qRT-PCR 证实,二者均可显著下调艰难梭菌毒素基因 tcdA、tcdB 及其转录调控因子 tcdR 的表达,减少毒素合成。
结果3:黄腐酚和 CBs 重塑艰难梭菌的全蛋白质组,调控不同核心通路
黄腐酚:在艰难梭菌中鉴定出 2251 个蛋白(覆盖其已知蛋白组 60%),筛选出 662 个差异表达蛋白(286 下调、376 上调),核心富集于氨基酸生物合成、碳代谢、鞭毛组装等通路;其中鞭毛组装相关蛋白显著下调,解释了其定植抑制作用,而代谢通路蛋白普遍上调,提示细菌产生代谢代偿性应激。
CBs:筛选出 435 个差异表达蛋白(360 下调、75 上调),核心富集于同源重组和核糖体生物发生通路;其中核糖体大小亚基共 35 个蛋白显著下调,抑制细菌蛋白质合成,同时同源重组修复蛋白上调,提示细菌应对应激的 DNA 修复反应。
二者共同下调鞭毛组装通路相关蛋白,提示这是其抗艰难梭菌的共同靶点之一。
结果4:黄腐酚和 CBs 通过调控赖氨酸乙酰化,靶向干预艰难梭菌糖酵解通路
黄腐酚的乙酰化调控:鉴定出 733 个蛋白的 2653 个赖氨酸乙酰化位点,61% 的蛋白含多个修饰位点;差异乙酰化蛋白核心富集于碳代谢、糖酵解 / 糖异生通路,糖酵解关键酶(FBA-K280、ENO-K105)呈高乙酰化,而核糖体蛋白乙酰化水平显著下调。
CBs 的乙酰化调控:鉴定出 708 个蛋白的 2266 个赖氨酸乙酰化位点;差异乙酰化蛋白与核糖体组分高度相关,同时糖酵解通路酶的丰度显著降低,乙酰化修饰整体下调。
二者共有 162 个乙酰化位点发生改变,其中 11 个位于糖酵解关键酶上,提示糖酵解通路的赖氨酸乙酰化调控是二者抗艰难梭菌的核心共同机制。
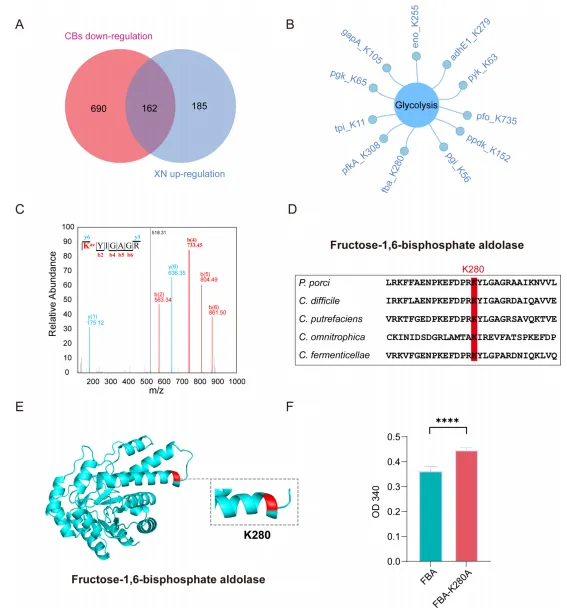
结果5:FBA-K280 乙酰化是调控艰难梭菌糖酵解的关键靶点
质谱鉴定发现艰难梭菌 FBA 的 K280 位点存在特异性乙酰化,该位点在多种梭菌中高度保守,且位于 FBA 的催化结构域,对酶的结构完整性至关重要。
定点突变构建 FBA-K280A(赖氨酸突变为丙氨酸,消除乙酰化),酶活检测显示,突变体的催化活性显著降低,证实 K280 乙酰化是维持 FBA 酶活的必要条件。
黄腐酚和 CBs 通过调控 FBA-K280 乙酰化水平,干扰艰难梭菌糖酵解代谢通量,进而抑制细菌能量代谢和毒力。
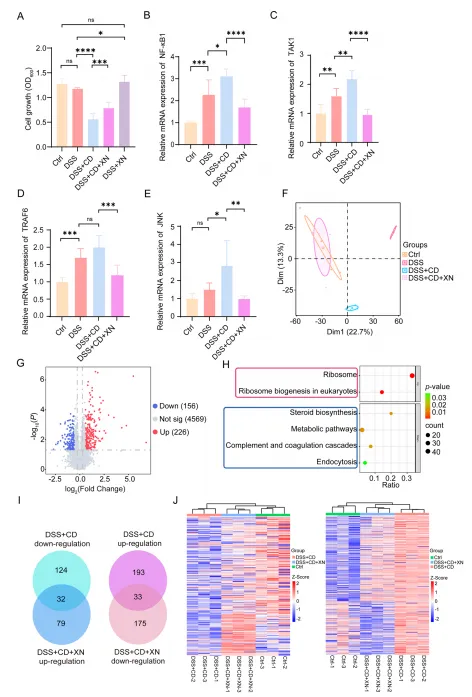
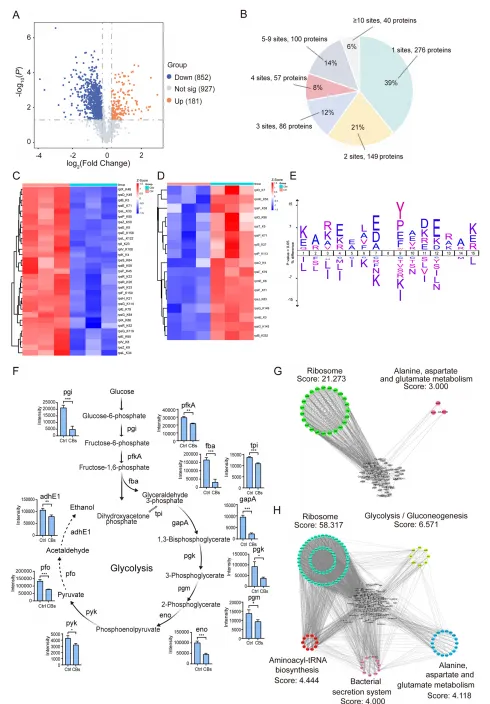
Fig. 1:艰难梭菌(C. difficile) 会加重 DSS 诱导的 Caco-2 细胞损伤,而XN可缓解这一效应
本研究通过细胞活力检测、炎症因子表达分析、蛋白质组学主成分分析、火山图、KEGG 通路富集及维恩图等多维度实验手段,证实了艰难梭菌(C. difficile)可显著加重 DSS 诱导的 Caco-2 细胞损伤,其机制可能与激活 NF-κB 等炎症通路、调控大量差异表达蛋白及相关信号通路密切相关;而XN(某种干预物质)则可有效逆转这一损伤效应,通过上调被艰难梭菌抑制的关键蛋白表达,发挥细胞保护作用,为临床应对艰难梭菌相关肠道损伤提供了潜在的干预靶点与策略。
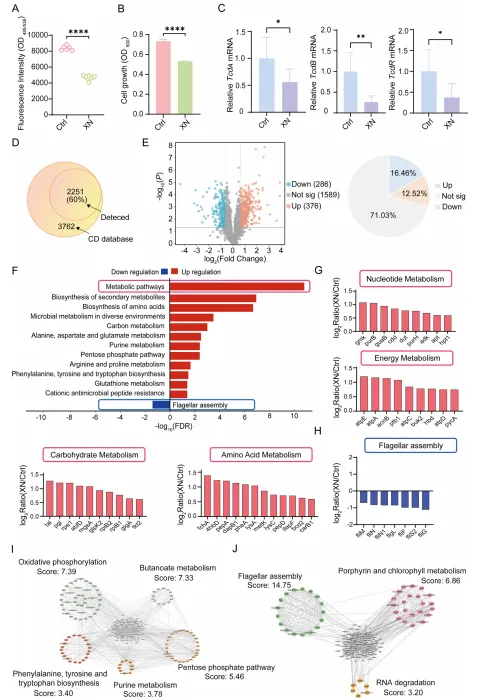
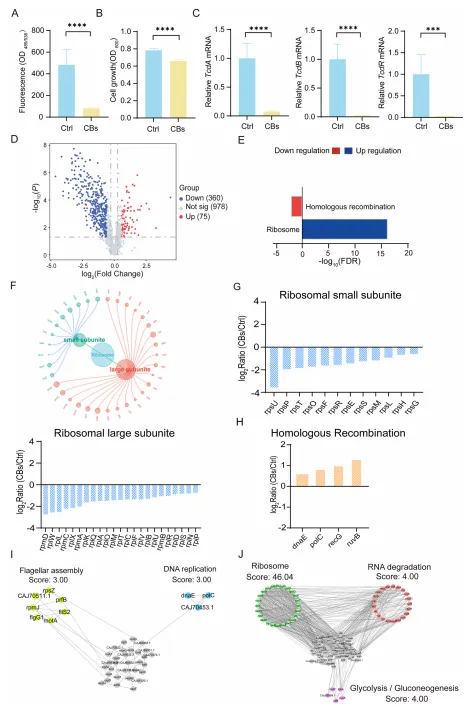
该研究通过乙酰化组学系统分析,揭示了XN 干预可显著调控艰难梭菌的赖氨酸乙酰化修饰,在全菌范围内鉴定出大量差异乙酰化位点及蛋白,并发现这些乙酰化蛋白主要富集于糖酵解 / 糖异生等核心代谢通路;其中,XN 可通过调控糖酵解关键酶(如 pgi、fba、pfk、pyk 等)的乙酰化水平,重塑艰难梭菌的代谢调控网络,进而干扰其能量代谢与致病进程,为靶向乙酰化修饰开发抗艰难梭菌感染的干预策略提供了新的分子靶点与理论依据。
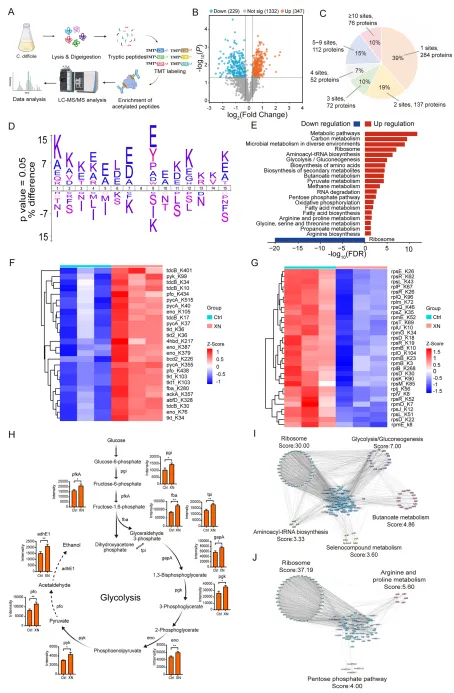
四、总 结
Summary
该研究通过蛋白质组学与赖氨酸乙酰化修饰组学技术,系统阐明了黄腐酚和丁酸梭菌上清液抗艰难梭菌的核心分子机制,二者均能通过调控艰难梭菌的赖氨酸乙酰化水平,靶向干扰糖酵解代谢通路,抑制细菌定植、增殖与毒素产生,从而降低其致病性;其中果糖 - 1,6 - 二磷酸醛缩酶(FBA)的 K280 位点乙酰化是关键调控靶点,该位点的乙酰化状态直接决定其催化活性,进而影响艰难梭菌的能量代谢与毒力表型。同时黄腐酚还兼具宿主肠道保护作用,可缓解艰难梭菌叠加结肠炎引发的肠上皮细胞损伤,抑制 NF-κB、JNK 等炎症信号通路激活,对炎症性肠病合并艰难梭菌感染的病理状态尤为适用。
该研究填补了天然产物调控艰难梭菌翻译后修饰的研究空白,首次发现糖酵解通路乙酰化修饰这一抗艰难梭菌新靶点,证实了黄腐酚和丁酸梭菌上清液作为低毒性、非抗生素类抗艰难梭菌感染候选方案的潜力,为解决临床抗生素耐药问题提供了全新思路。研究也存在一定局限性,仅基于体外细胞模型完成验证,尚未明确二者调控乙酰化的直接分子靶点,未来需在动物模型与临床样本中进一步验证,并探究二者协同作用及其他酰化修饰的调控机制,为艰难梭菌感染的精准治疗提供更坚实的理论与实验基础。
https://link.springer.com/article/10.1186/s13020-026-01343-x


