药物降脂致心缺陷:为验证人群发现的因果关系,研究人员采用两种叶酸代谢干扰药物处理怀孕母鼠:甲氨蝶呤(抑制二氢叶酸还原酶)和磺胺嘧啶(抑制肠道菌群叶酸合成)【图2A】。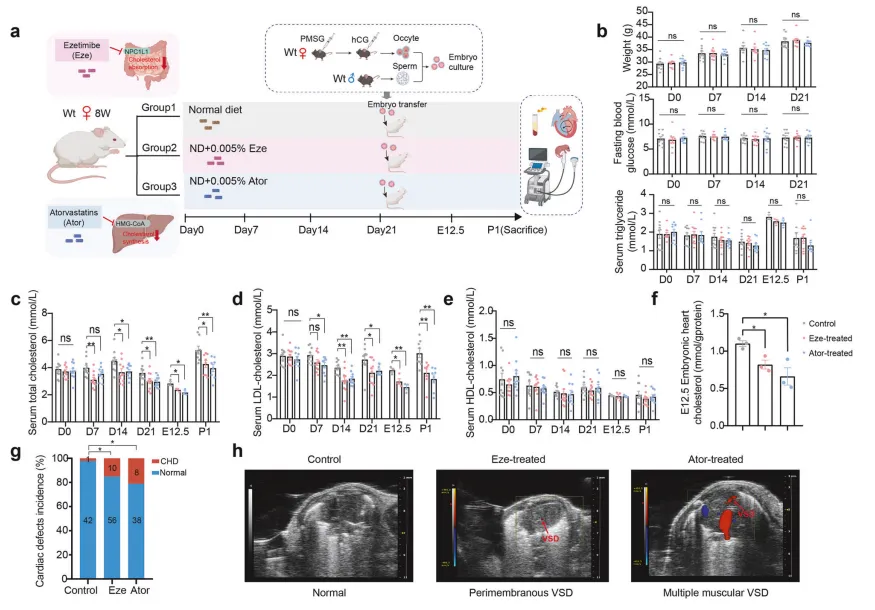 结果显示,药物处理成功降低了孕鼠血清及胚胎神经管的叶酸水平【图2C-F】,并直接导致子代神经管缺陷发生率显著升高:对照组仅为1.8%,甲氨蝶呤组升至16.5%,磺胺嘧啶组达14.2%【图2G】,证实孕期母体叶酸短期缺乏即可严重干扰胚胎神经管闭合过程。
结果显示,药物处理成功降低了孕鼠血清及胚胎神经管的叶酸水平【图2C-F】,并直接导致子代神经管缺陷发生率显著升高:对照组仅为1.8%,甲氨蝶呤组升至16.5%,磺胺嘧啶组达14.2%【图2G】,证实孕期母体叶酸短期缺乏即可严重干扰胚胎神经管闭合过程。
对86例神经管缺陷患儿的全基因组测序显示,叶酸代谢关键基因MTHFR的功能性突变(C677T)与疾病高度相关。
该突变在人群中携带率较高,在两个独立出生队列验证中均显示,携带者神经管缺陷风险为正常人群的2.8~3.5倍。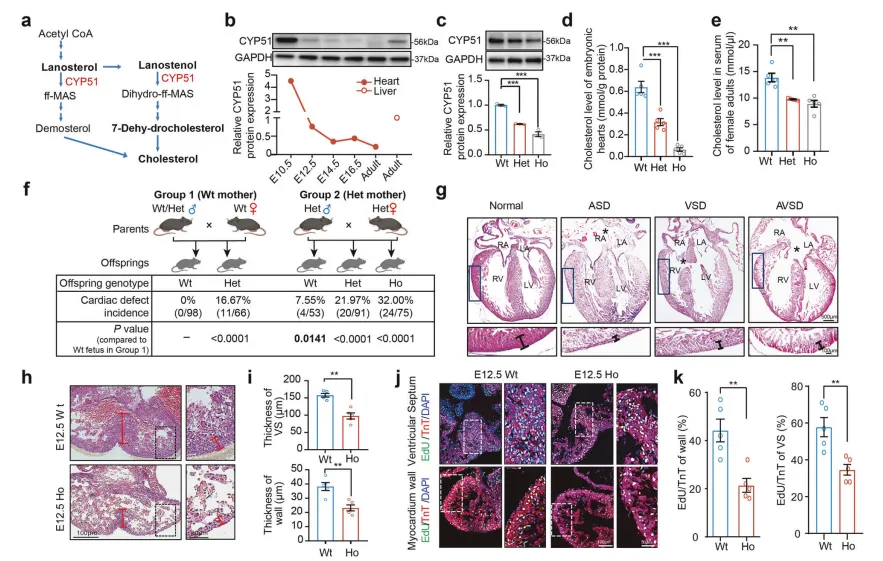
构建携带同源突变的Mthfr基因敲入小鼠模型证实,该突变导致MTHFR酶活性显著下降【图3C】,纯合突变小鼠胚胎神经管及胚胎组织中叶酸水平降低约70%【图3D】,28%的新生纯合突变小鼠出现脊柱裂、无脑畸形等神经管缺陷表型【图3F-H】。
核心机制在于突变体神经上皮细胞增殖能力显著受损,导致神经褶闭合延迟、融合失败【图3J, K】。
单细胞测序分析发现,突变体神经上皮细胞中胚胎发育关键通路Wnt/β-catenin的活性显著抑制【图4A, B】,该通路的信号传导高度依赖叶酸介导的DNA甲基化修饰: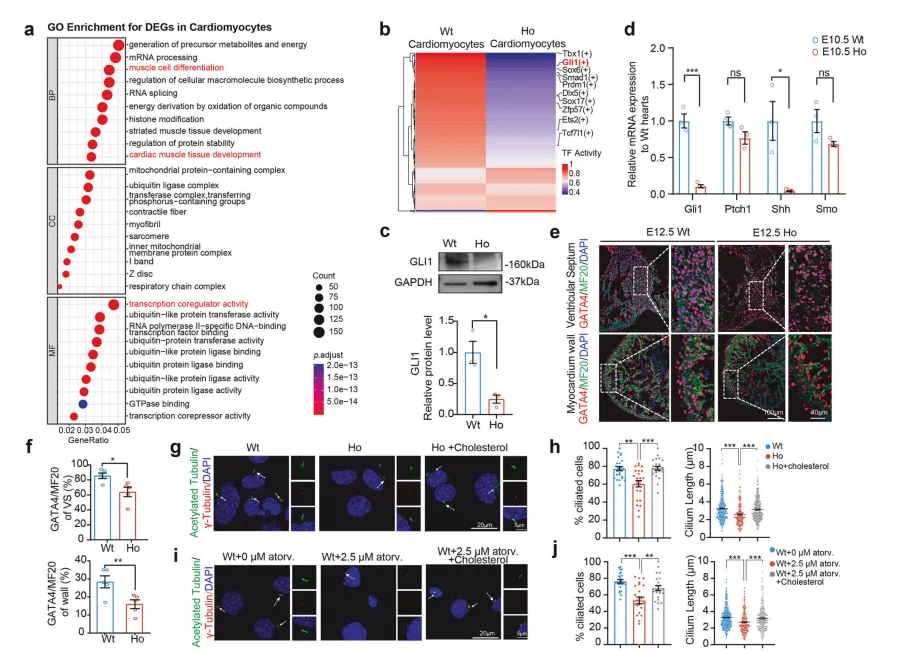
直接抑制通路核心蛋白:突变体中Wnt/β-catenin通路核心效应蛋白β-catenin的核内积累显著减少【图4C】;
破坏信号接收微环境:神经上皮细胞顶端的肌动蛋白骨架是维持Wnt信号极性的结构基础,叶酸缺乏导致骨架紊乱、极性丧失,信号传导效率大幅下降【图4G-J】。
β-catenin可直接结合神经管闭合关键转录因子Pax3的启动子调控其表达,最终形成“叶酸缺乏→骨架紊乱→Wnt信号减弱→Pax3表达下降→神经管闭合缺陷”的完整致病链条【图4E, F】。
“挽救实验”显示,给携带Mthfrᶜ⁶⁷⁷ᵀ突变的怀孕母鼠补充高剂量5-甲基四氢叶酸后,纯合突变子代小鼠的神经管缺陷发病率从28.3%大幅降至6.9%【图5C】。
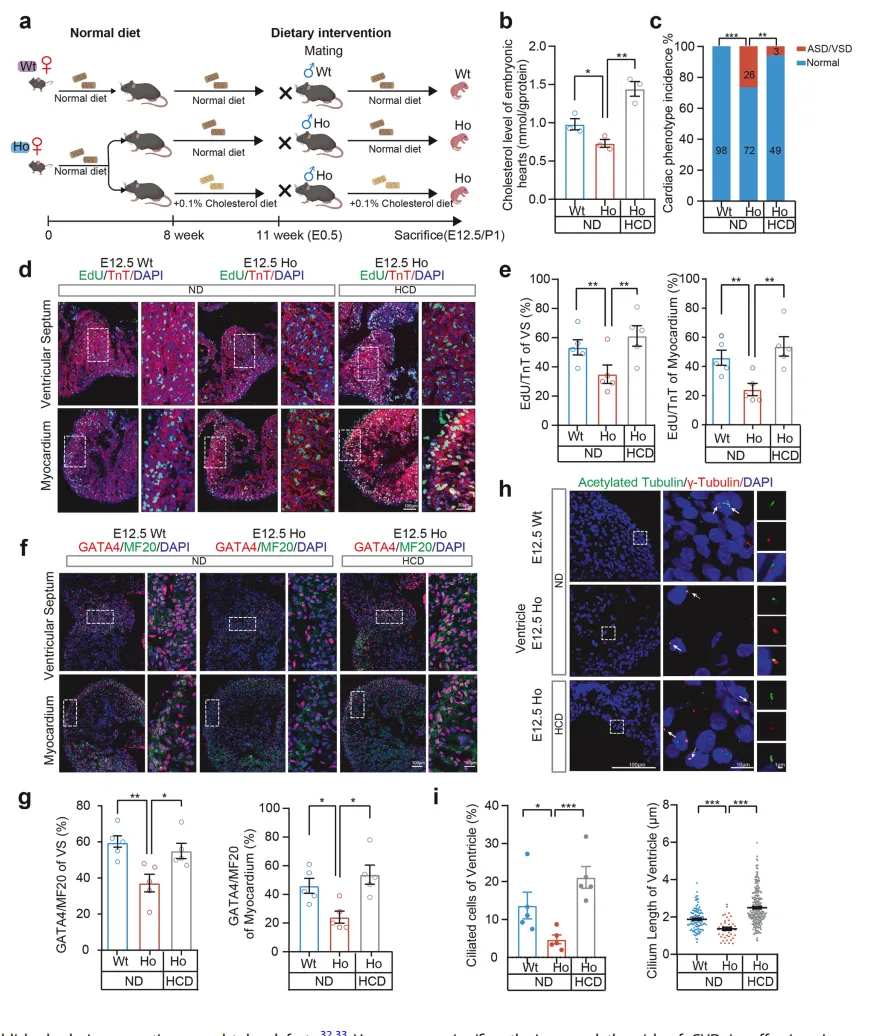 补充5-甲基四氢叶酸不仅恢复了胚胎神经管的叶酸水平【图5B】,还同步提升了神经上皮细胞的增殖活性【图5D, E】、恢复了Pax3和β-catenin的表达【图5F, G】,并修复了肌动蛋白骨架的极性排列【图5H, I】。
补充5-甲基四氢叶酸不仅恢复了胚胎神经管的叶酸水平【图5B】,还同步提升了神经上皮细胞的增殖活性【图5D, E】、恢复了Pax3和β-catenin的表达【图5F, G】,并修复了肌动蛋白骨架的极性排列【图5H, I】。