PNAS | 南京大学魏嘉/湖南大学邢航团队联合开发内溶酶体回收嵌合体平台,可以循环清除PD-L1,重塑肿瘤免疫网络从而增强疗效
- 2026-05-17 19:23:55




【期刊】Proceedings of the National Academy of Sciences of the United States of America
【影响因子】9.1
【doi】10.1073/pnas.2525047123


癌症免疫治疗,尤其是免疫检查点阻断(immune checkpoint blockade,ICB),通过重新激活机体抗肿瘤免疫反应,已经显著改变了多种肿瘤的治疗格局。然而,仍有相当比例患者对ICB治疗无明显获益,提示其疗效受到复杂机制的限制。越来越多研究表明,肿瘤免疫微环境(tumor immune microenvironment,TIME)中的免疫抑制网络是导致免疫治疗耐药的重要原因。
在TIME中,免疫检查点分子的调控并非仅局限于肿瘤细胞。以PD-L1为代表的关键免疫检查点分子,还广泛表达于多种髓系免疫细胞,包括巨噬细胞、中性粒细胞以及树突状细胞(DCs)。这些PD-L1阳性的髓系细胞群体能够主动抑制T细胞活化和效应功能,从而形成多细胞协同的免疫抑制网络,限制抗肿瘤免疫反应。因此,全面理解TIME中的多细胞免疫调控网络并开发能够系统性重塑该网络的治疗策略,对于提升免疫治疗疗效至关重要。
目前已获临床批准的PD-L1单克隆抗体,如阿特珠单抗、度伐利尤单抗和阿维鲁单抗,通过阻断PD-L1与PD-1的结合,在多种癌症治疗中取得了显著进展。然而,传统抗体疗法通常仅通过阻断PD-L1的细胞外表位发挥作用,并不会清除PD-L1蛋白本身。因此,残留的受体支架仍可能参与其他信号交互,且阻断效应往往是短暂和可逆的,从而限制了长期疗效。
近年来,细胞外靶向蛋白降解(extracellular targeted protein degradation,eTPD)逐渐成为一种具有潜力的新策略。该类技术通过招募细胞内内溶酶体降解通路,能够实现膜蛋白或分泌蛋白的不可逆清除。代表性平台包括溶酶体靶向嵌合体(LYTAC)等。这类双特异性分子通常同时结合目标蛋白(如PD-L1、EGFR或IL-4R)和溶酶体运输受体,例如阳离子非依赖性甘露糖-6-磷酸受体(CI-M6PR)。在受体介导下,靶蛋白被内吞进入内体并最终转运至溶酶体降解,从而实现“由外向内”的蛋白质清除机制。与传统ICB疗法相比,eTPD能够彻底移除完整的蛋白结构,从而对信号网络产生更持久的调控作用。
尽管如此,当前eTPD策略仍面临两大关键挑战:第一,大多数PD-L1降解剂主要针对肿瘤细胞,而忽视了TIME中大量表达PD-L1的髓系免疫细胞群体,导致免疫抑制网络仍然存在;第二,许多降解剂在完成一次靶蛋白清除后即被消耗,缺乏多周期降解能力,从而限制了持续的免疫重编程效果。
2026年3月2日,南京大学魏嘉与湖南大学邢航团队在Proceedings of the National Academy of Sciences 在线发表题为“Dynamic reprogramming of the tumor immune network via multicycle checkpoint degradation for cancer immunotherapy” 的研究论文。该研究提出了一种受体介导的内溶酶体循环嵌合体(Receptor-mediated Endolysosomal Recycling Chimera,RECYC)平台,用于实现多周期、持续性的PD-L1降解。
RECYC通过工程化设计,将CI-M6PR靶向适配体与一种具有pH响应特性的PD-L1结合肽相结合。在细胞表面,RECYC首先与PD-L1结合并被CI-M6PR介导内吞进入内体;随后在内体酸性环境中发生解离并被回收至细胞表面,从而能够再次结合新的PD-L1分子,实现循环使用和多轮降解。
在体外共培养体系以及小鼠肿瘤模型中,RECYC能够同时清除肿瘤细胞及肿瘤相关髓系细胞(包括巨噬细胞、中性粒细胞和树突状细胞)表面的PD-L1。这一策略显著削弱TIME中的免疫抑制网络,并促使肿瘤免疫环境由抑制状态转变为免疫激活状态。进一步研究表明,RECYC可增强CD8⁺ T细胞抗肿瘤应答,并逆转免疫抑制性髓系细胞的极化状态。
值得注意的是,在免疫“冷”型和免疫“热”型小鼠肿瘤模型中,RECYC均表现出优于传统PD-L1抗体阻断疗法的抗肿瘤效果。
总体而言,该研究提出了一种能够在TIME中实现多细胞谱系PD-L1清除的多周期降解策略。通过持续诱导PD-L1降解并重塑肿瘤免疫网络,RECYC为突破ICB耐药、实现持久免疫治疗反应提供了新的技术平台和潜在治疗方向。

Results
主要研究结果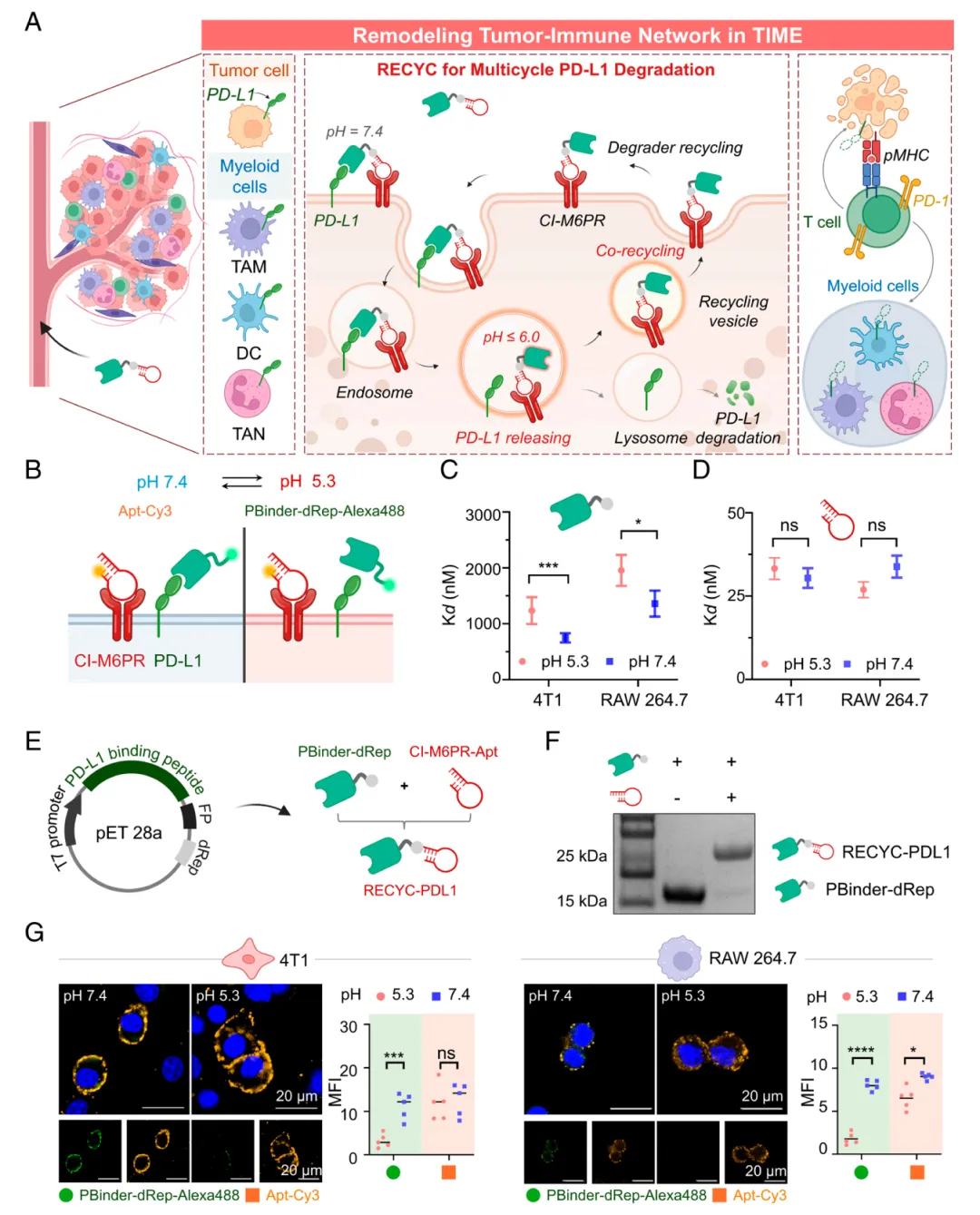
图1. pH响应性 RECYC 设计用于多周期检查点降解。(A) 示意图展示 RECYC 介导的肿瘤和髓系细胞膜PD-L1降解,以及TIME中肿瘤-免疫网络的后续重塑。 RECYC 结合PD-L1和CI-M6PR,经历网格蛋白介导的内吞作用,并通过内体区室转运。pH敏感的PD-L1结合肽在酸性区室中与PD-L1解离,允许PD-L1的溶酶体降解及降解产物与CI-M6PR的循环利用。该过程将PD-L1高表达的TIME转化为PD-L1低表达状态,重塑肿瘤-免疫网络以增强癌症免疫治疗。(B) PBinder-dRep与PD-L1的pH敏感结合示意图,以及CI-M6PR适配体与CI-M6PR的pH稳定结合。(C和D) 通过流式细胞术测量的4°C下pH 7.4和pH 5.3缓冲液中Alexa488标记的PBinder-dRep和Cy3标记的CI-M6PR适配体与4T1和RAW 264.7细胞的平衡解离常数(Kd)。(E) RECYC 合成过程示意图。PBinder-dRep在大肠杆菌中表达,并通过HUH介导的共价1:1连接位点特异性偶联CI-M6PR适配体。(F) 结合前后 RECYC 的SDS-PAGE分析。条带迁移证实了在优化条件下共价偶联。(G) 共聚焦成像显示4T1(左)和RAW 264.7(右)细胞在4°C下与500 nM Alexa488标记的PBinder-dRep和Cy3标记的CI-M6PR适配体孵育1小时后,在不同pH条件下的成像。细胞在37°C条件下用10 μM Vacuolin-1预处理6小时以抑制内吞作用。荧光强度沿图像中箭头所示方向测量。(比例尺:20 μm 。)
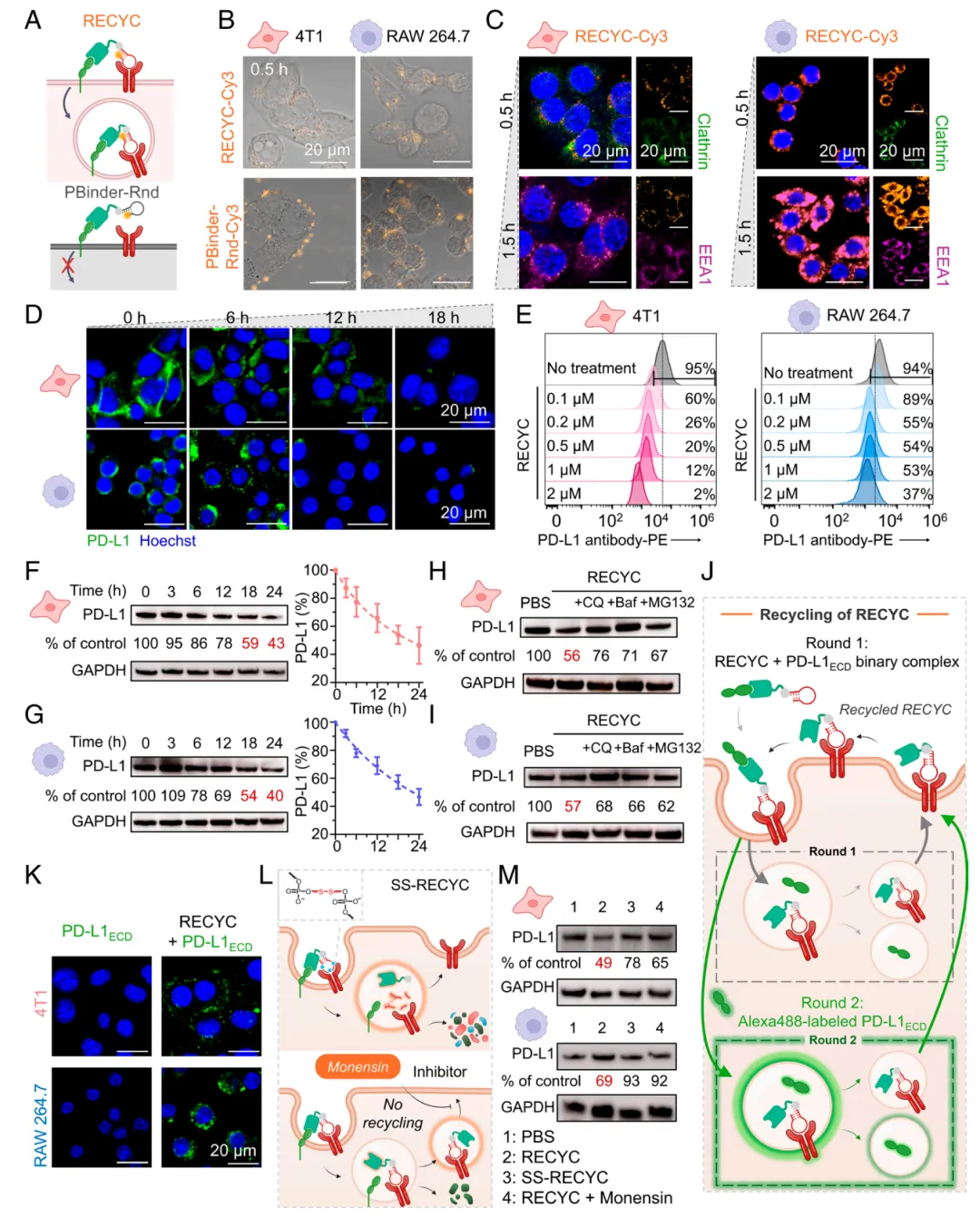
图2. RECYC 促进肿瘤细胞与髓系细胞中膜PD-L1的内化及多循环降解。(A) 内化机制示意图。PBinder-dRep分别与CI-M6PR适配体 RECYC 或乱序DNA对照(PBinder-Rnd)偶联。仅 RECYC 能实现PD-L1与CI-M6PR的双重靶向,促进CI-M6PR介导的内吞作用。(B) 4T1与RAW 264.7细胞经100 nM RECYC -Cy3或PBinderRnd-Cy3在37°C处理0.5小时后的共聚焦图像。(C) RECYC -Cy3(橙色)与网格蛋白(绿色,0.5小时)或EEA 1(洋红色,1.5小时)的共定位分析。细胞核经Hoechst染色。(D) 4T1与RAW 264.7细胞经500 nM RECYC 处理0、6、12或18小时后PD-L1(绿色)与细胞核(蓝色)的共聚焦图像。(E) 4T1与RAW 264.7细胞经不同浓度 RECYC(0至2000 nM)处理18小时后表面PD-L1水平的流式细胞术分析。(F和G) 4T1与RAW 264.7细胞经1 μM RECYC 处理指定时间后总PD-L1表达的蛋白质印迹分析。(H和I) 4T1与RAW 264.7细胞经溶酶体抑制剂(氯喹5 μM ;巴非霉素A1 100 nM)或蛋白酶体抑制剂MG132(5 μM)预处理后,再经1 μM RECYC 处理18小时的总PD-L1表达蛋白质印迹分析。(J) 多循环降解实验示意图。 RECYC 与过量未标记可溶性PD-L1ECD预孵育12小时后洗涤。随后评估了Alexa488标记的PD-L1ECD的细胞摄取情况。(K)共聚焦显微镜图像显示Alexa488标记的可溶性PD-L1ECD在4T1和RAW264.7细胞中的摄取情况,实验组与对照组分别经非荧光 RECYC -PD-L1ECD复合物预孵育。(绿色:Alexa488标记的PD-L1ECD;蓝色:细胞核)。(L)两种单轮降解策略示意图:1)二硫键适配体 RECYC (SS- RECYC );2)莫能菌素预处理抑制CI-M6PR循环。(M) Western印迹分析4T1和RAW 264.7细胞中多轮 RECYC 与单轮SS- RECYC 或莫能菌素处理 RECYC 的总PD-L1降解情况。
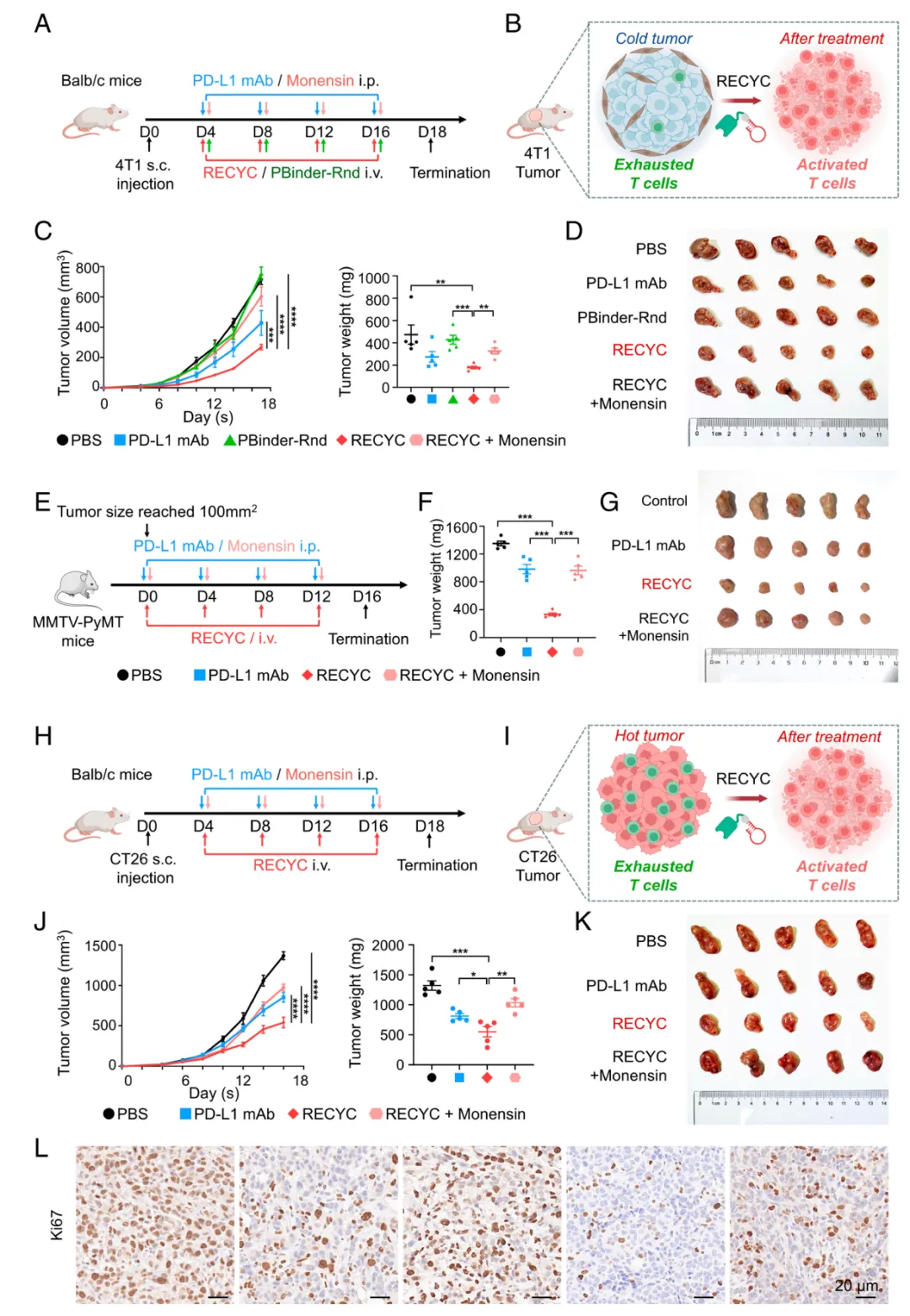
图3. RECYC 在免疫冷型和免疫热型小鼠肿瘤模型中均诱导肿瘤消退。(A) 4T1乳腺癌模型(免疫冷型)示意图:Balb/c小鼠(每组n=5)皮下接种2×10⁵个4T1细胞,并按方案分别腹腔注射PD-L1单克隆抗体(10 mg/kg)、莫能菌素(2 nmol),或静脉注射 RECYC(2 nmol)或PBinder-Rnd(2 nmol)。(B) RECYC 通过增强CD8+ T细胞浸润和活化,将免疫冷型肿瘤(4T1)转化为免疫热型表型的示意图。(C) 不同治疗组小鼠肿瘤体积和重量测量结果(n=5)。(D) (C)组小鼠于第18天处死,获取肿瘤进行进一步分析。(E) MMTV -PyMT乳腺肿瘤模型示意图: FVB 背景MMTVPyMT转基因小鼠(每组n=5)监测自发性乳腺肿瘤发展,当单个肿瘤体积达约100 mm³时启动治疗。随后按计划对小鼠分别注射PD-L1单克隆抗体(10 mg/kg,腹腔注射)、莫能菌素(2 nmol,腹腔注射)或 RECYC(2 nmol,静脉注射)。(F) 不同治疗组小鼠的肿瘤重量测量结果(n=5)。(G) (E)组小鼠于第16天处死,取肿瘤组织进行后续分析。(H) CT26结肠癌模型(免疫热点)示意图:Balb/c小鼠(每组n=5)经皮下接种5×10⁵个CT26细胞后,按(A)所述方法处理。(I) RECYC 治疗后免疫热点肿瘤(CT26)中CD8+ T细胞活化增强的示意图。(J) 不同治疗组小鼠的肿瘤体积与重量测量结果(n=5)。(K) (H)组小鼠于第18天处死,取肿瘤组织进行后续分析。(L) 第18天4T1肿瘤代表性Ki-67 IHC 染色图像(比例尺, 20μm)。
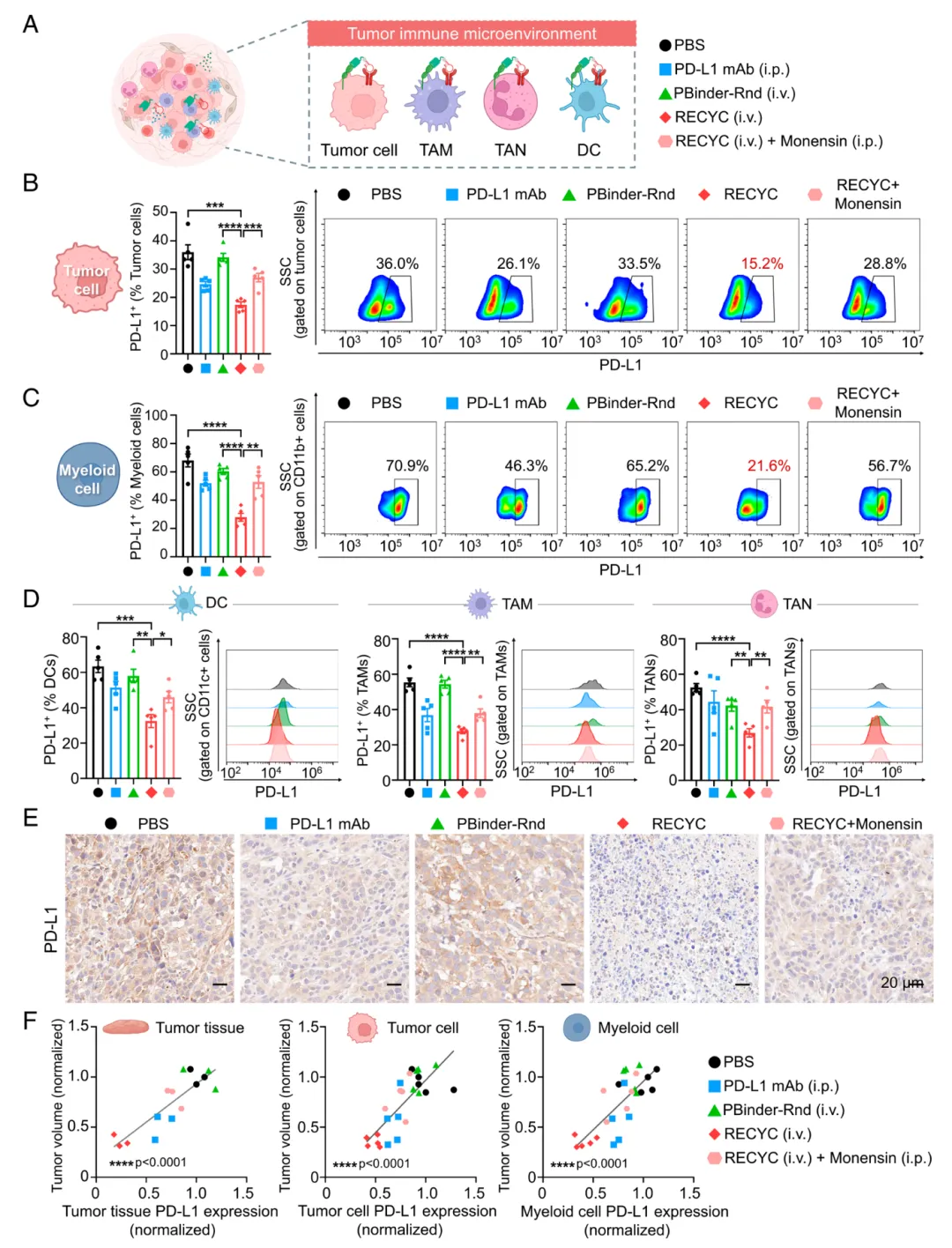
图4. RECYC 显著降低TIME内PD-L1表达。(A)示意图展示 RECYC 介导的PD-L1在4T1肿瘤组织微环境中对肿瘤细胞及肿瘤相关髓系细胞(TAMs、TANs和DCs)的降解作用。(B–D)终点时PD-L1阳性细胞群的流式细胞术分析:(B)肿瘤细胞,(C)总髓系细胞,(D)髓系亚群(DCs、TAMs和TANs)在不同治疗组中的分布(每组n=5)。(E)治疗后4T1肿瘤切片PD-L1的代表性 IHC 染色图像(比例尺:20 μm)。(F)不同组别间肿瘤体积与PD-L1表达水平的相关性分析(每组n=5),数据涵盖全肿瘤组织、肿瘤细胞及髓系细胞。
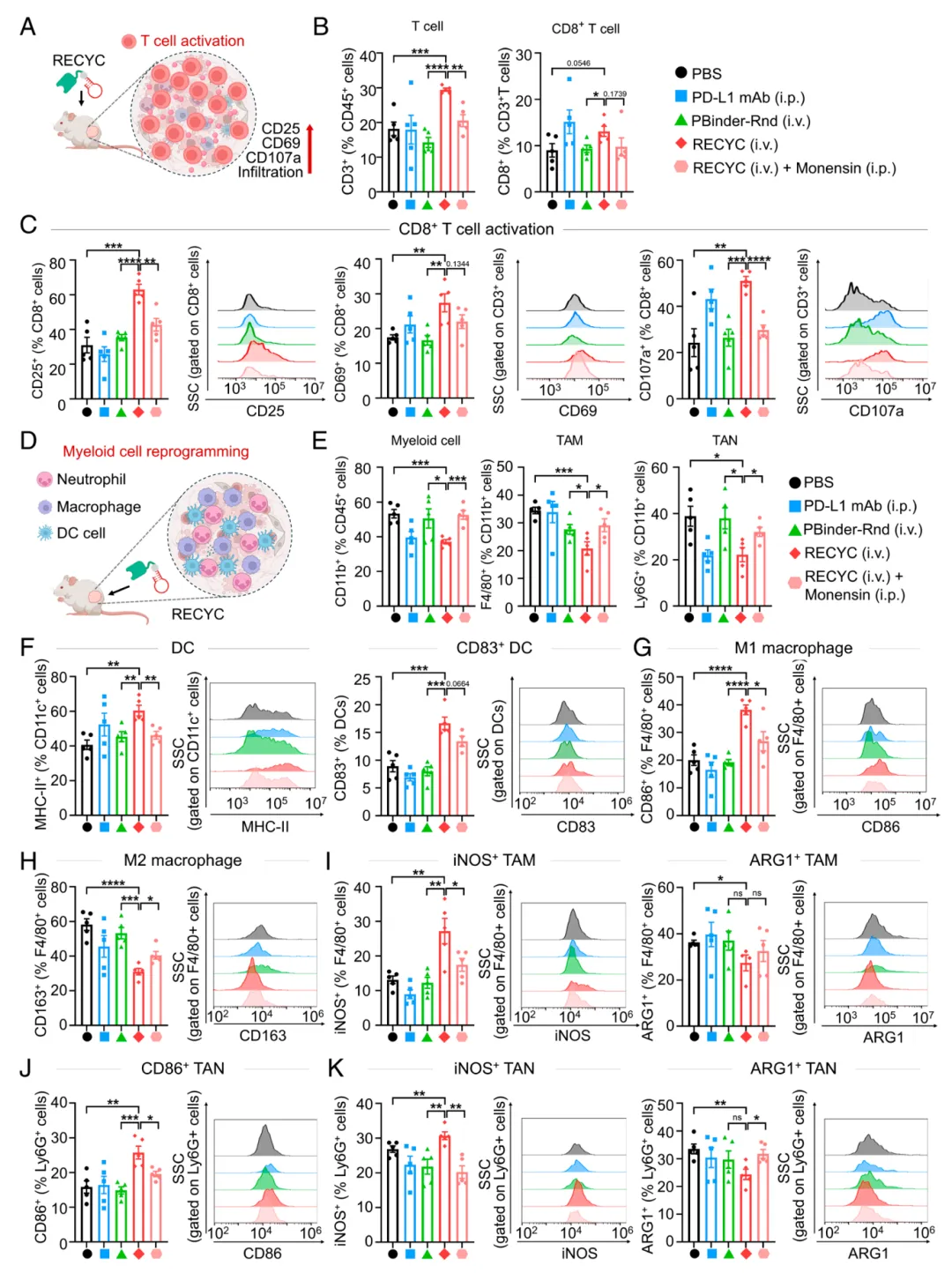
图5. RECYC 增强TIME内适应性与先天性抗肿瘤免疫。(A) 4T1模型中 RECYC 介导的PD-L1在肿瘤细胞及肿瘤相关髓系细胞上的降解示意图,从而增强CD8+ T细胞的适应性应答。(B和C) 4T1小鼠模型终点时肿瘤浸润免疫细胞的流式细胞术分析:(B) T细胞(CD8+/CD45+)与CD8+ T细胞(CD8+/CD45+)比例;(C) CD8+ T细胞的活化标志物(CD25+、CD69+和CD107a+)(每组n=5)。(D) RECYC 介导的PD-L1在肿瘤相关髓系细胞上的降解示意图,逆转4T1 TIME中的髓系诱导免疫抑制。(E) 4T1肿瘤中髓系细胞(CD11b+/CD45+)、肿瘤相关巨噬细胞(TAMs,F4/80+/CD11b+)及肿瘤相关神经元(TANs,Ly6G+/CD11b+)比例的流式细胞术分析(每组n=5)。(F–K) 4T1肿瘤终点时髓系细胞亚群比例的流式细胞术分析:(F) MHCII +/CD11c+与CD83+树突状细胞;(G) CD86+/F4/80+ M1型巨噬细胞;(H) CD163+/F4/80+ M2型巨噬细胞;(I) iNOS+/F4/80+与ARG1+/F4/80+ TAMs;(J) CD86+/Ly6G+ TANs;(K) iNOS+/Ly6G+与ARG1+/Ly6G+ TANs(每组n=5)。
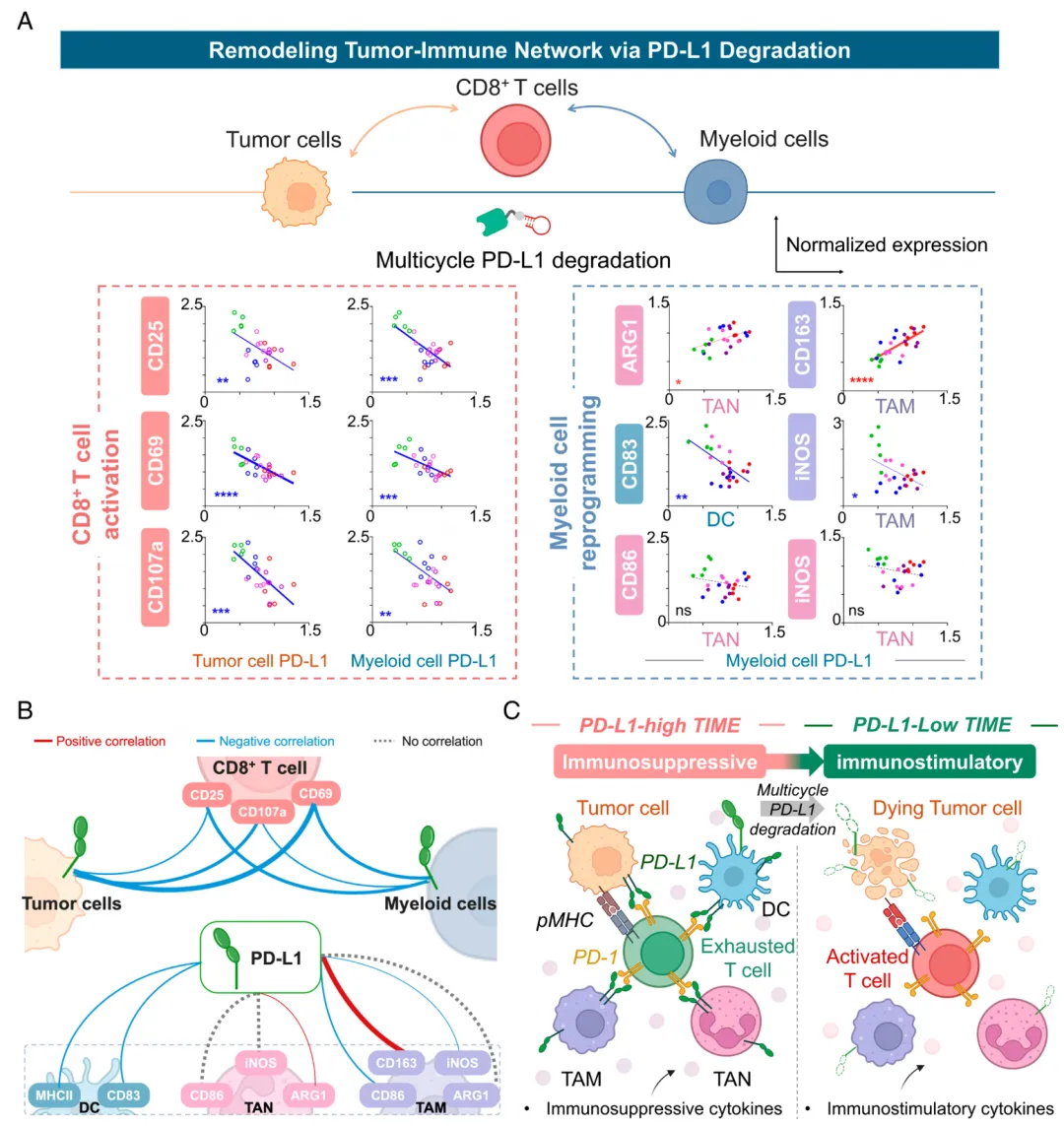
图6. RECYC 重塑TIME内的肿瘤-免疫网络以提升癌症免疫治疗效果。(A和B)相关性分析及细胞间肿瘤-免疫网络图谱显示, RECYC 介导的PD-L1在肿瘤细胞和髓系细胞上的降解与肿瘤体积缩小及免疫细胞表型改变相关。(C)示意图模型展示 RECYC 通过PD-L1在多种细胞类型的多轮降解,将免疫抑制性TIME转化为免疫刺激性TIME。
以上内容均来自期刊官网、Pubmed平台,本公众号仅做整理分享。
投稿邮箱:gyong4926@gmail.com
编辑:思文玥
推荐阅读:
Nature Cancer | 西湖大学高晓飞/浙江省人民医院杨柳/浙江大学梁廷波/冯宇雄团队等开发首款红细胞抗体偶联药物,安全有效治疗晚期癌症
Adv Sci|复旦大学附属眼耳鼻喉科医院陈健/吴海涛团队揭示人源化和电荷优化的CSPG4特异性CAR-T细胞对头颈部鳞状细胞癌显示出增强的疗效
Gut|复旦大学附属中山医院周俭院士和杨欣荣教授团队发表CD177+中性粒细胞能够驱动肝再生最新研究结果

文献PDF请识别下方二维码直接下载
Dynamic reprogramming of the tumor immune network via multicycle checkpoint degradation for cancer immunotherapy.pdf

近期如有需要发表SCI可以咨询,留下您的研究方向,可辅导!!
