ELA抑制TAD进展:本研究首次证实内源性多肽ELA在胸主动脉夹层中发挥关键保护作用。在血管紧张素II诱导和β-氨基丙腈联合血管紧张素II两种经典TAD小鼠模型中,持续泵入ELA多肽均可显著降低夹层相关死亡率【图1D】。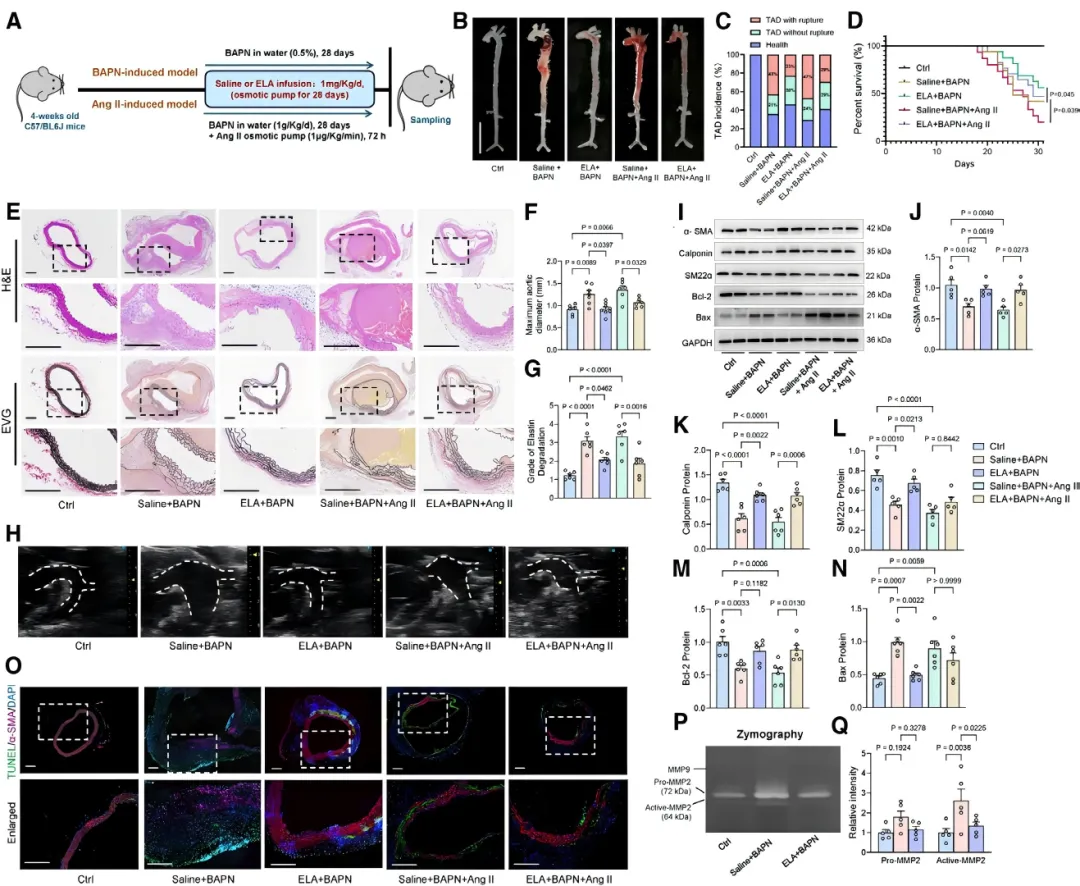 通过主动脉大体形态观察【图1B】、超声动态监测及组织病理学染色【图1E, 1H】分析发现,ELA治疗可显著抑制主动脉扩张,减轻血管中膜弹性纤维的断裂与降解【图1F, 1G】,证实ELA能够有效延缓TAD的病理进程。
通过主动脉大体形态观察【图1B】、超声动态监测及组织病理学染色【图1E, 1H】分析发现,ELA治疗可显著抑制主动脉扩张,减轻血管中膜弹性纤维的断裂与降解【图1F, 1G】,证实ELA能够有效延缓TAD的病理进程。
胸主动脉夹层的核心病理机制在于血管平滑肌细胞(VSMC)的稳态失调。本研究证实,ELA输注可显著上调TAD小鼠主动脉中收缩型VSMC标志蛋白的表达【图1I-1L】,同时有效抑制细胞凋亡【图1M-1O】,从而恢复VSMC的正常功能表型。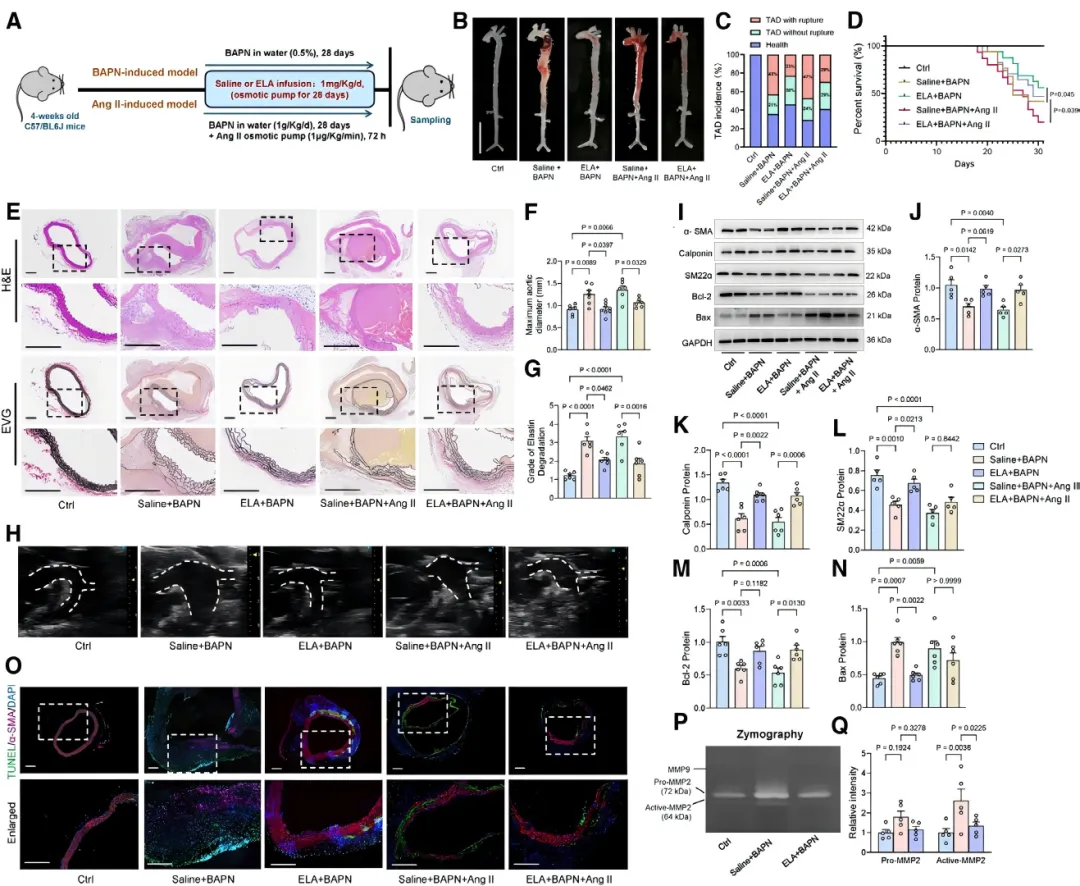 与此同时,ELA还能够显著抑制基质金属蛋白酶的异常活化【图1P, 1Q】,减少细胞外基质的过度降解,从而有效维护主动脉壁的结构完整性。
与此同时,ELA还能够显著抑制基质金属蛋白酶的异常活化【图1P, 1Q】,减少细胞外基质的过度降解,从而有效维护主动脉壁的结构完整性。
为验证ELA对血管平滑肌细胞的直接调控作用,研究者使用血小板衍生生长因子处理人主动脉VSMC。结果显示,PDGF刺激后,细胞内源性ELA的表达水平显著下调【图2A-2C】。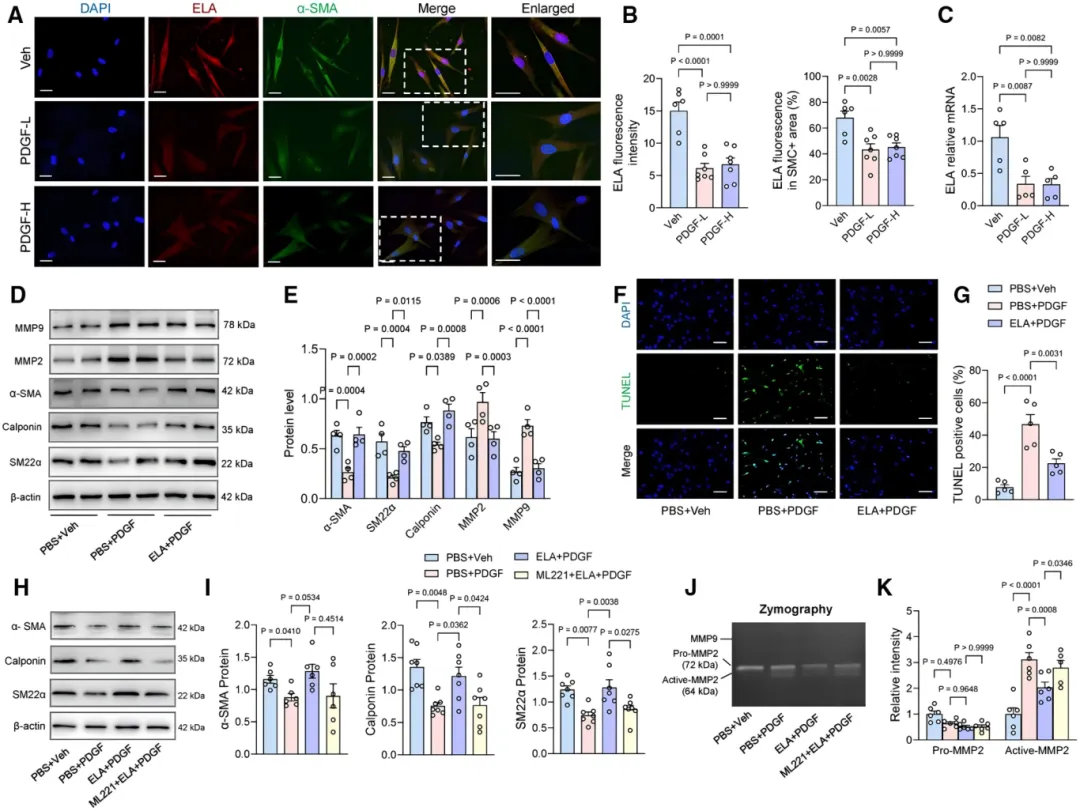 补充外源性ELA可显著逆转VSMC由收缩表型向合成表型的恶性转换【图2D】,并有效抑制高浓度PDGF诱导的细胞凋亡【图2F, 2G】。上述保护效应可被APJ受体拮抗剂ML221完全阻断【图2H-2K】,证实ELA通过其同源受体APJ发挥维持VSMC稳态的关键功能。
补充外源性ELA可显著逆转VSMC由收缩表型向合成表型的恶性转换【图2D】,并有效抑制高浓度PDGF诱导的细胞凋亡【图2F, 2G】。上述保护效应可被APJ受体拮抗剂ML221完全阻断【图2H-2K】,证实ELA通过其同源受体APJ发挥维持VSMC稳态的关键功能。
为在体内水平进一步验证APJ受体是否介导ELA的保护效应,研究者对TAD小鼠给予ELA输注的同时,联合使用APJ拮抗剂ML221进行干预。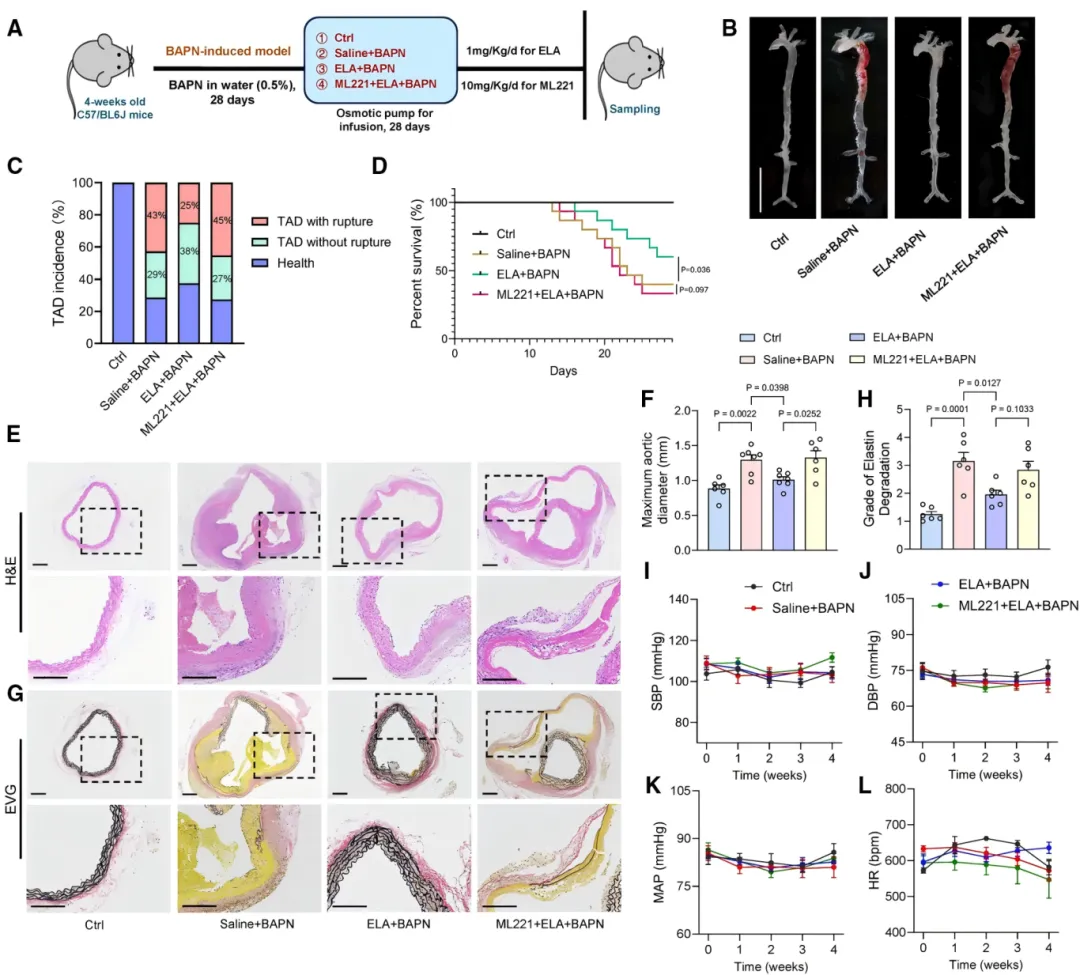 结果显示,ML221几乎完全抵消了ELA带来的生存获益【图3D】及其抑制主动脉扩张的保护作用【图3E, 3F】。各组小鼠的血压与心率水平均无显著差异【图3I-3L】,表明ELA是直接作用于血管壁发挥保护效应,而非通过影响血流动力学间接起效。
结果显示,ML221几乎完全抵消了ELA带来的生存获益【图3D】及其抑制主动脉扩张的保护作用【图3E, 3F】。各组小鼠的血压与心率水平均无显著差异【图3I-3L】,表明ELA是直接作用于血管壁发挥保护效应,而非通过影响血流动力学间接起效。
主动脉转录组测序分析显示,ELA输注可显著下调NOD样受体信号通路及中性粒细胞胞外陷阱形成相关基因的表达水平【图4C, 4D】。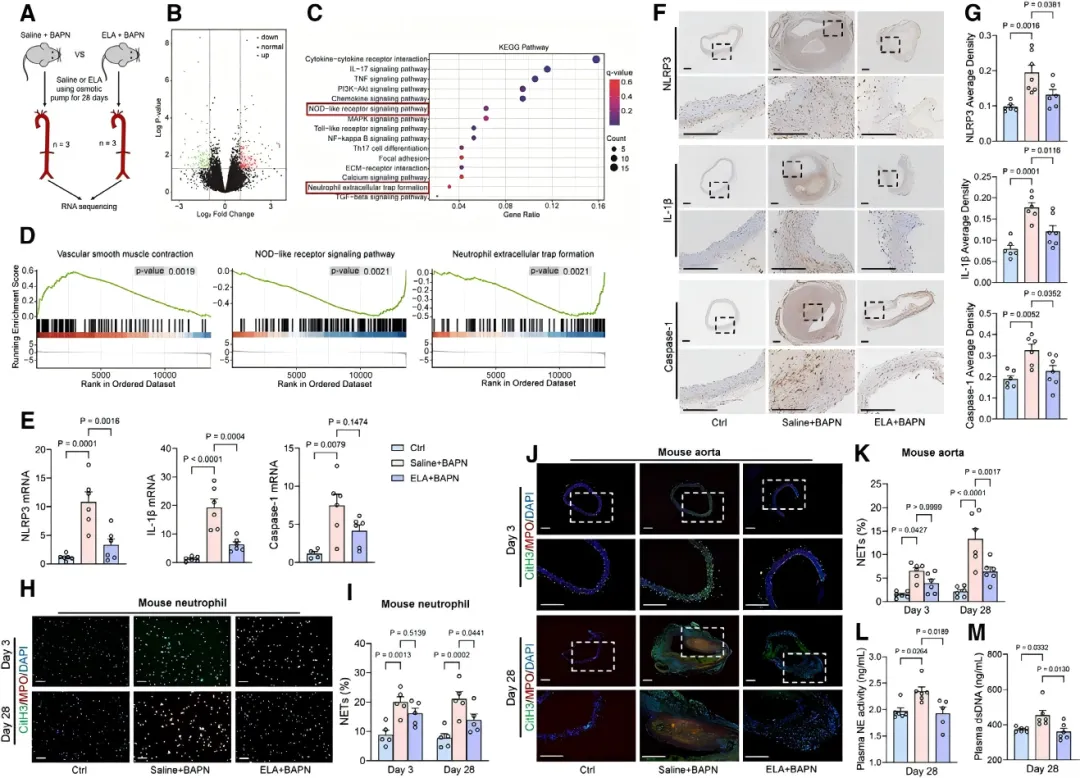 进一步的实验验证表明,ELA能够显著抑制主动脉组织中NLRP3炎症小体及其下游效应分子IL-1β的激活【图4E-4G】,同时有效降低循环中中性粒细胞胞外陷阱标志物的水平【图4H-4M】,提示ELA通过抗炎和调控NETs双重途径发挥血管保护作用。
进一步的实验验证表明,ELA能够显著抑制主动脉组织中NLRP3炎症小体及其下游效应分子IL-1β的激活【图4E-4G】,同时有效降低循环中中性粒细胞胞外陷阱标志物的水平【图4H-4M】,提示ELA通过抗炎和调控NETs双重途径发挥血管保护作用。
机制层面,研究者揭示了一个双向调控环路。一方面,ELA可直接作用于中性粒细胞,通过抑制NOX2介导的活性氧生成,有效阻断NETs的形成【图5C-5G】。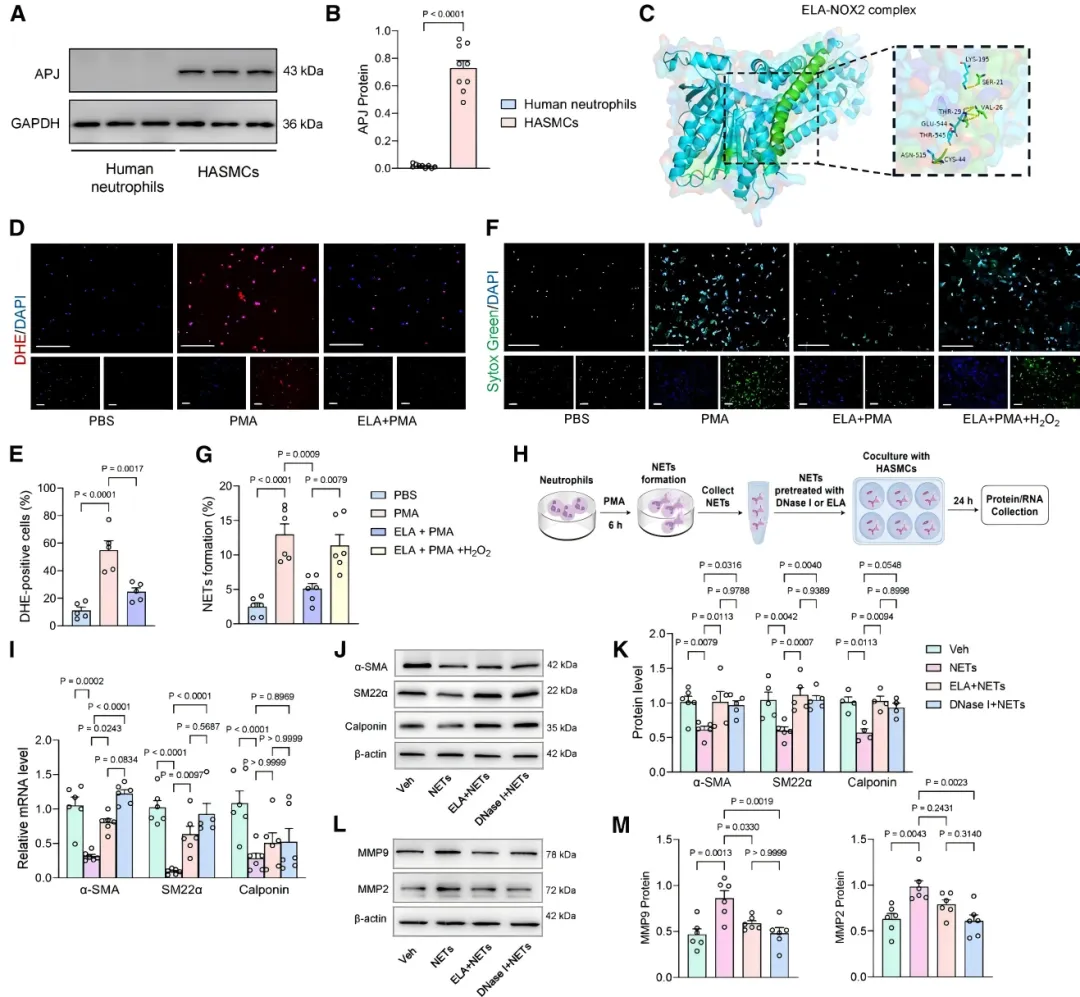 另一方面,在血管平滑肌细胞中,ELA通过结合APJ受体激活AMPK信号通路,抑制PDGF诱导的NLRP3炎症小体活化及IL-1β分泌【图6A-6C, 6P, 6Q】,从而减少由VSMC来源的IL-1β所触发的NETosis【图6E, 6G】。
另一方面,在血管平滑肌细胞中,ELA通过结合APJ受体激活AMPK信号通路,抑制PDGF诱导的NLRP3炎症小体活化及IL-1β分泌【图6A-6C, 6P, 6Q】,从而减少由VSMC来源的IL-1β所触发的NETosis【图6E, 6G】。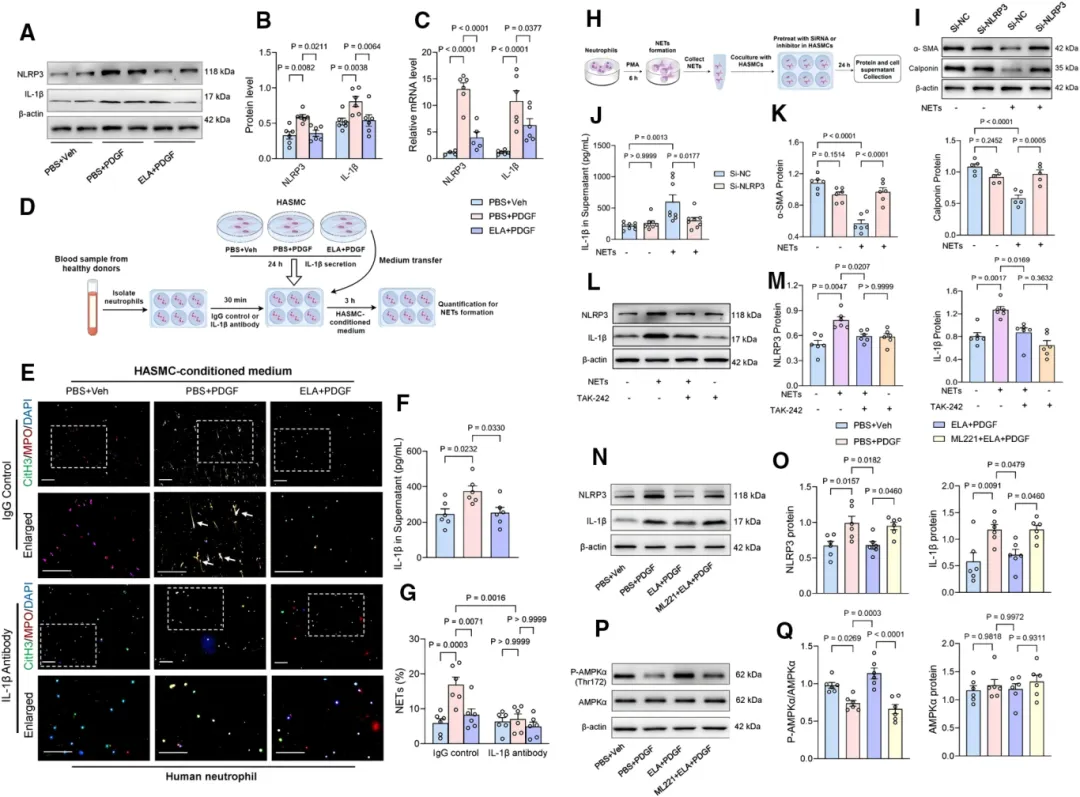
值得注意的是,NETs一旦形成,又会反向作用于血管平滑肌细胞,形成恶性循环。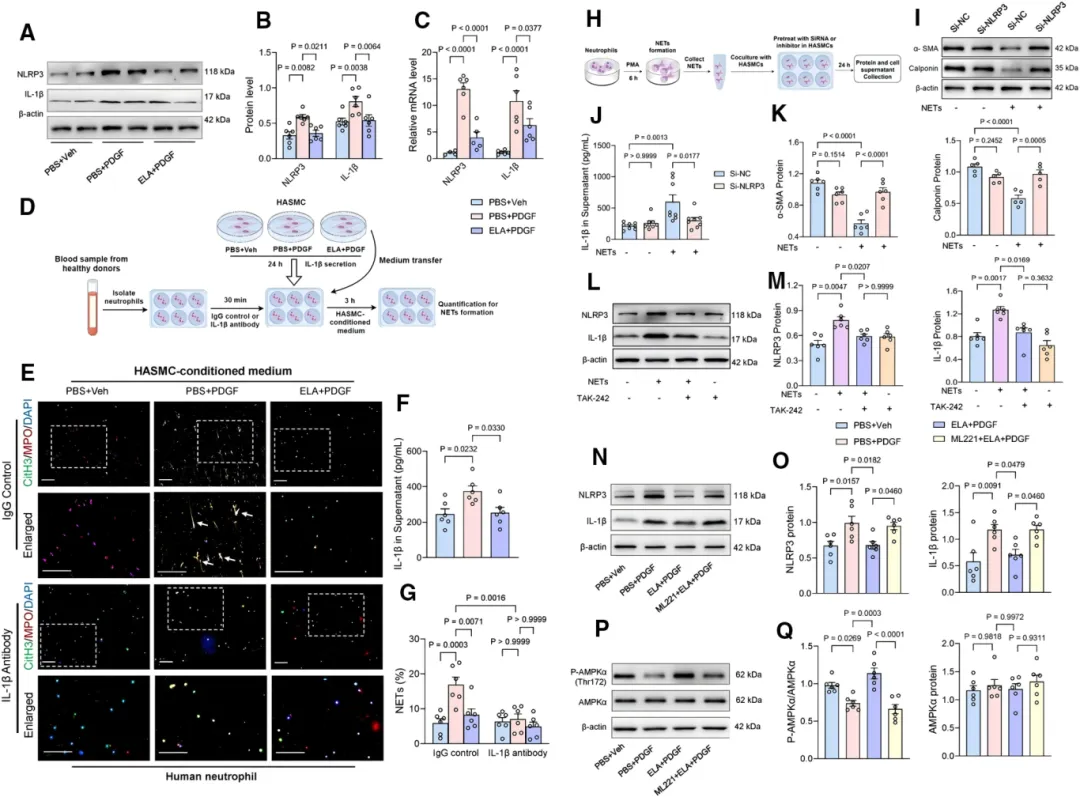 研究发现,NETs可激活VSMC表面的TLR4受体,触发NLRP3炎症小体活化【图6L, 6M】,进而诱导VSMC发生表型转换【图6I-6K】,形成NETs→炎症→VSMC失调→更多炎症的正反馈恶性循环。而ELA能够同时作用于这一循环的两端——既抑制中性粒细胞NETs形成,又保护VSMC免受炎症损伤,从而有效阻断TAD的进展。
研究发现,NETs可激活VSMC表面的TLR4受体,触发NLRP3炎症小体活化【图6L, 6M】,进而诱导VSMC发生表型转换【图6I-6K】,形成NETs→炎症→VSMC失调→更多炎症的正反馈恶性循环。而ELA能够同时作用于这一循环的两端——既抑制中性粒细胞NETs形成,又保护VSMC免受炎症损伤,从而有效阻断TAD的进展。
最后,研究团队在临床样本中验证了上述发现的转化价值。与健康对照组相比,TAD患者主动脉组织中的ELA及其受体APJ表达水平均显著下调【图7A-7D】,同时血浆ELA浓度明显降低而NETs标志物水平显著升高【图7E-7G】,进一步支持ELA作为TAD生物标志物和治疗靶点的临床潜力。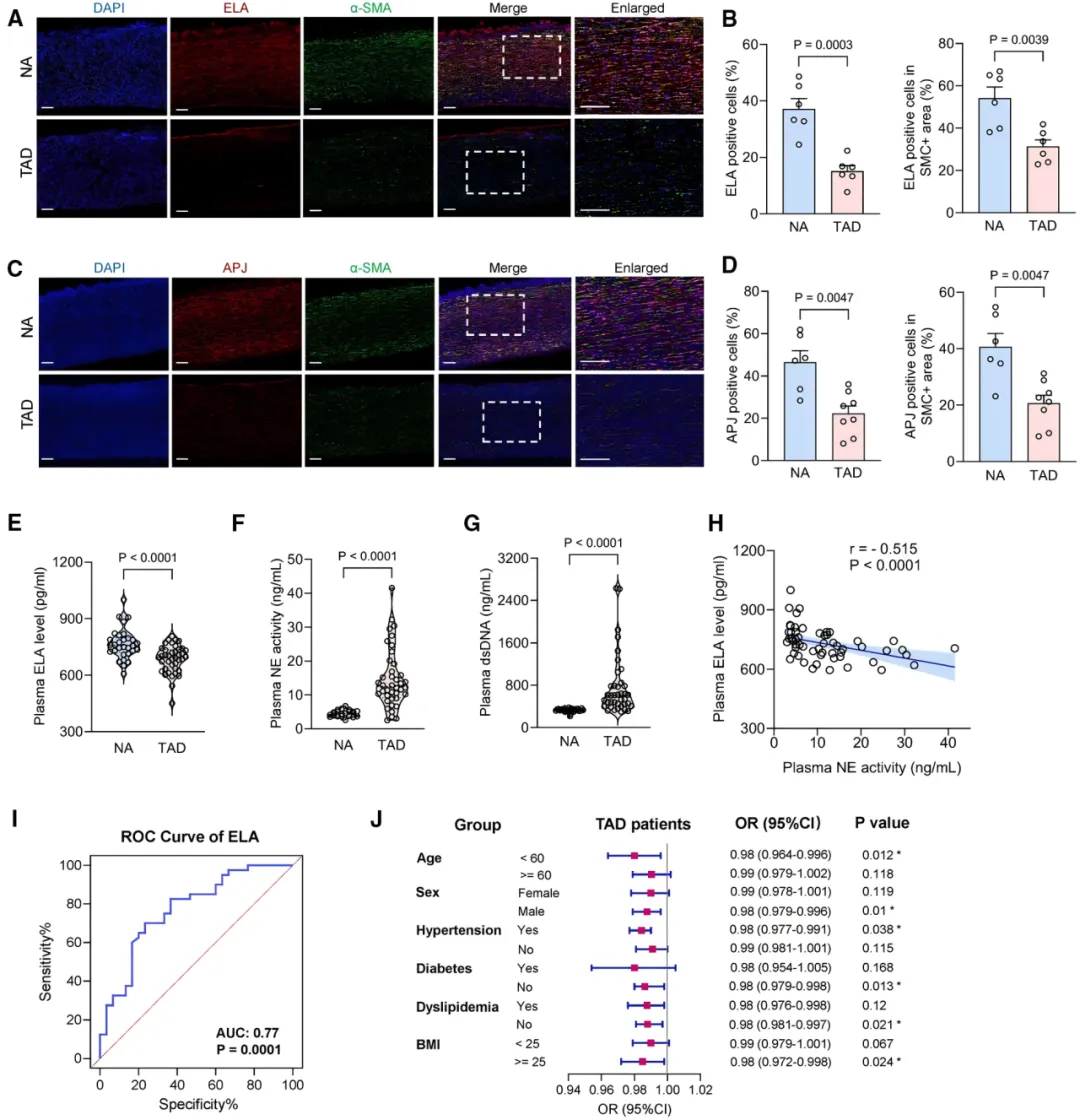 相关性分析显示,血浆ELA水平与NETs标志物呈显著负相关【图7H】。低血浆ELA对TAD具有潜在的诊断价值【图7I】,且与更高的患病风险密切相关【图7J】,提示ELA有望成为TAD早期筛查、风险分层和临床管理的新型生物标志物。
相关性分析显示,血浆ELA水平与NETs标志物呈显著负相关【图7H】。低血浆ELA对TAD具有潜在的诊断价值【图7I】,且与更高的患病风险密切相关【图7J】,提示ELA有望成为TAD早期筛查、风险分层和临床管理的新型生物标志物。