摘要概括
该研究报道了一种新型人工光酶催化体系,成功实现了高对映选择性的[2π+2σ]环加成反应,用于合成具有重要价值的手性Bicyclo[2.1.1]己烷 (BCHs) 骨架。该体系的核心是研究者理性设计的光活性辅因子MeO-BpAD(一种NAD+类似物)与工程化的Rr12aHSDH-M4 突变体蛋白的结合。在400 nm光照下,该人工光酶可高效催化喹啉-2(1H)-酮与单取代双环[1.1.0]丁烷之间的环加成反应,以中等到优异的产率(最高达88%)和高达94%的对映选择性(ee)得到目标产物。该策略通过调节辅因子的光物理性质抑制了背景反应,并利用蛋白质骨架提供的精确手性环境实现了出色的立体控制,为传统方法难以实现的挑战性转化提供了新思路。
研究背景
Bicyclo[2.1.1]己烷 (BCHs) 是邻位/间位取代苯环的重要三维生物电子等排体,在药物化学中具有巨大潜力,可改善代谢稳定性并引入多个立体中心,从而优化药理学性质。然而,尽管外消旋BCH的合成方法发展迅速,高效、通用的不对称合成策略仍然有限。现有方法主要依赖手性路易斯酸/布朗斯特酸、过渡金属或有机光催化剂,但通常对底物(尤其是单取代底物)的普适性和立体选择性控制存在挑战。
与此同时,人工酶和光酶催化领域的发展为结合合成化学的反应多样性与生物催化的精确立体控制提供了可能。研究者所在课题组前期开发了光活性辅因子BpAD,可将NAD+依赖的蛋白重编程为人工光酶。在此基础之上,本研究旨在开发一个通用平台,实现此前具有挑战性的对映选择性[2π+2σ]环加成来构建手性BCHs。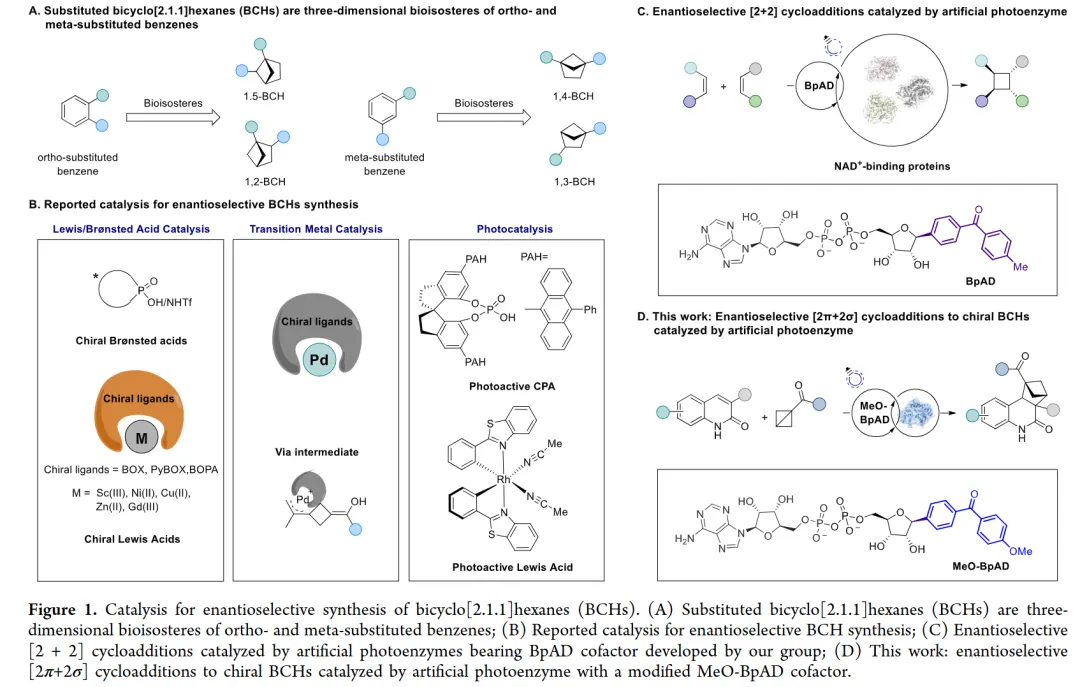
研究问题
如何开发一种通用、高效且高立体选择性的催化方法,用于合成手性BCHs,特别是能够兼容在药物发现中更具吸引力但反应难度更大的单取代双环[1.1.0]丁烷底物,并克服在光反应条件下显著的背景非对映反应问题?
研究方案
辅因子设计与优化:为解决背景反应问题,研究者对前期开发的BpAD辅因子进行结构修饰,引入了甲氧基,得到了MeO-BpAD。该修饰使其吸收光谱发生红移,可在400 nm波长下被选择性激发,从而有效抑制了底物在365 nm光下的直接活化与背景反应。
人工光酶组装与筛选:将MeO-BpAD与一系列野生型及工程化的NAD+依赖型酮还原酶结合,筛选最佳催化组合。最终发现,与Rr12aHSDH-M3突变体(及其进一步优化的M4突变体,含A92Q突变)结合时,催化性能最佳。
反应条件优化:对光照波长、缓冲液、pH、共溶剂、底物当量和催化剂负载量等条件进行系统优化,确定了最优反应条件:400 nm光照,PBS缓冲液,Rr12aHSDH-M4 (2.5 mol%) 与 MeO-BpAD (2.5 mol%),氮气氛围,4°C。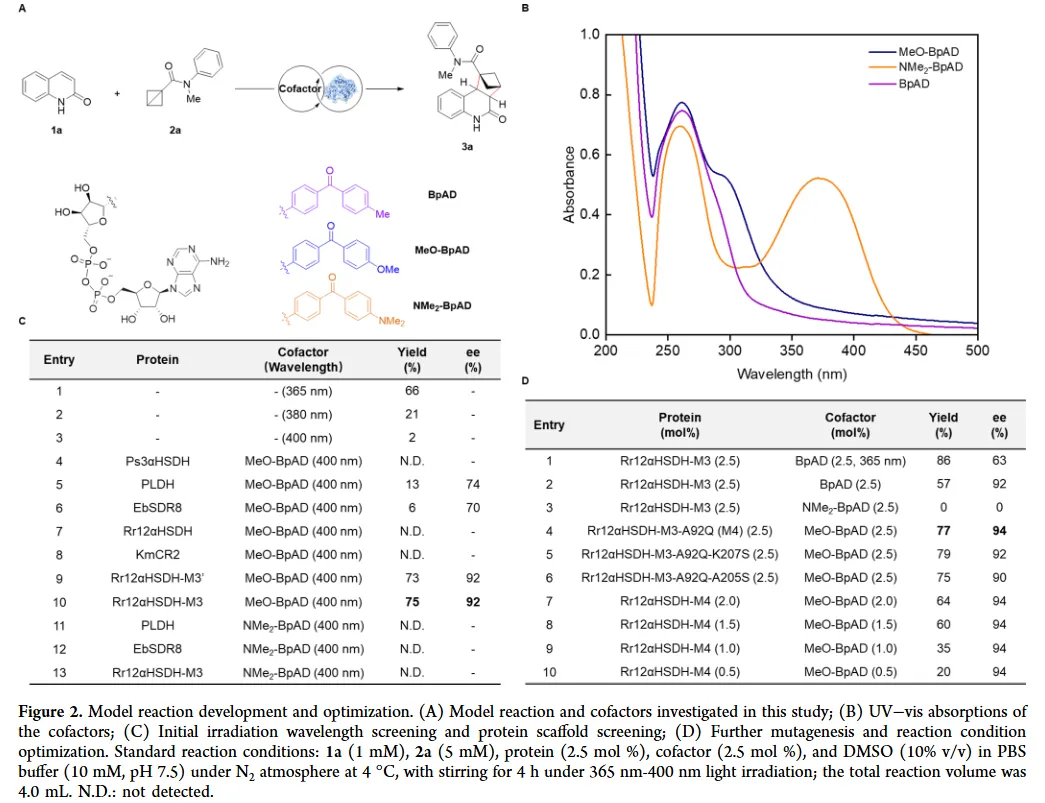
底物普适性考察:在最优条件下,广泛考察了单取代双环[1.1.0]丁烷(带有酰胺、酯、酰基等不同取代基)和一系列喹啉-2(1H)-酮衍生物的适用性。结果表明,BCB底物适用范围较广,能普遍以高产率和高对映选择性得到产物;而喹啉酮骨架上取代基的位阻和电子效应对反应活性影响显著。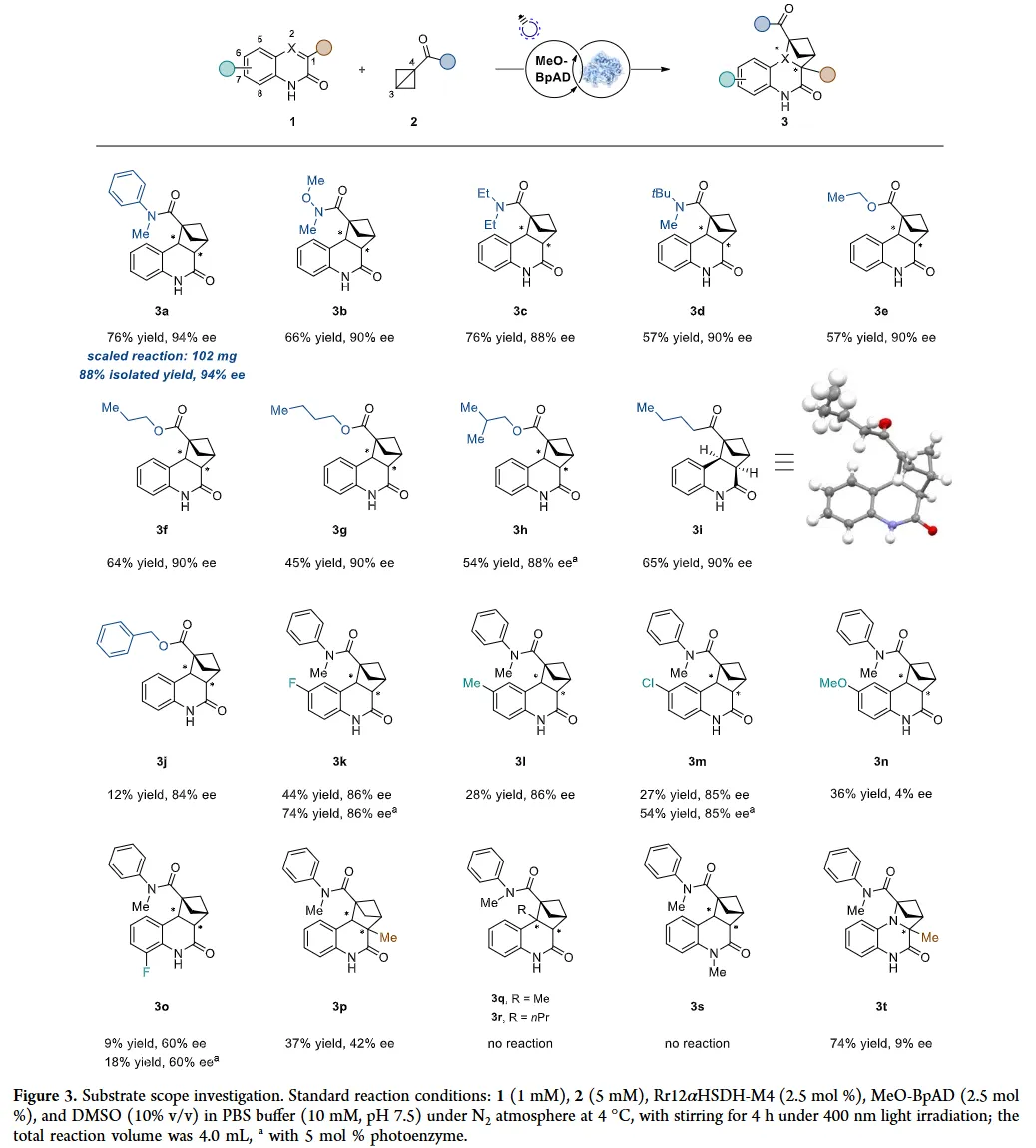
机理研究:通过**等温滴定量热法(ITC)** 证实MeO-BpAD与蛋白质骨架结合良好(结合常数Kd ~2 μM)。瞬态吸收光谱显示蛋白质环境将MeO-BpAD激发态寿命延长了约100倍,显著稳定了三重态。这些实验为光酶的高效性提供了物理化学基础。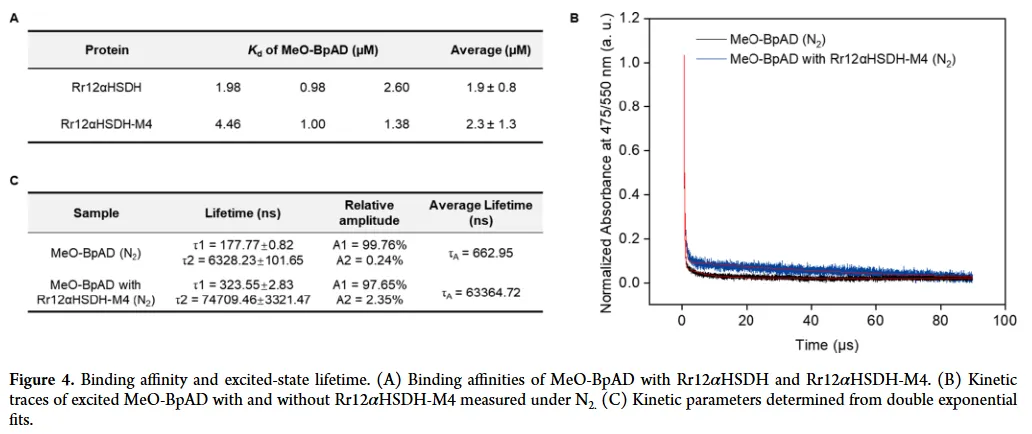
结合分子动力学模拟(MD) 和QM/MM计算,揭示了反应通过能量转移和激基复合物中间体进行,并阐明了立体选择性来源于活性口袋内特定的非共价相互作用(如π-π堆积、静电作用)。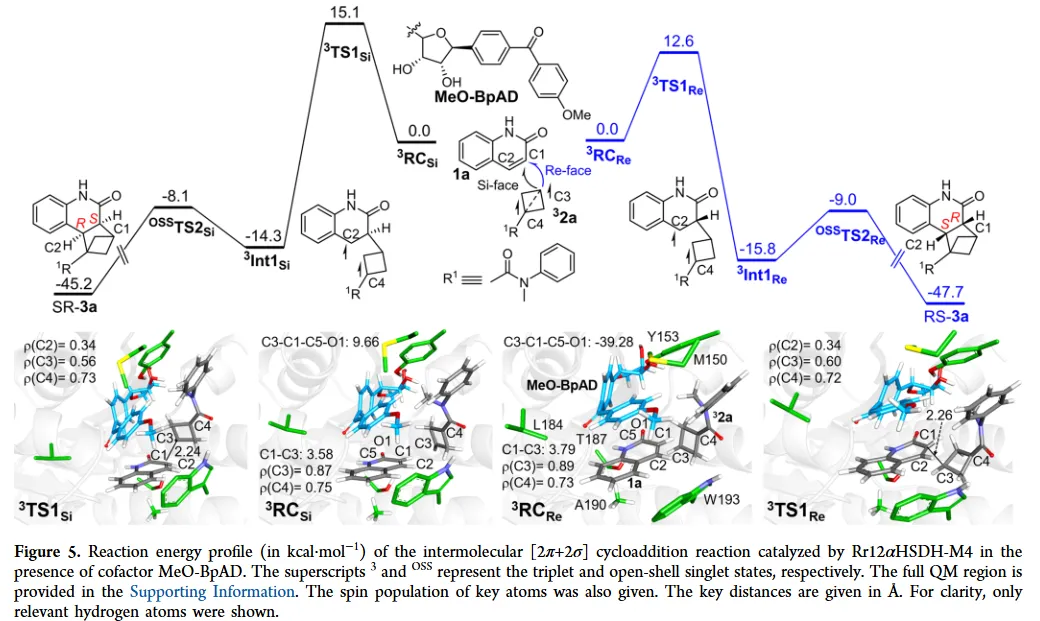
研究结论与创新点
本研究成功建立了一种基于人工光酶的不对称BCH合成通用策略,其创新性主要体现在:
辅因子工程策略:通过理性设计MeO-BpAD辅因子,调节其光物理性质(红移吸收),实现了在特定波长(400 nm)下的高效激发,同时最大限度地抑制了非手性的背景反应,这是实现高手性诱导的关键前提。
平台通用性:该策略基于NAD+类似物辅因子,理论上可与大量已知的NAD(P)+结合蛋白结合,从而快速构建多样化的光酶库,用于开发其他挑战性转化,展示了“即插即用”型人工光酶平台的潜力。
优异的催化性能:该人工光酶系统在温和条件下,实现了对单取代BCBs的高对映选择性转化,产率中等到优秀,对映选择性高达94%,并具有良好的可放大性(0.34 mmol规模)。
深入的机理阐释:研究不仅展示了合成应用,还通过光物理、MD模拟和QM/MM计算等多维度手段,从分子层面阐明了蛋白质骨架在稳定辅因子激发态、控制底物结合构象以及通过非共价相互作用实现立体控制中的关键作用,为后续理性设计提供了坚实依据。
总之,这项工作通过巧妙的辅因子设计与蛋白质工程相结合,将天然酶的精密结合口袋与合成光敏剂的强大功能融合,为解决传统小分子催化难以实现的高选择性转化提供了创新方案。
点击下载文献
enantioselective-2π-2σ-cycloaddition-to-bicyclo-2-1-1-hexanes-enabled-by-an-artificial-photoenzyme.pdf