最新!南京工业大学院士团队Bioresour Technol-合成生物-构建支架介导的法夫驹形氏酵母双酶展示系统及固定化细胞在连续生物催化中的应用
- 2026-04-16 04:08:19
(点击页面左下角阅读原文,直达文献页面)
一、中文标题
构建基于支架介导的法夫驹形氏酵母双酶展示系统及其固定化细胞在连续生物催化中的应用(Construction of a scaffold-mediated dual-enzyme display system in Komagataella phaffii with immobilized cells for continuous biocatalysis)
二、发表单位及通讯作者
发表单位:南京工业大学生物与制药工程学院
通讯作者:Huanqing Niu、Yong Chen
三、科学问题
如何在 法夫驹形氏酵母表面构建基于 TRAP 支架的高效、稳定、可重复使用的双酶共展示系统,以实现连续生物催化并克服传统多酶体系中酶分散、传质受限等问题?
四、发表时间
时间:2026年4月
链接:
https://www.sciencedirect.com/science/article/pii/S0960852426006085

五、摘要
本研究首次在法夫驹形氏酵母细胞表面构建了基于四肽重复亲和蛋白(TRAP)支架的双酶展示系统,用于连续生物催化。通过优化连接肽和细胞壁工程,将展示效率提升至92.1%。成功共展示了木聚糖酶(Xyn)和β-木糖苷酶(Hixyl43A),与游离酶相比,细胞表面展示酶具有更优的热稳定性和pH稳定性。在木聚糖降解中,双酶展示细胞表现出显著的协同作用。进一步通过生物膜固定化将双酶展示细胞共固定于载体上,显著提高了操作稳定性和重复使用性,在15个循环后仍保留87.2%的相对酶活性。该研究为多酶协同催化提供了高效的空间组织策略,并为绿色生物制造中的连续催化过程提供了技术支持。
六、研究背景
多酶催化系统在药物合成、能源生产和精细化学品制造中具有重要应用价值。然而,传统的游离酶系统由于酶分子随机分布、中间产物依赖扩散传递,导致催化效率低、中间产物积累易引起反馈抑制或副反应,限制了其工业化应用。为解决这些问题,研究者开发了基于蛋白支架的酵母表面展示技术,通过将酶分子有序组装在细胞表面,增强酶-酶邻近效应和底物通道效应,提高级联反应效率。
目前已发展的支架系统主要包括源自纤维小体的Cohesin-Dockerin系统和SpyCatcher/SpyTag系统。然而,这些系统存在支架分子尺寸大、结合效率低、非天然环境下稳定性差、组装精度不高等问题,制约了其工业应用。因此,开发新型高效、灵活、稳定的蛋白支架系统具有重要意义。
近年来,工程化四肽重复亲和蛋白(TRAP)因其优异的正交结合特异性、较小的结合肽段、良好的可设计性和多功能性,在体外多酶组装中展现出潜力。然而,TRAP尚未被用于细胞表面酶展示系统。同时,Komagataella phaffii(原名毕赤酵母)作为一种工业上重要的表达宿主,具有蛋白分泌少、翻译后修饰正确、高密度发酵能力强等优点,是表面展示和连续催化的理想底盘。
基于此,本研究首次将TRAP支架引入K. phaffii细胞表面,建立了一套集TRAP介导的多酶共展示、细胞壁工程优化、生物膜固定化于一体的连续催化平台,并以木聚糖降解为模型,系统验证其催化性能、稳定性和重复使用性,为多酶协同催化和绿色生物制造提供新策略。
七、研究结果
结果1、TRAP支架在K. phaffii表面的构建与验证
研究首先构建了TRAP支架展示菌株TPS,将含有三个TPR重复单元(TRAP1-3)、刚性连接肽PAPAP和细胞壁锚定蛋白SED1p的融合蛋白表达于K. phaffii表面。免疫荧光和流式细胞术证实TRAP支架成功锚定在细胞表面,但展示效率仅为32.2%,存在明显异质性。进一步通过体外自组装实验,将E. coli表达的GFP-M1和GFP-M3与TPS菌株孵育,流式细胞术显示细胞荧光显著增强,证明TRAP支架能有效捕获带特异性肽标签的蛋白。同时,在单一宿主中构建TPS-GFP和TPS-mruby2菌株,共聚焦显微镜观察到绿色和红色荧光分布于细胞表面,上清中游离荧光蛋白量远高于锚定量,提示展示效率仍有提升空间。
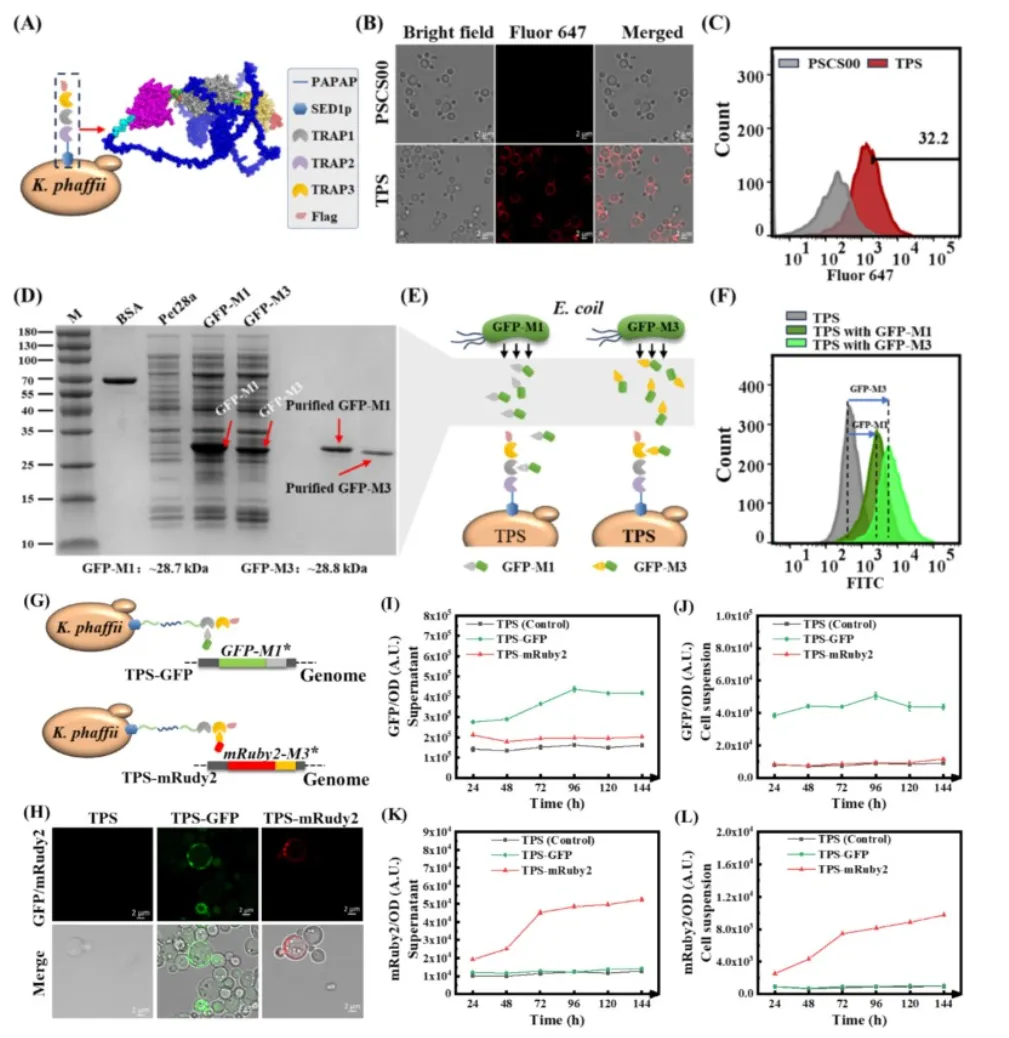
图1 支架构建和验证
结果2、不同连接肽对TRAP支架展示效率的影响
为提升展示效率,设计了不同长度和类型的连接肽。结果表明,柔性连接肽(GGGGS)n显著提高展示效率,其中(GGGGS)3(菌株TG3S)达到40.1%;而刚性连接肽(EAAAK)n效果较差。混合连接肽GGGGSEAAAAGGGGGS(菌株TGEGS)表现最佳,展示效率达48.3%,平均荧光强度较原始TPS提高73.7%。这说明柔性-刚性组合连接肽能优化蛋白折叠和空间取向,提升锚定效率。
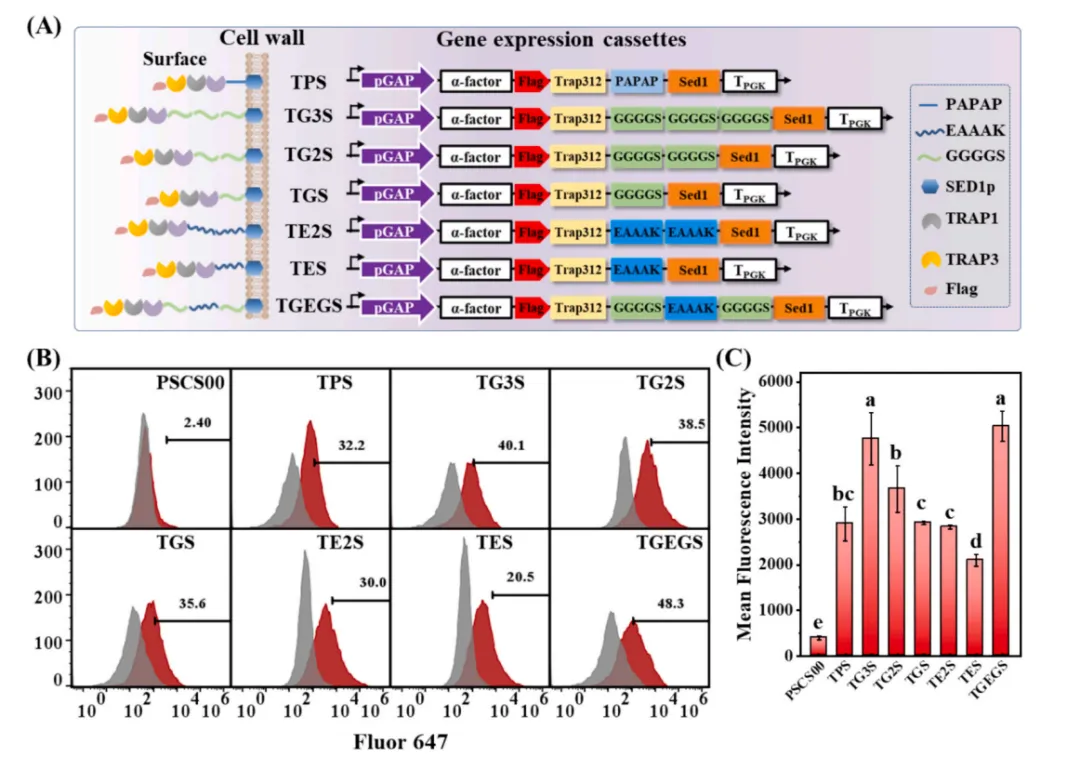
图2 连接肽的影响
结果3、细胞壁工程对TRAP支架展示效率的影响
为提供更多锚定位点,系统敲除了与细胞壁多糖合成及GPI锚定蛋白相关的基因(GCW12、GCW21、GCW61、mnn2、PAS_chr1-3_0225、PAS_chr1-3_0226)。结果显示,除TGEGSΔ0226外,其余敲除菌株生长正常。流式分析表明,所有敲除菌株的展示效率均显著提升,其中TGEGSΔGCW21达到最高92.1%。细胞壁敏感性实验证实,敲除这些基因改变了细胞壁组成(如几丁质、甘露聚糖含量),从而增加了锚蛋白的可及位点。
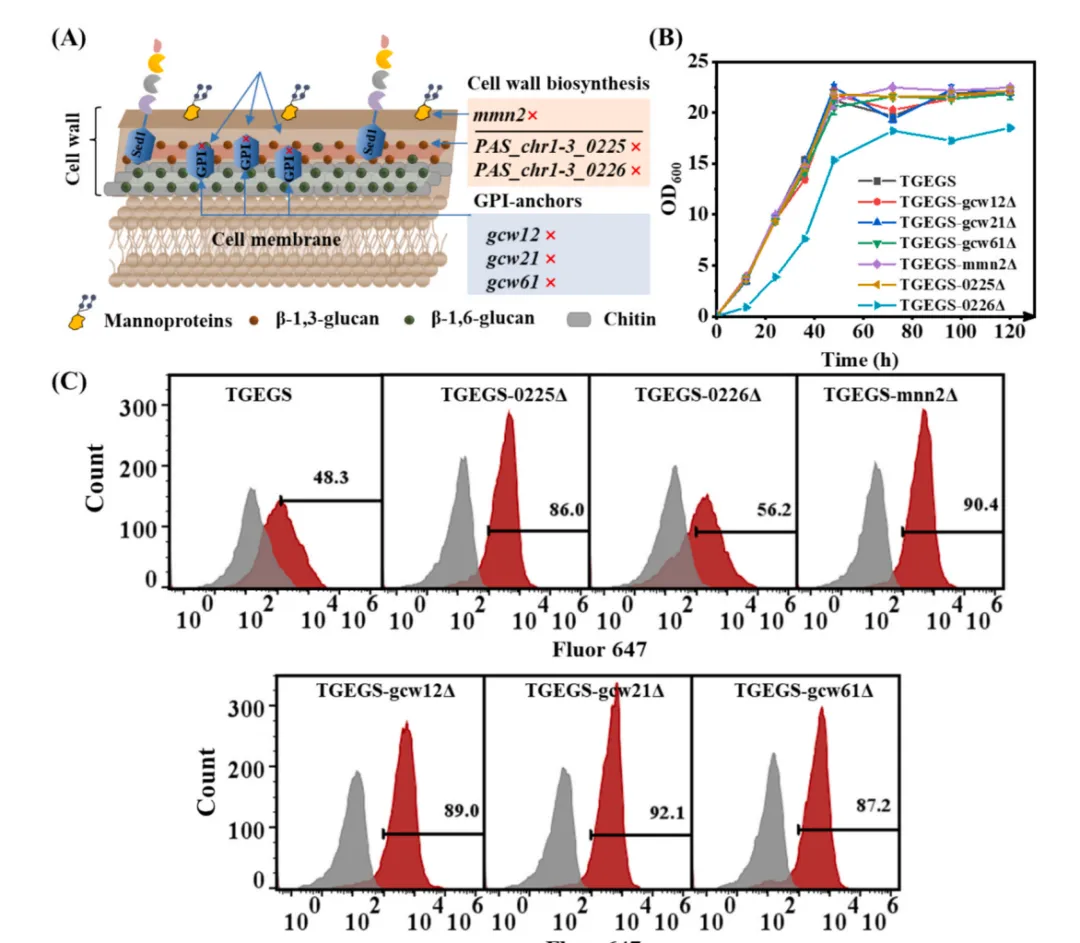
图3 构建和验证
结果4、双酶展示菌株的构建与功能验证
在优化后的支架菌株基础上,共展示了Xyn和Hixyl43A。与对照菌株TGEGS-XH相比,所有细胞壁工程改造的双酶展示菌株的胞内Xyn和Hixyl43A活性均显著提高,其中TGEGSΔGCW21-XH的Xyn活性达1.10 U/mL,Hixyl43A活性达4.01 U/mL。木聚糖降解实验显示,改造菌株在60分钟内即可完全降解底物,而对照需150分钟,表明双酶共展示显著增强了协同催化效率。
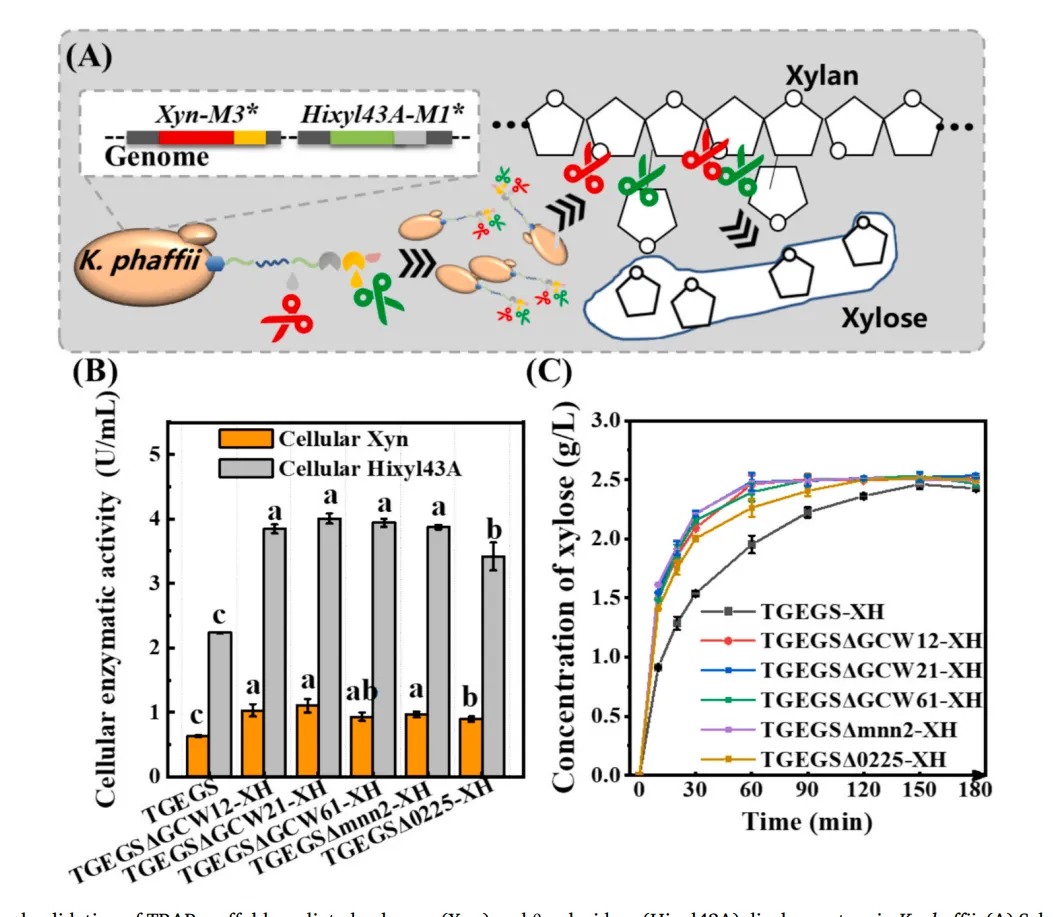
图4 催化效率验证
结果5、展示酶与游离酶的酶学性质比较
细胞表面展示的Xyn和Hixyl43A的最适温度和pH与游离酶基本一致(55°C,pH 5.5-6.5)。但在热稳定性方面,55°C处理5 h后,展示Xyn和Hixyl43A的残余活性分别为78.1%和85.1%,显著高于游离酶的64.7%和68.4%。在pH稳定性方面,展示酶在pH 5.5-6.5范围内均表现出更高的残余活性。这表明TRAP支架展示不仅保持了酶的催化特性,还显著增强了其对高温和pH变化的耐受性。
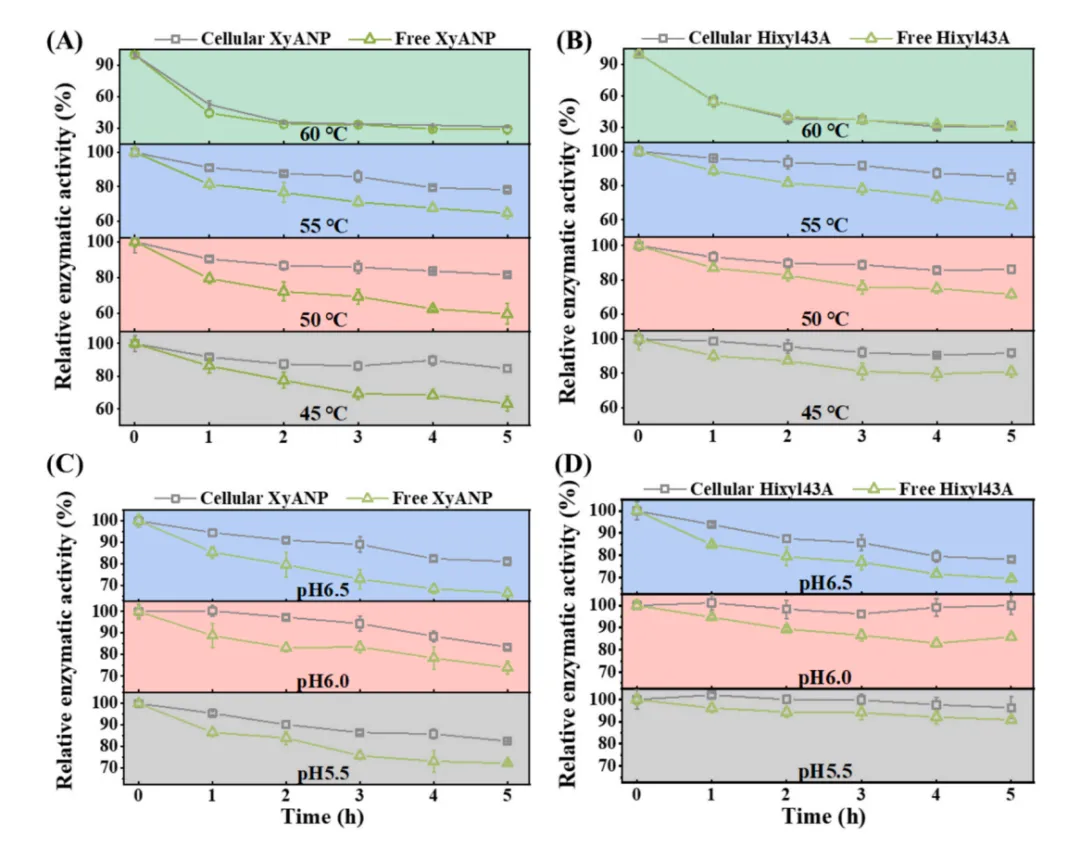
图5 催化条件验证
结果6、共固定化双酶展示细胞的稳定性和重复使用性
引入具有生物膜固定化能力的KpFlo11C结构域,构建了TGEGSΔGCW21-XH-KpFlo11C菌株。在连续8个批次的催化反应中,固定化细胞在前3个循环保持97.6%的相对转化率,第8循环仍达85.9%,而游离细胞仅剩59.9%。在每5个循环后通过YPD培养基再生的条件下,固定化细胞在第6和11循环分别恢复至99.1%和98.2%的相对转化率,第15循环仍保持87.2%的活性,而游离细胞降至48.2%。这表明共固定化策略能有效维持细胞密度、实现细胞再生,显著提升系统的操作稳定性和重复使用性。
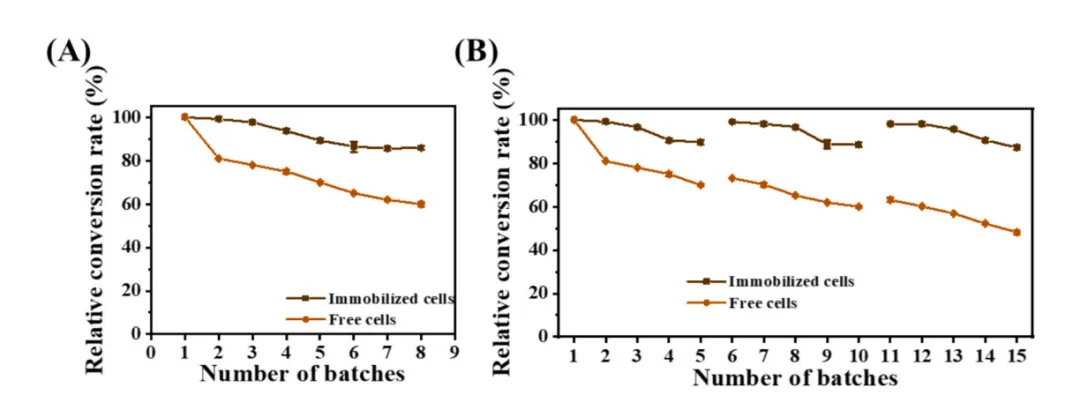
图6 固定化验证
八、讨论
本研究首次将TRAP支架应用于K. phaffii细胞表面,成功构建了双酶共展示系统,并通过连接肽优化和细胞壁工程将展示效率提升至92.1%。与游离酶相比,展示酶具有更优的热稳定性和pH稳定性,双酶协同显著加速木聚糖降解。进一步结合生物膜固定化,实现了高效、稳定、可再生的连续催化体系,15个循环后仍保留87.2%活性。该系统克服了传统支架分子大、组装精度低、稳定性差等局限,为多酶协同催化和绿色生物制造提供了新平台。未来可进一步拓展至其他工业酶和底物体系,并探索其在真实木质纤维素原料中的应用潜力。
