南京医科大学徐志鹏、季旻珺、中科院上海药物研究所周子凯Cell Reports!!找到胎儿神经发育异常关键通路,益生菌可拦截
- 2026-04-16 02:07:01
医学研究前沿——聚焦医学前沿研究进展。100多万医学领域硕博医生们订阅的微信公众号。点击标题下蓝字“医学研究前沿”关注,我们将为您提供最有价值、最前沿的医学前沿资讯。

母体免疫激活(MIA)是子代罹患自闭症谱系障碍、精神分裂症等神经发育缺陷的公认危险因素,但其产前机制长期成谜。孕期暴露于弓形虫速殖子可溶性抗原(STAg)可诱导MIA,导致成年子代出现持续性行为异常及外周炎症,STAg-MIA模型成为研究免疫介导神经发育病理的理想工具。然而,母体STAg暴露与胎脑功能异常的关联,尤其是上游母体因素及母胎界面的下游效应,此前尚不明确。肠道微生物群作为调节宿主免疫与稳态的核心因素,其与MIA的关联在多模型中已有提示,但弓形虫抗原是否会扰乱母体菌群并引发连锁损伤,仍是机制研究的空白。南京医科大学徐志鹏、季旻珺团队联合中国科学院上海药物研究所周子凯,聚焦这一关键问题展开攻关。
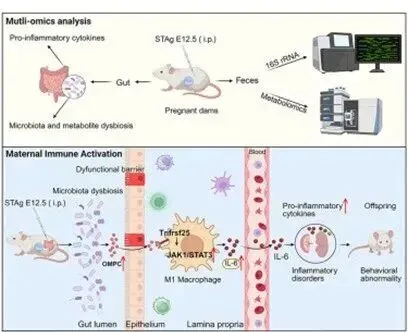
研究团队利用STAg产前诱导构建小鼠MIA模型,发现母体肠道菌群紊乱是子代行为缺陷的核心驱动因素。具体表现为厚壁菌门和放线菌门丰度升高,伴随肠道屏障完整性破坏、代谢与炎症失衡——M1型巨噬细胞活化、IL-6水平上升,关键代谢物1-油酰基-2-肉豆蔻酰基-sn-甘油-3-磷酸胆碱(OMPC)显著蓄积。机制上,OMPC作为“坏信使”,通过与巨噬细胞表面Tnfrsf25受体结合,激活JAK1/STAT3/IL-6信号轴,进而放大胎盘炎症反应,诱发胎脑神经炎症,最终导致子代行为异常。这一发现首次揭示肠道来源的OMPC在STAg诱导MIA中的核心作用,明确了“菌群紊乱-代谢物蓄积-信号轴激活-母胎炎症-神经损伤”的完整致病链条,填补了母体因素与子代神经发育关联的机制空白。
基于上述机制,团队提出针对性干预策略:母体补充鼠李糖乳杆菌GG(LGG)益生菌。实验证实,LGG可有效恢复肠道-免疫稳态,降低OMPC水平,抑制JAK1/STAT3/IL-6信号轴过度激活,从而减轻胎盘炎症与胎脑神经损伤,显著改善子代行为障碍。该研究不仅阐明弓形虫参与神经发育风险的新路径,更将母体肠道与胎盘确立为可干预的关键界面,为高危妊娠胎儿神经发育保护提供了“微生物组靶向”的预防思路。LGG作为临床常用益生菌,其安全性与可及性为成果转化奠定基础,有望为MIA相关神经发育缺陷的早期防控开辟新方向。



说明:
🔹本文仅作科研人员学术交流。
🔹本文内容若存在版权问题,请联系我们及时处理。
🔹欢迎广大读者对本文进行转发宣传。
🔹《医学研究前沿》会不断提升自身水平,为读者分享更加优质的材料研究成果解读,欢迎关注我们。
欢迎广大科研工作者投稿最新研究成果。
