利用酶触发电荷变化的双通道纳米传感器,实现多菌种无标记检测
第一作者:Ruyi Wang,Lingfei Han
通讯作者:Chen Wang
通讯单位:南京师范大学;南京鼓楼医院
发表时间:2026年4月14号
发表期刊:Journal of the American Chemical Society
这篇文章作者提出了一种基于非对称双通道纳米移液管(ADNP)的无标记细菌检测方法。作者在两个纳米通道中分别修饰可响应 β-Gal 和 β-Glu 的探针,利用不同细菌的酶表达差异触发表面电荷变化,进而改变离子流整流行为,形成具有区分度的 I–V 信号。该平台可在 30 min 内实现多菌种识别,对 E. coli 和 K. pneumoniae 的检测限分别达到 12 CFU/mL 和 126 CFU/mL,并在牛奶、饮用水和血清等复杂样本中验证了较好的回收率和稳定性。其核心价值在于把“细菌酶指纹”转化为“纳米通道电信号”,为食品安全和临床感染快速筛查提供了一种新的传感思路。
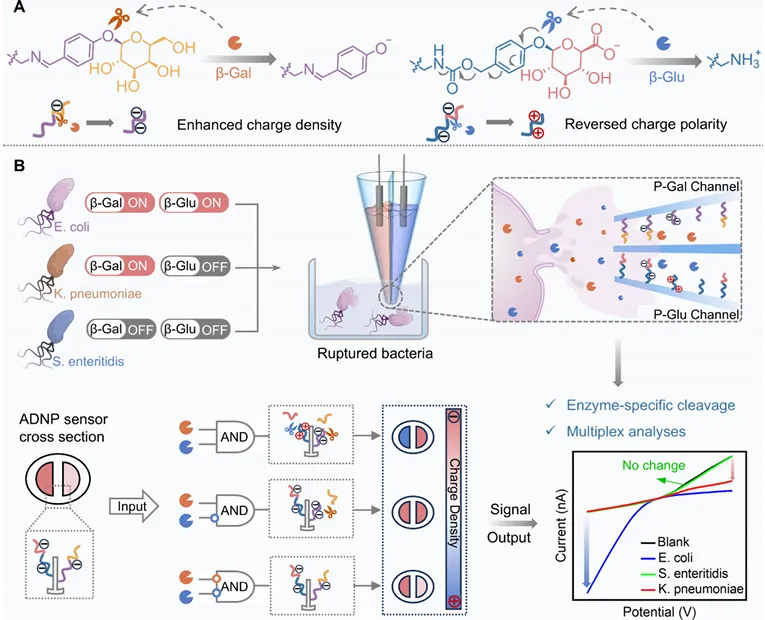
1、提出“酶指纹”检测思路,绕开传统抗体/核酸体系。 利用细菌特异性酶(β-Gal、β-Glu)实现识别,本质是从“结构识别”转向“功能识别”。
2、双通道纳米移液管实现“电荷不对称放大”。 通过两通道电荷差异 反映离子流整流(ICR)变化 ,实现信号放大和区分能力提升。
3、实现真正的无标记、多重检测(multiplex)。 不依赖荧光/标记物,仅靠电流曲线形态变化区分不同细菌。
Figure 1 这张图主要证明 ADNP 传感器被成功构建。作者利用 θ 型毛细管拉制出具有两个独立纳米通道的双通道纳米移液管,并通过 SEM、暗场成像和荧光成像确认其双通道结构。随后,两个通道分别修饰 P-Gal 和 P-Glu 探针,通过 I–V 曲线和 ICR 比值变化证明通道内表面功能化成功。Figure 1 是整篇文章的结构基础:只有双通道独立修饰成立,后面的“电荷不对称调控”和多重检测才有意义。
Figure 1.(A–C)双通道纳米移液管的结构表征,包括 SEM、暗场图像和荧光图像;(D)纳米通道内表面功能化过程示意图;(E–H)P-Gal 和 P-Glu 通道构建过程中的 I–V 响应及 ICR 比值变化。
Figure 2 解释了 ADNP 的核心响应机制。P-Gal 和 P-Glu 分别与 β-Gal、β-Glu 发生特异性酶切反应,导致通道表面电荷发生变化。β-Gal 作用后,P-Gal 通道负电性增强,使双通道电荷趋于对称,I–V 曲线接近欧姆行为;β-Glu 作用后,P-Glu 通道发生电荷反转,形成正/负双极性不对称结构,引起反向整流增强。Figure 2 说明信号来源不是传统结合事件,而是“酶切反应引发的表面电荷重构”。
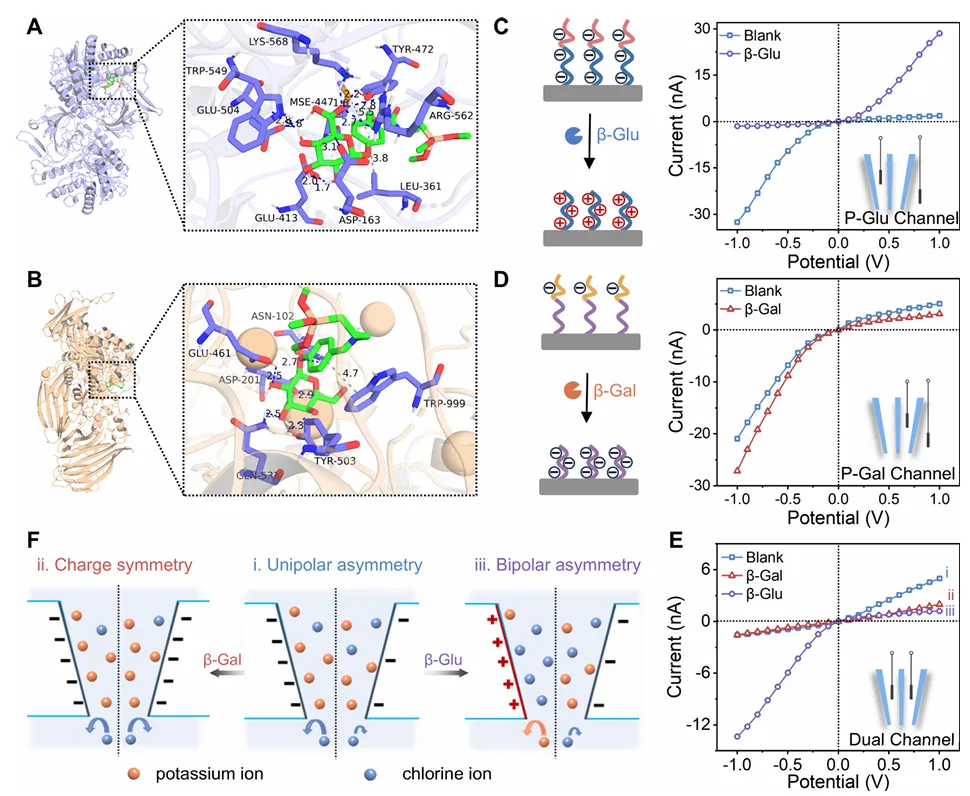
Figure 2.(A, B)β-Glu/P-Glu 和 β-Gal/P-Gal 的分子对接模拟;(C, D)P-Glu 和 P-Gal 单通道在酶作用前后的 I–V 曲线;(E)ADNP 在 β-Gal 或 β-Glu 处理前后的 I–V 响应;(F)不同表面电荷状态下的离子传输与整流机制示意图。
Figure 3 验证 ADNP 对目标酶的分析性能。作者先优化了反应时间,确定 30 min 可以获得稳定响应;随后分别检测 β-Gal 和 β-Glu,建立 IGR 与酶浓度之间的定量关系。结果显示,ADNP 对 β-Gal 和 β-Glu 均具有较低检测限,并且双通道结构比单通道结构更灵敏。选择性实验和抑制实验进一步说明,信号确实来自特异性酶切,而不是其他酶或非特异吸附干扰
Figure 3. (A)ADNP 固定装置示意图;(B)ADNP 对酶响应的时间变化;(C)ADNP 对 β-Gal 或 β-Glu 的响应示意;(D, E)β-Gal 和 β-Glu 检测的 I–V 曲线及校准曲线;(F)单通道与双通道检测限对比;(G, H)选择性和抑制实验验证。
Figure 4 是文章从酶检测实现细菌检测的关键。作者利用不同细菌的酶表达差异建立“酶指纹”:S. enteritidis 不表达 β-Gal/β-Glu,K. pneumoniae 主要表达 β-Gal,E. coli 同时表达 β-Gal 和 β-Glu。经过裂解释放酶后,不同细菌会触发不同通道响应,从而产生不同 I–V 曲线和 IGR 变化。PCA 结果进一步显示三种细菌可以被清晰区分,证明该平台具备多菌种无标记识别能力。
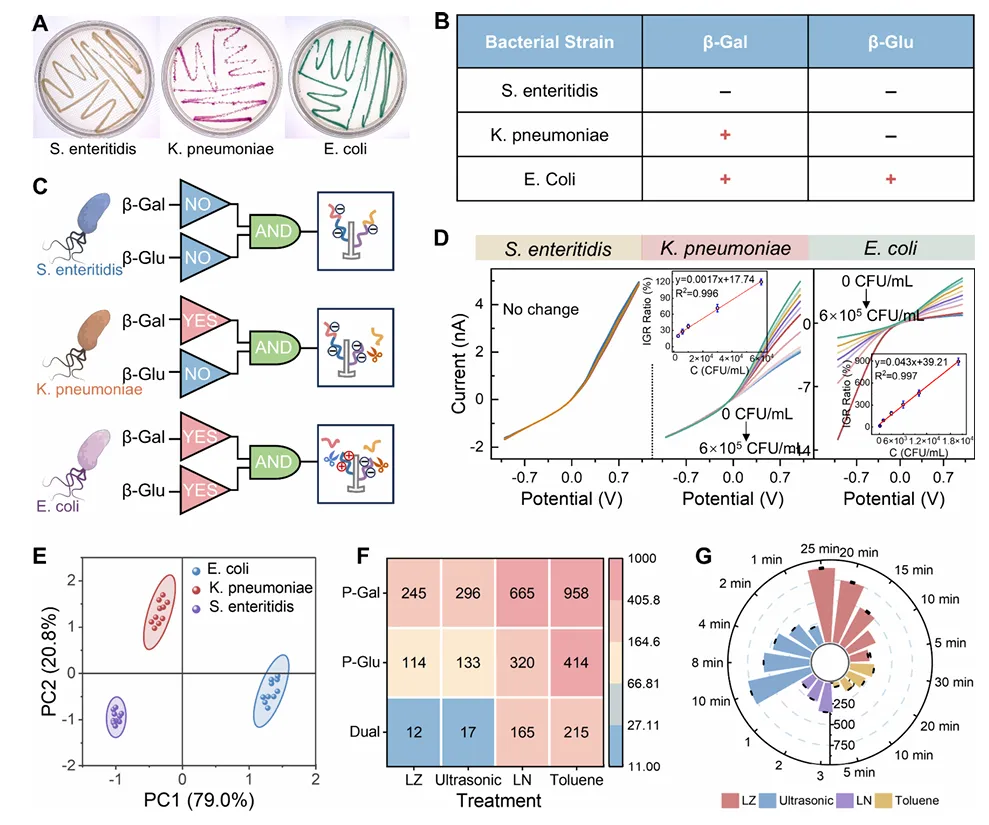
Figure 4. (A)E. coli、K. pneumoniae 和 S. enteritidis 在显色培养基上的表现;(B)三种细菌的 β-Gal 和 β-Glu 表达情况;(C)ADNP 对不同细菌输入的响应逻辑;(D)不同细菌裂解液的 I–V 曲线及校准关系;(E)PCA 区分结果;(F, G)不同应激条件下的检测限和信号变化。
Figure 5 这张图验证 ADNP 在实际复杂样本中的应用能力。作者将 E. coli 和 K. pneumoniae 加标到饮用水和牛奶中,经处理后用 ADNP 检测,结果显示 I–V 曲线和 IGR 比值随细菌浓度变化而变化,说明该方法在食品和环境样本中仍能工作。回收率和 RSD 结果表明检测准确性和重复性较好,进一步支持其在食品安全和现场筛查中的应用潜力。
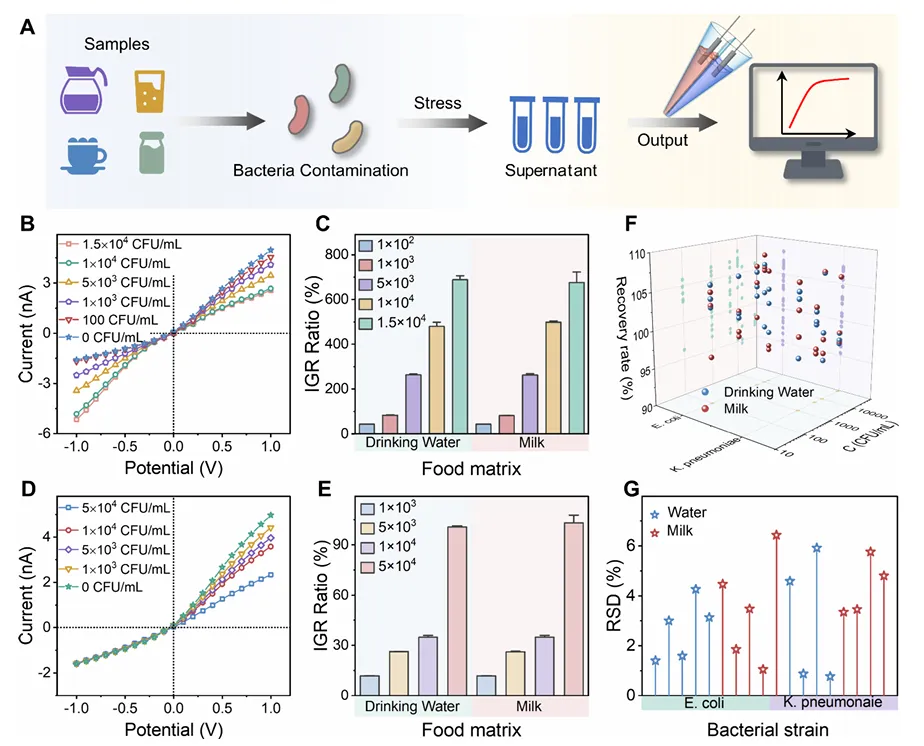
Figure 5. (A)食品基质中细菌定量检测流程示意;(B)牛奶中加标 E. coli 的 I–V 曲线;(C)饮用水和牛奶中 E. coli 的 IGR 变化;(D)牛奶中加标 K. pneumoniae 的 I–V 曲线;(E)饮用水和牛奶中 K. pneumoniae 的 IGR 变化;(F, G)水和牛奶样本中的回收率与 RSD 分析。
这篇工作的创新不在于把细菌测得更低,而在于换了一条检测逻辑:不依赖抗体或核酸识别,利用细菌的酶功能差异作为信息源,通过双通道纳米移液管把这种差异转化为可编程的电荷不对称变化,进一步放大为可区分的离子流整流信号。双通道结构不仅提供了多重检测能力,还通过电荷对称/反转带来的信号形态变化实现更稳定、更高信噪比的读出,从而在复杂样本中仍能保持可靠性。为传感体系从“分子识别”走向“功能响应”提供了一个可扩展的思路。
https://doi.org/10.1021/jacs.5c23220