南京农业大学张秋勤副教授团队:利用酵母发酵驱动魔芋葡甘聚糖形成可食用3D多孔支架,显著提升益生菌生物膜形成与冷冻干燥耐受性
- 2026-05-10 22:09:03
南京农业大学张秋勤副教授团队:利用酵母发酵驱动魔芋葡甘聚糖形成可食用3D多孔支架,显著提升益生菌生物膜形成与冷冻干燥耐受性

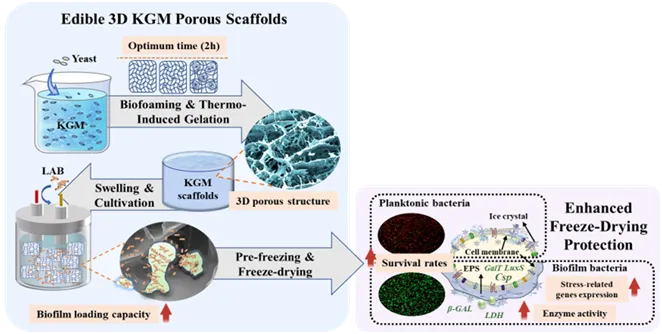
乳酸菌(LAB)作为益生菌和工业发酵剂被广泛应用。然而冷冻干燥作为行业标准的保藏手段,常对菌体造成包括细胞膜破裂和代谢休眠在内的严重损伤,大幅降低其工业活性。传统的冷冻保护剂如糖类和脱脂乳仅能提供部分保护,并可能对终产品的感官和营养特性产生不良影响。一个具有前景的替代方案在于“生物膜态”益生菌,它们可形成由胞外聚合物(EPS)组装而成的坚固基质,对酸、渗透和热胁迫具有卓越的耐受性,被视为超越传统浮游态菌体的下一代益生菌。
生物膜的成功定殖与增殖,需要一个能让细菌深度渗透并形成结构化群落的多孔环境,这依赖于互联的大孔网络来提供充足的粘附表面积和实现营养物质对流传输。然而,可食用载体在结构上存在局限,比如电纺纳米纤维孔隙互联性差,水凝胶则多限于纳米级孔隙,仅适用于封装浮游细胞,无法支撑浸润式生物膜生长。在制造方法层面,冷冻干燥、三维打印和静电纺丝等宏观多孔水凝胶制备策略多属于高能耗的实验室规模技术,而新兴的气体发泡方法则依赖非生物降解的表面活性剂或有毒发泡试剂,难以满足食品级要求。因此,如何通过温和、绿色的策略构建兼具可食性与互联大孔结构的三维支架,以引导和支撑益生菌生物膜形成,仍是尚未解决的挑战。
为应对益生菌工业冻干活性损失大及传统载体孔隙连通性不足等挑战,本研究通过优化KGM浓度并引入酵母驱动生物发泡技术,成功制备了具有层次化互联大孔结构的最优支架(7% KGM,发泡2 h)。该支架孔隙率从47.8%显著提升至85.5%,生物膜负载量达8.66 log CFU/cm³。所培养的生物膜态L. plantarum在冻干后的存活率较浮游态菌体提高约30%,同时保持了更完整的细胞膜、更高的β-半乳糖苷酶和乳酸脱氢酶活性,并显著上调了冷休克蛋白、群体感应等胁迫应答关键基因的表达。这些优势归因于生物膜胞外聚合物基质的物理屏障作用及其介导的群体感应适应性响应。
与现有高能耗的物理致孔或依赖化学交联剂的策略相比,本研究的创新之处在于:利用GRAS微生物和温和加工条件,全程无需引入毒害化学试剂,为食品级多孔益生菌载体的制备提供了绿色、可放大的技术路径。此外,该支架平台的普适性初步得到了多种乳酸菌的验证,为进一步拓展应用奠定了基础。
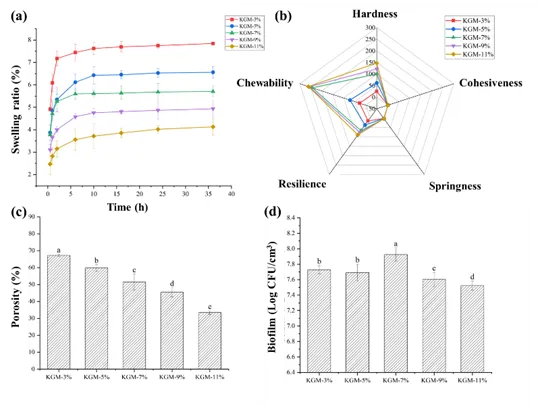
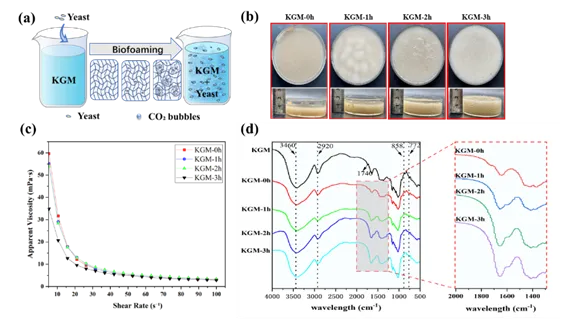
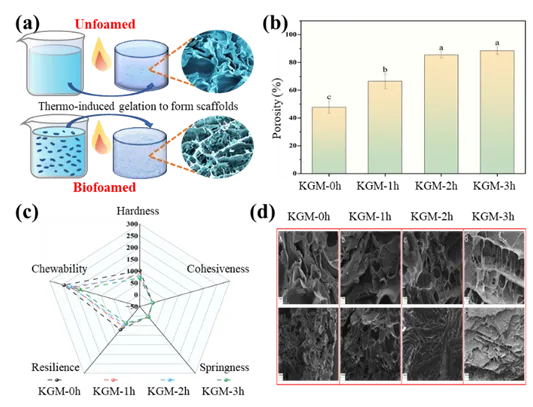
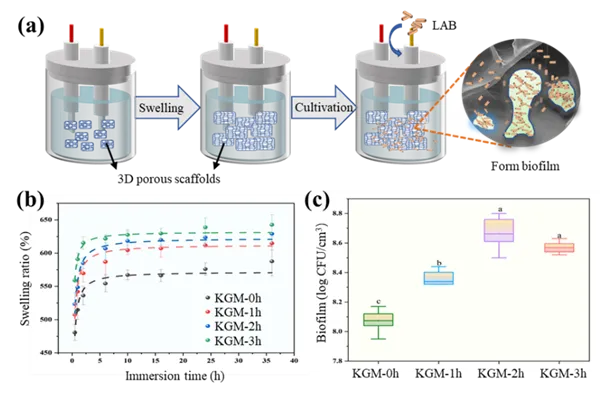
图4. KGM 3D多孔支架作为生物膜载体应用的示意图(a)、发泡时间对KGM支架溶胀能力(b)和生物膜定殖(c)的影响。注:不同小写字母表示差异显著(P <0.05)。
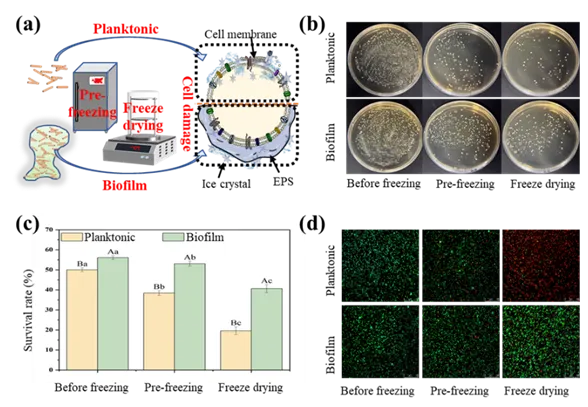
图5. 冷冻干燥过程中细胞损伤示意图(a)、浮游态和生物膜态细菌在预冷冻和冷冻干燥后的细胞活力(b)、溶菌酶敏感性(c)和细胞染色(d)。注:大写字母表示生物膜态与浮游态之间差异显著(P < 0.05),小写字母表示不同阶段之间差异显著(P <0.05)。
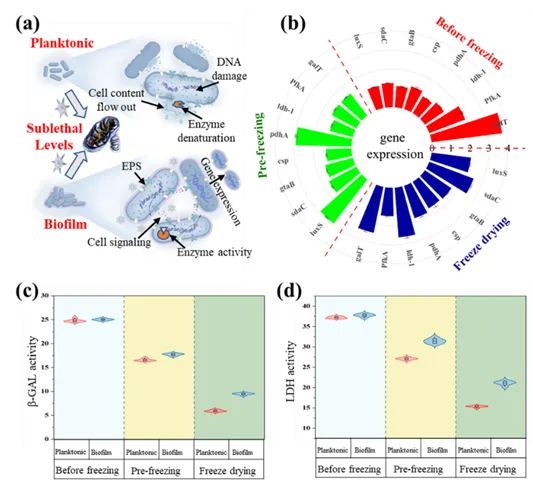
图6. 冷冻干燥过程中细菌活力示意图(a)、生物膜态与浮游态L. plantarum在冷冻干燥过程中胁迫相关基因的相对表达量(b)以及β-半乳糖苷酶(c)和乳酸脱氢酶(d)的活性。
张秋勤,南京农业大学食品科技学院副教授,生物工程系副主任,江苏省淮安区博里镇科技副镇长,研究方向为食品微生物资源挖掘及应用、功能性食品开发,主持并参与国家自然科学基金面上项目、国家自然科学基金青年项目、江苏省农业科技自主创新资金项目、三亚崖州湾科技城“崖州湾”菁英人才科技专项、企业横向合作等项目10余项,共计发表SCI论文50余篇,国家授权发明专利2项。参编CRC Press英文专业书籍1部,参译英文专业书籍1部。曾任“江苏省科技副总”以及“国家食药同源产业科技创新联盟理事”等职务;Food chemistry、Foods等期刊的审稿人;Molecules特刊的客座主编。
版权声明
本文转载自“食品放大镜”微信公众号,转载仅用于学术分享,若有侵权,请后台留言联系修改或删除!
 千人盛会||第四届食药同源功能食品大会--广州 2026年7月16-18日
千人盛会||第四届食药同源功能食品大会--广州 2026年7月16-18日