单细胞测序分析:TAMs高表达MCT4,GSCs高表达MCT1,且两者在GBM组织中空间共定位。[图1a-d]
功能验证:TAM敲除MCT4后,上清液乳酸水平下降70%,GSC摄取乳酸减少;GSC敲除MCT1后,13C标记乳酸摄取量降低约55%,证实MCT4-MCT1依赖的乳酸转运。[图1g-k]
动物模型:髓系特异性敲除MCT4的小鼠,肿瘤体积缩小,生存期延长,肿瘤细胞内乳酸水平降低40%。[图1m-p]
图1. GSCs与TAMs中的乳酸代谢及转运蛋白特性
GSC增殖实验:外源性乳酸以剂量依赖方式促进GSC增殖,TAM上清液可刺激GSC神经球形成,而MCT4敲除TAM的上清液则抑制该效应,外源性乳酸可挽救。[图2a-c]
MCT1功能验证:GSC敲除MCT1后,乳酸诱导的增殖和神经球形成被阻断,回补MCT1可恢复。[图2f-i]
体内实验:GSC敲除MCT1的小鼠模型中,肿瘤生长减缓,生存期延长。[图2j-k]
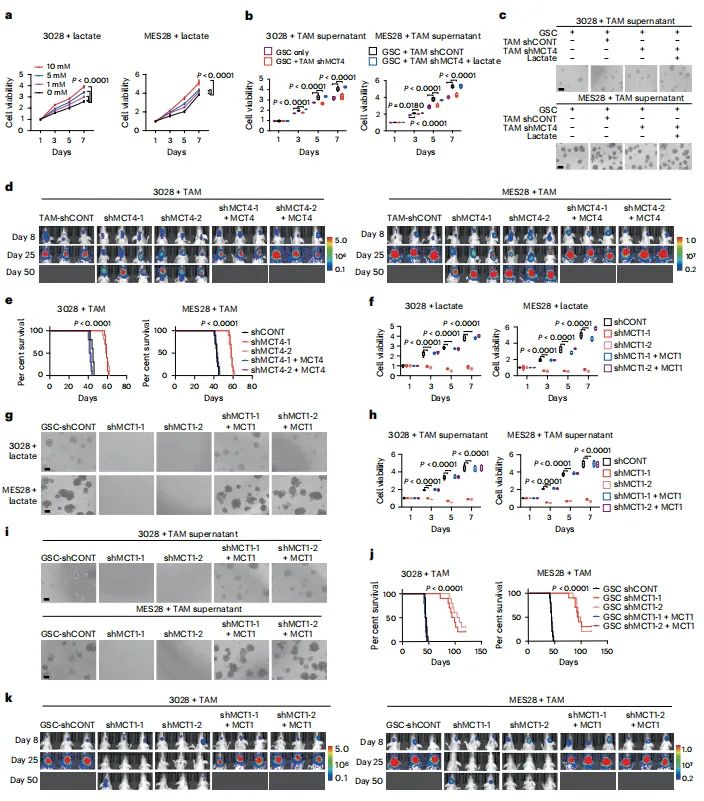 图2. 通过MCT1–MCT4在胶质瘤干细胞与肿瘤相关巨噬细胞之间转运乳酸可促进GSCs增殖
图2. 通过MCT1–MCT4在胶质瘤干细胞与肿瘤相关巨噬细胞之间转运乳酸可促进GSCs增殖
核心发现:TAMs通过MCT4分泌乳酸,GSCs通过MCT1摄取乳酸,形成代谢耦联。
KU70 K317乳酸化调控GSC干性与DNA修复
乳酸化水平检测:GSC的泛乳酸化水平显著高于NSC,TAM上清液刺激可提升GSC乳酸化,而MCT1敲除或MCT4敲除则降低乳酸化。[图3a-c]
KU70 K317乳酸化鉴定:质谱显示KU70是GSC中差异乳酸化最显著的蛋白之一,K317位点乳酸化在GSC中高表达,而总KU70水平无差异。[图3d-h]
功能实验:KU70敲除抑制GSC增殖,回补WT KU70可恢复,而回补K317R突变体则无法完全恢复,且K317R组小鼠生存期延长、肿瘤体积缩小。[图3j-m]
图3. TAM来源的乳酸诱导了DNA损伤修复蛋白KU70 K317的乳酰化,从而导致胶质瘤干细胞增殖
NHEJ修复效率:MCT1敲除或KU70 K317R突变显著降低NHEJ活性,增加γ-H2AX水平。[图4a,d]
干性维持:MCT1敲除或KU70 K317R突变导致GSC干性标志物表达下降,NHEJ抑制剂NU7441可模拟该效应。[图4g-h]
分子机制:KU70的Ku核心区是与KU80结合的关键区域,K317R突变削弱KU70-KU80-DNA-PKcs复合物形成 。[图4j-k]
图4. KU70K317位点的乳酰化修饰可增强NHEJ功能并维持GSC的干性
核心发现:TAM来源乳酸诱导KU70 K317乳酸化,增强NHEJ修复并维持GSC干性。
KU70 K317乳酸化抑制
cGAS-STING通路与免疫抑制
通路富集分析:MCT1敲除、KU70敲除或K317R突变均富集IFN-α/β应答通路,提示cGAS-STING激活。[图5a-c]
胞质dsDNA与cGAS激活:MCT1敲除或KU70 K317R突变导致GSC胞质dsDNA积累,cGAS与dsDNA共定位增加。[图5e-f]
信号通路验证:MCT1敲除或KU70 K317R突变激活cGAS-STING-TBK1-IRF3通路,增加IFN-α/β分泌,而回补WT KU70可抑制该通路 。[图5g-h]
免疫细胞浸润:TCGA数据库分析显示MCT1高表达与CD8⁺T细胞signatures负相关,提示免疫抑制。[图5k-l]
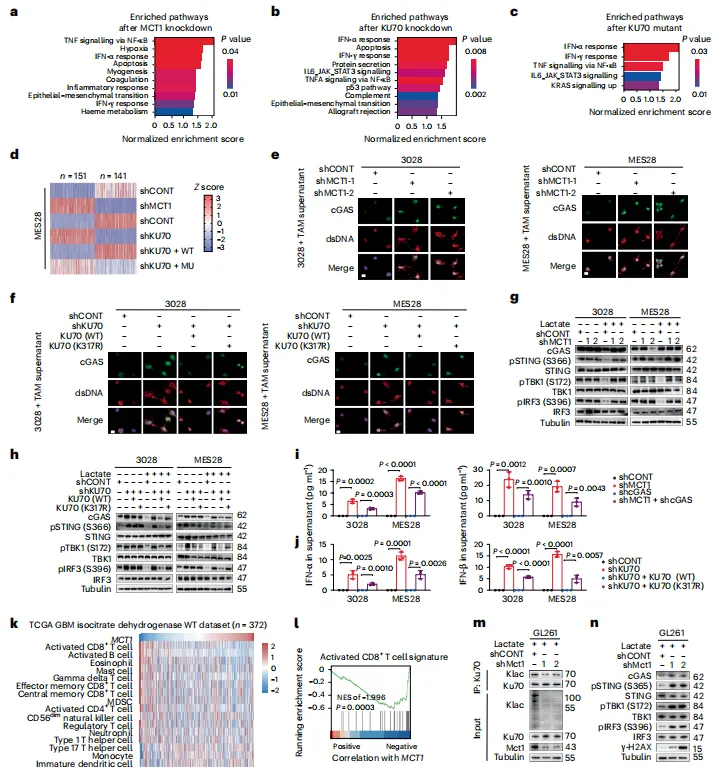 图5. KU70K317位点的乳酰化可抑制cGAS–sting信号通路,并维持免疫抑制TME
图5. KU70K317位点的乳酰化可抑制cGAS–sting信号通路,并维持免疫抑制TME
用hM3Dq激活IBS小鼠vDG颗粒细胞后,旷场中心时间增加、悬尾和强迫游泳不动时间减少(图6A-F)。vDG神经元活性是缓解情绪症状的“充分条件”——不需要吲哚,直接激活vDG就能起效。
抑制vDG→吲哚白白浪费:用hM4Di抑制vDG颗粒细胞后,吲哚的抗焦虑和抗抑郁效果全部消失(图6G-L)。vDG神经元活性同时也是吲哚起效的“必要条件”——没有vDG参与,吲哚再多也没用。 一正一反,闭环完美。
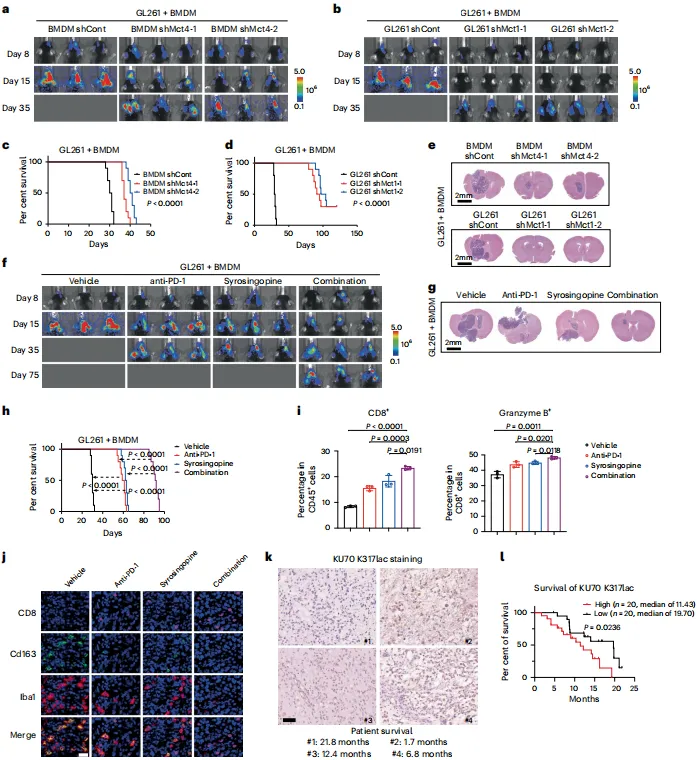 图6. 乳酸转运体抑制剂联合PD-1抗体在GBM中的治疗效果
图6. 乳酸转运体抑制剂联合PD-1抗体在GBM中的治疗效果
核心发现:KU70 K317lac通过减少胞质dsDNA积累,抑制cGAS-STING通路,导致免疫抑制。
MCT抑制剂单药疗效:TAM敲除MCT4或GSC敲除MCT1均显著抑制肿瘤生长,延长小鼠生存期。[图6a-e]
联合治疗:MCT抑制剂联合抗PD-1抗体较单药更显著缩小肿瘤体积,延长生存期,CD8⁺T细胞浸润和颗粒酶B分泌增加,TAMs减少 。[图6f-h]
KU70 K317肽靶向治疗:KU70 K317-Peptide联合抗PD-1抗体可抑制肿瘤生长,延长生存期。[图6o-p]
临床相关性:GBM患者样本中KU70 K317lac高表达与生存期缩短显著相关(中位生存期:11.43vs.19.70个月,P=0.0236)。[图6k-l]
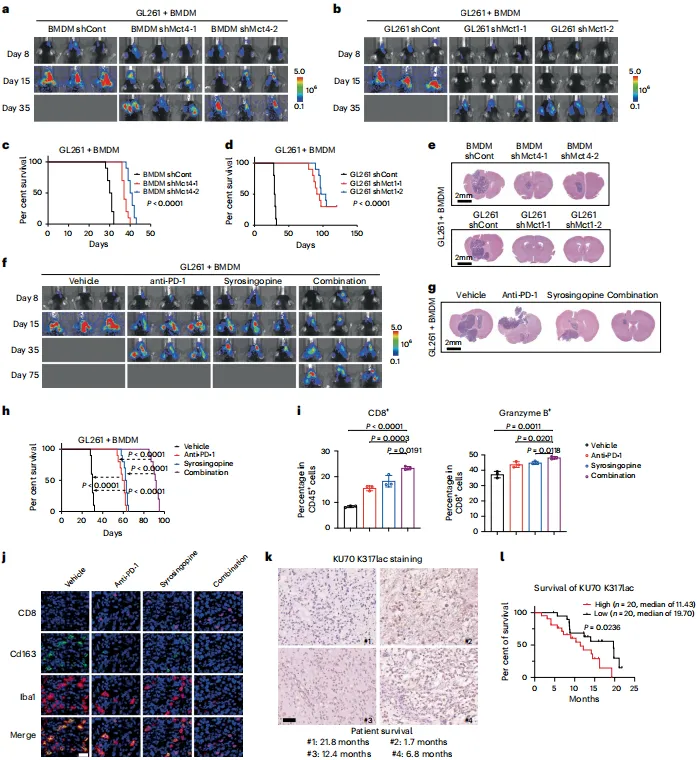 图6. 乳酸转运体抑制剂联合PD-1抗体在GBM中的治疗效果
图6. 乳酸转运体抑制剂联合PD-1抗体在GBM中的治疗效果
核心发现:靶向乳酸转运或KU70乳酸化联合抗PD-1抗体可增强抗肿瘤效果。