Med Rev | 徐州医科大学钟丹丹/北京大学国际癌症研究院谢正伟阐述衰老与代谢性疾病的机制及治疗
- 2026-04-08 02:20:05

衰老与代谢性疾病之间存在着错综复杂的双向分子机制联系,从而形成一个有害的生理衰退循环。这一循环由多种关键因素驱动,包括营养感知异常、线粒体功能障碍、细胞衰老、慢性炎症、表观遗传修饰、昼夜节律紊乱以及肠道菌群失衡。
针对衰老-代谢轴的新兴干预措施有望显著延长健康寿命。这些方法包括使用药理模拟物、衰老细胞清除剂、多组学策略以及微生物组调节,所有这些方法都旨在恢复代谢稳态并减轻与年龄相关的病理。
然而,将这些策略转化为临床实践仍然面临诸多挑战。这些挑战包括需要实现组织特异性靶向、确保干预措施的长期安全性以及解决医疗保健服务获取方面的社会经济差异。
未来的研究重点在于整合多组学技术、类器官和人类细胞模型,并构建公平的精准医疗框架。这些举措旨在延长健康寿命,并减少与衰老相关的代谢疾病对全球的影响。
衰老过程中组织特异性代谢改变
衰老会引发不同组织中不同的代谢改变,这些改变共同导致全身功能衰退和疾病风险增加。这些组织特异性代谢转变是衰老过程的核心,驱动着与年龄相关的机能衰退、虚弱以及对各种疾病易感性的增加(图 1)。
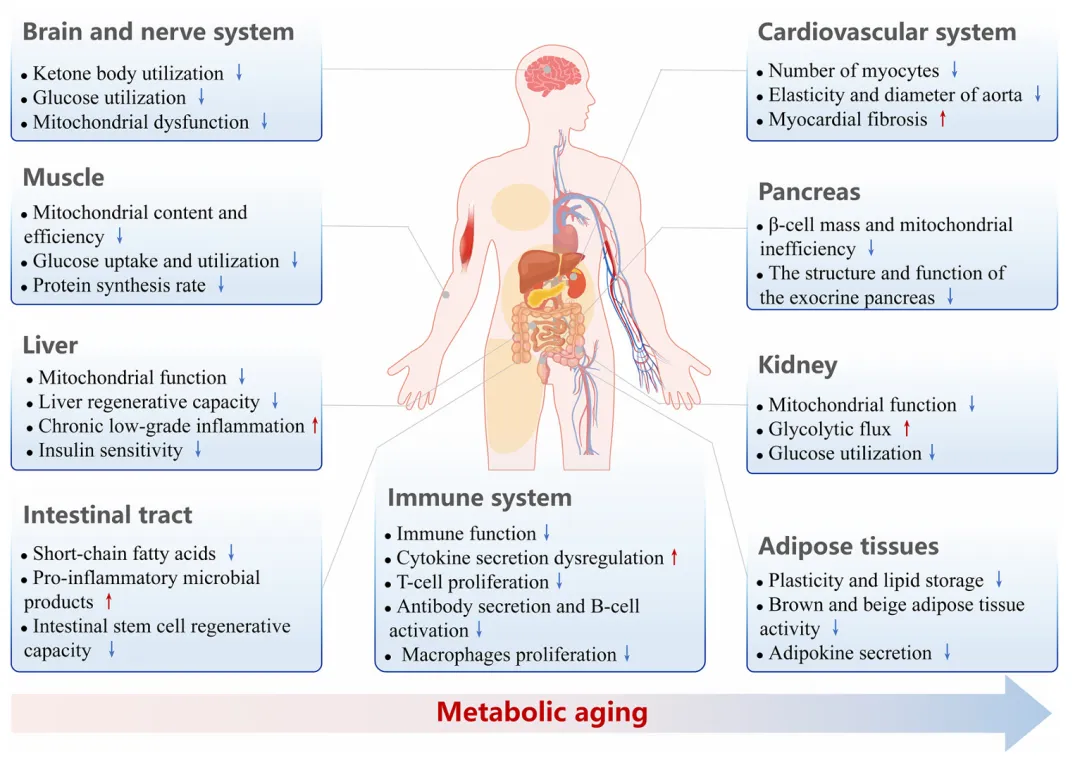
图1. 代谢衰老及其靶组织。
衰老-代谢通路的分子机制
衰老伴随着一系列特征性的代谢改变,这些改变导致细胞和组织功能逐渐衰退。这些相互关联的代谢变化驱动着衰老过程,损害再生能力,并增加对年龄相关疾病的易感性,凸显了代谢作为促进健康老龄化和长寿干预措施的核心靶点(图2)。
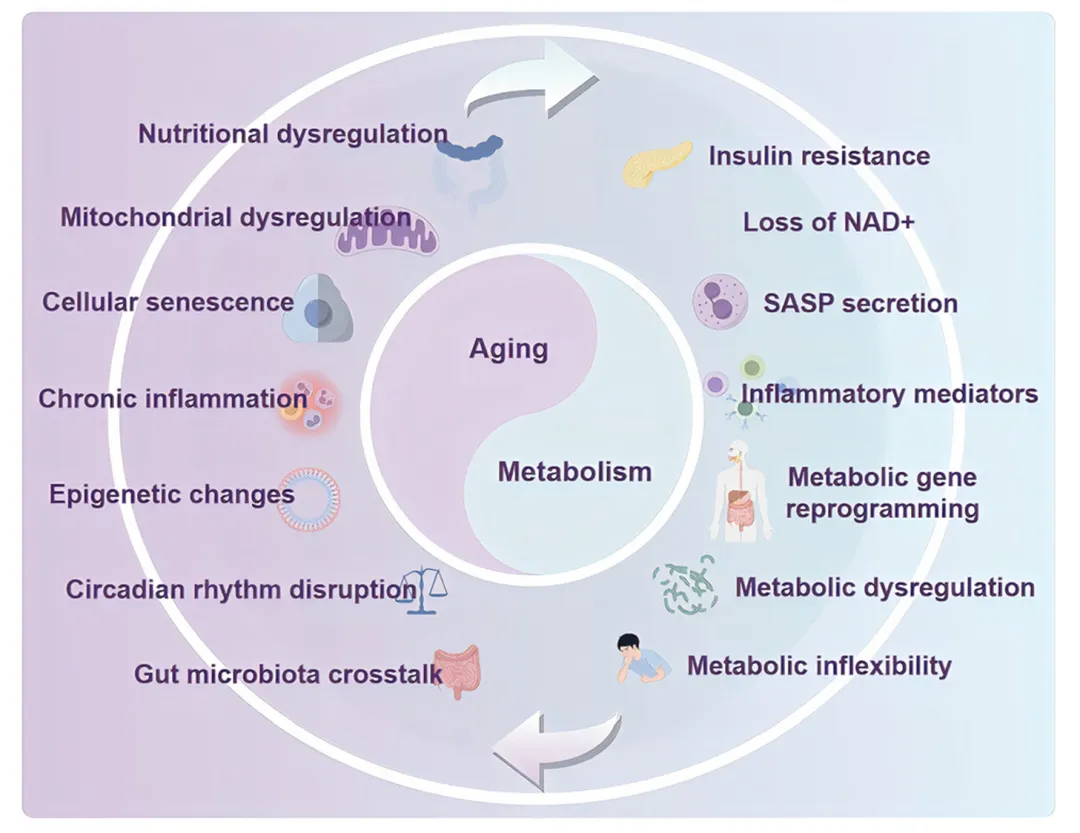
图2. 衰老与代谢性疾病之间的相互作用机制。
昼夜节律紊乱
衰老会扰乱昼夜节律,而昼夜节律控制着代谢过程的每日波动,从而加剧肥胖、2型糖尿病和心血管疾病的风险。核心时钟基因,例如BMAL1和CLOCK,调节营养感知通路和线粒体功能,但它们的表达会随着年龄的增长而下降,导致脂质和葡萄糖代谢失调。相反,代谢紊乱——例如高脂血症和胰岛素抵抗——会通过改变组蛋白乙酰化模式和降低BMAL1表达来加剧昼夜节律紊乱,从而形成双向反馈回路。
此外,与年龄相关的昼夜节律紊乱还会扰乱肠道菌群节律,减少丁酸等有益代谢物,并增加促炎分子(例如脂多糖)的水平,从而损害肠道屏障功能和全身胰岛素敏感性。在代谢相关脂肪肝(MASLD)中,肝脏生物钟紊乱会通过失调PPARα介导的脂肪酸氧化促进脂质积累。
治疗策略,例如限时进食和补充褪黑素,可以恢复昼夜节律与代谢的同步性,从而改善临床前模型中的葡萄糖耐量和线粒体功能。靶向生物钟增强化合物或NAD+增补剂可能为将衰老与代谢衰退解耦提供新的干预手段。因此,解决昼夜节律功能障碍是缓解年龄相关代谢疾病的关键前沿领域。
文献链接:
