南京医科大学团队研发新型乙酰胆碱纳米传感器:揭秘脊髓类器官中神经元单囊泡存储与释放之谜
- 2026-04-29 19:31:21

乙酰胆碱(ACh)是一种关键的神经递质,通过突触传递调节认知和肌肉收缩等多种生理功能。然而,在单细胞水平上对单囊泡储存和释放动力学进行原位定量化学分析仍是一项重大的技术挑战,阻碍了对生理和病理状态下胆碱能突触可塑性机制的理解。
该研究开发了一种Ti₃C₂ MXene/酶功能化(M@E@CF)纳米传感器,能够实时监测原代胆碱能神经元和人脊髓类器官中囊泡ACh的储存和胞吐释放。
这一研究结果揭示了小鼠和人源神经元中均存在亚量子释放模式。为了进一步阐明胞吐动力学的调控机制,该研究利用一维卷积神经网络(1D-CNN)深度学习模型,根据信号峰值形状对单囊泡胞吐模式进行分类,揭示了不同模式下释放分子数量和动力学参数的显著差异。在唐氏综合征模型中观察到单囊泡ACh的储存和释放显著减少,同时释放分数升高,且胞吐过程中融合孔的持续时间缩短。
因此,M@E@CF纳米传感器平台建立了一个用于探究神经递质储存和释放时空动态的通用工具,为探索胆碱能系统生理功能和病理机制提供了关键的技术基础。
文章介绍

题目:一种用于活体神经元和类器官中单囊泡存储及亚量子胞吐的新型乙酰胆碱纳米传感器
英文题目:A Novel Acetylcholine Nanosensor for Single Vesicle Storage and Sub-Quantal Exocytosis in Living Neurons and Organoids
杂志:Angewandte Chemie International Edition
影响因子:17.0
PMID:41518282
发表时间:2026年1月
Part.01
研究背景
研究囊泡内ACh的化学储存与释放动力学,对于理解胆碱能系统在各种生理和病理状态下的功能至关重要。然而,目前主要的分析局限性源于对同时具备高时间分辨率(微秒级)和高空间分辨率(单细胞水平)的严格要求,尤其是在探究功能完整的系统(如活体神经元或人类类器官)中天然ACh的储存与动力学时。
研究人员开发了胞内囊泡撞击电化学细胞计量法(IVIEC)用于定量活体系统中囊泡内的神经递质含量。单细胞安培法(SCA)与IVIEC的结合能够证明单个囊泡的神经递质释放模式,揭示了儿茶酚胺和谷氨酸在细胞模型和活体神经元中均存在进化上保守的亚量子释放模式。然而,目前尚未实现对单个囊泡水平上ACh在生理和病理刺激下的释放模式进行直接测量。
纳米材料工程的最新进展表明,通过酶固定化基底的合理设计有望克服局限性。MXene具有高比表面积、优异的导电性、丰富的表面官能团和生物相容性,是该应用领域极具前景的候选材料。在各种MXene变体中,Ti₃C₂Tₓ具有优异的电化学响应、催化性能和电子传导能力,有望在稳定酶活性的同时增强电子转移动力学,从而实现对单囊泡水平ACh储存和释放动力学的高灵敏度检测。
该研究提出了一种基于Ti₃C₂Tₓ MXene/酶功能化的新型高灵敏度、高选择性纳米传感器平台,用于ACh分析,实现了对小鼠MGE和人脊髓类器官中胆碱能神经元囊泡ACh储存与释放动力学的实时、高时空分辨率监测,为单囊泡水平的亚量子级ACh释放提供了突破性证据。
总之,这一单囊泡化学分析与监测平台深化了对胆碱能神经传递的基础理解,并为神经系统疾病的研究提供了关键见解。
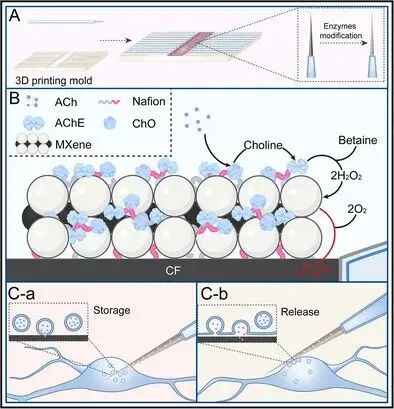
图形摘要:M@E@CF纳米传感器用于检测胆碱能神经元和脑类器官中囊泡储存与释放的示意图。(A) 通过3D打印模具对纳米尖端微电极进行修饰。(B) 电极界面处乙酰胆碱检测的反应机制。(C) 利用M@E@CF纳米传感器对胆碱能神经元囊泡中乙酰胆碱储存(a)的定量分析及囊泡释放(b)的监测。
Part.02
研究关键点
1、 开发基于Ti₃C₂Tx MXene/酶功能化的M@E@CF纳米传感器,利用3D打印模具修饰碳纤维电极,结合乙酰胆碱酯酶(AChE)和胆碱氧化酶(CHO)双酶系统,将非电活性的ACh转化为可检测的电活性物质。
2、 单囊泡乙酰胆碱储存量的电化学检测与药理学验证以及单囊泡量子化释放动力学分析与释放模式分类。
3、 引入1D-CNN模型,对释放信号峰形进行分类(简单峰、平台峰、递增峰、递减峰、重叠峰),揭示不同释放模式的动力学差异。
4、 将技术拓展至人脊髓类器官,验证ACh储存与释放规律的跨物种保守性。
Part.03
研究结果
1、Ti₃C₂Tₓ MXene/酶功能化纳米传感器的制备与表征
Ti₃C₂Tₓ MXene/酶功能化(M@E@CF)纳米传感器的制备实现了单囊泡乙酰胆碱(ACh)储存与释放的高灵敏度检测。
通过3D打印设计并制备定制化反应模具进行空间限域,依次对碳纤维纳米尖端微电极进行Ti₃C₂Tₓ MXene修饰以增强电化学表面积和电子转移,随后固定AChE和ChO,并以Nafion封盖层完成组装,最终构建一个双酶催化平台。
MXene能够增强电子转移,暴露于ACh时,在约+0.4 V处表现出明显的H₂O₂氧化峰。进一步制备包裹不同浓度ACh(14–800 mM)的脂质体以模拟生物囊泡,电流响应与ACh浓度之间存在强线性相关性。此外,纳米传感器对ACh的电流响应显著高于其他测试的干扰物。
这些结果验证纳米传感器可用于内源性生物囊泡中ACh的灵敏且特异性定量检测的可行性(图1)。
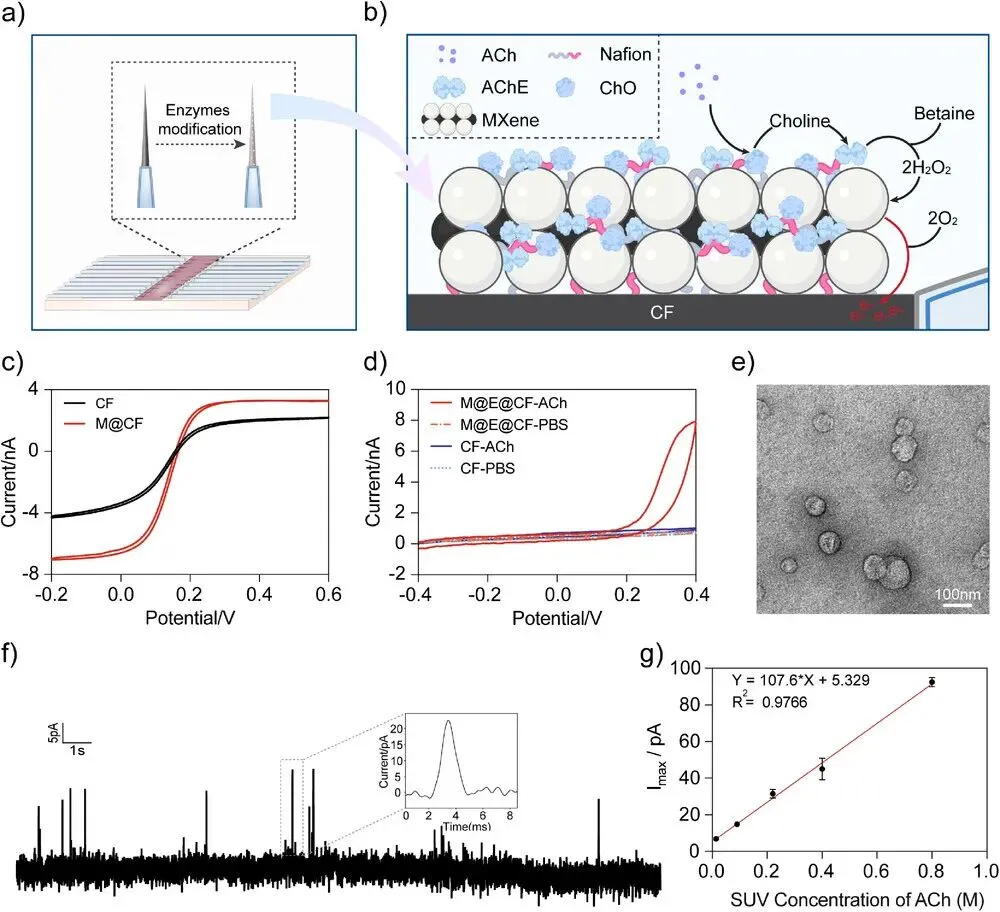
图1 展示M@E@CF纳米传感器制备与表征;SEM显示90 mM ACh脂质体直径约50 nm,安培检测呈现线性电流-浓度关系(R²=0.9766),证实可用于单囊泡定量。
2、通过IVIEC实现胆碱能神经元单囊泡ACh分析
为了验证纳米传感器用于单囊泡ACh检测的可行性,将该传感器应用于原代胆碱能神经元。神经元特异性标志物TUJ1、MGE标志物NKX2.1、前脑标志物FOXG1以及胆碱能神经元特异性标志物ChAT和囊泡乙酰胆碱转运蛋白(VAChT)均呈阳性表达,胆碱乙酰转移酶(ChAT)、TUJ1和GFP的共定位结果进一步验证。在施加电位+0.4 V下进行IVIEC检测,观察到大量尖峰状电流信号。
为了验证这些电流峰源于ACh在M@E@CF纳米传感器上的氧化还原反应,用10 µM胆碱转运体抑制剂(HC-3)对神经元进行4小时预孵育,结果信号强度显著降低。洗脱HC-3后信号强度恢复一半。
此外,当未修饰的CF微电极插入胆碱能神经元时,未观察到安培尖峰。洗脱HC-3后,ACh分子数量恢复至正常水平的56.91%。HC-3还显著降低了电流峰值,洗脱后部分恢复,但半峰宽(t)保持不变。
这些结果表明M@E@CF纳米传感器能够对原代胚胎胆碱能神经元单个囊泡中的ACh储存进行高灵敏度检测,为研究胆碱能神经传递的分子机制提供了一个可靠的平台(图2)。
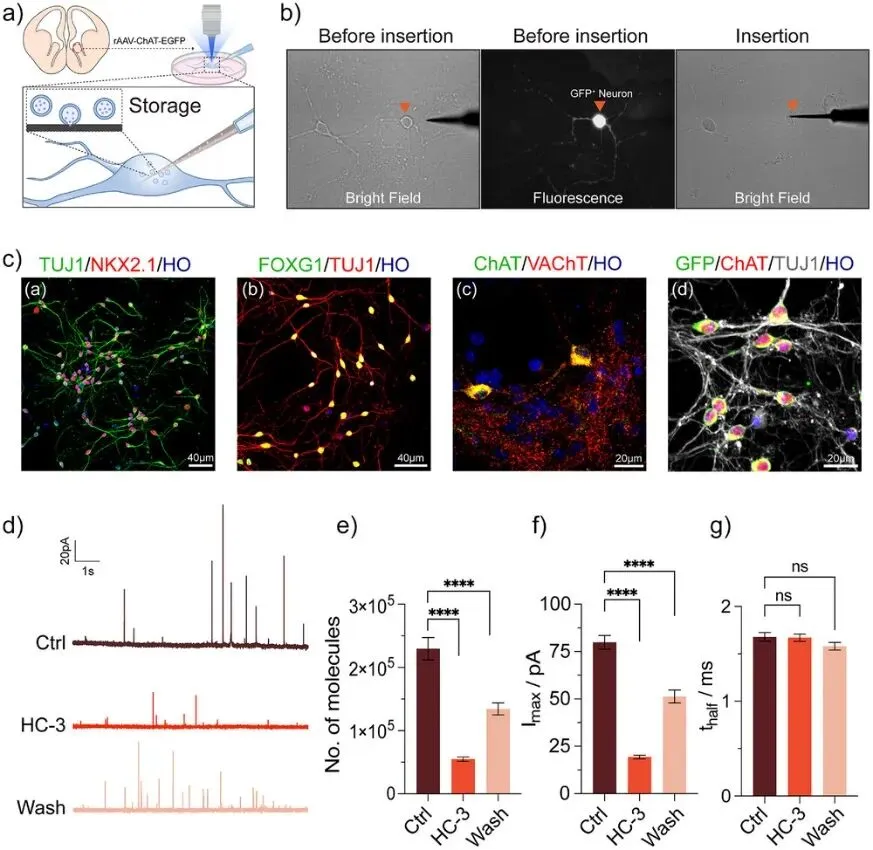
图2 在小鼠MGE原代胆碱能神经元进行IVIEC,记录到代表单囊泡ACh的电流尖峰,HC-3抑制后信号降76%,洗脱部分恢复,平均每个囊泡含约23万分子,验证传感器特异性与灵敏度。
3、SCA介导的胆碱能神经元胞吐过程中单囊泡ACh释放的定量与动力学分析
接下来利用M@E@CF纳米传感器研究ACh的动态释放。通过rAAV-GFP标记精确定位胆碱能神经元后,通过高钾溶液刺激并施加+0.4 V电位进行SCA检测。
对来自25个神经元的1439个囊泡释放事件的定量分析显示,每个囊泡释放的ACh分子数为83,391±2812。结合SCA和IVIEC技术量化单个囊泡中ACh的储存量和释放量,与来自27个神经元的637个囊泡中储存的ACh分子数(215,281±8806)相比,MGE脑区初级胆碱能神经元的平均释放分数约为39%。
这一结果首次证明初级胆碱能神经元的ACh释放遵循亚量子释放模式。基于释放动力学,单囊泡ACh释放峰分为五类:简单峰、平台峰、上升峰、下降峰和重叠峰。通过开发的1D-CNN深度学习模型进行客观分类,发现平台/上升/下降峰的ACh释放量显著高于简单峰,主要归因于动力学参数t的上调,而I值相对稳定。
这一发现不仅揭示了动力学变化是影响单囊泡释放模式的关键因素,也凸显了在细胞胞吐事件背景下动力学研究的重要性(图3)。
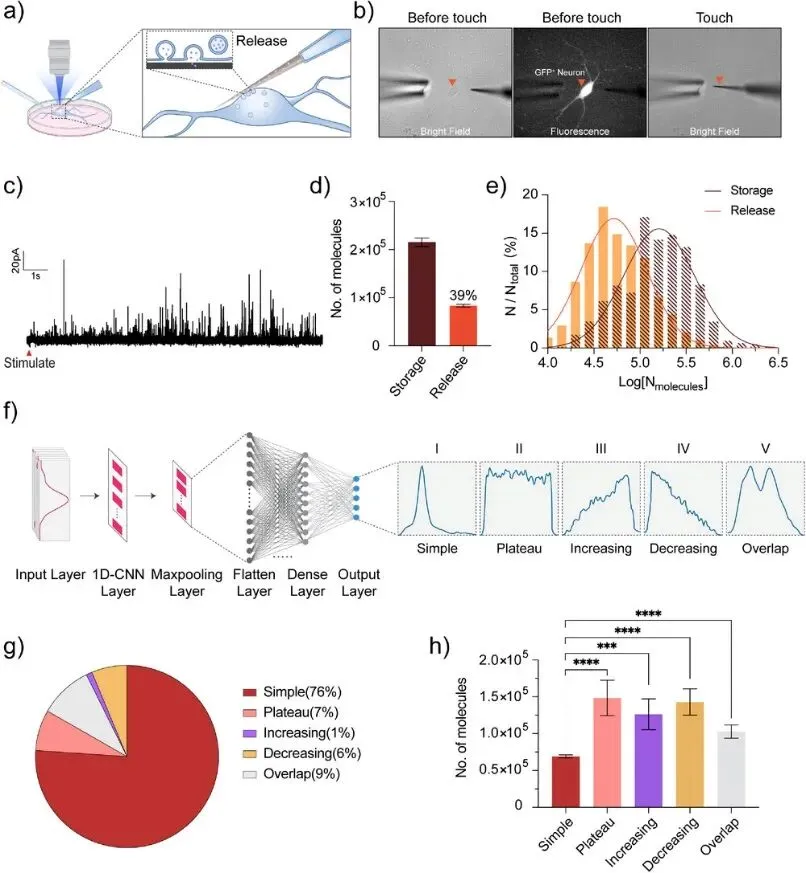
图3 高钾刺激下用SCA记录胞外释放,1439事件显示平均释放8.3万分子,释放分数约39%,首次证实ACh呈亚量子释放;1D-CNN将峰形分为五型,简单峰占76%,复杂峰释放量更高且t1/2更长。
4、人脊髓类器官中乙酰胆碱的储存与释放研究
进一步将这种M@E@CF纳米传感器方法应用于人类脊髓类器官,该类器官富含胆碱能运动神经元,从而研究单囊泡的储存与释放。
人类脊髓类器官在第18天表达KI67和TUJ1,而在第45天则表达ChAT、VAChT和TUJ1,证实了人类脊髓类器官的成功构建。
当将M@E@CF纳米传感器应用于检测人脊髓类器官中单个胆碱能神经元的ACh储存时,在微电极插入单个神经元胞体后观察到了连续的峰值信号。在与胆碱能转运体抑制剂HC-3孵育后,峰值强度显著降低;洗脱抑制剂后,峰值强度恢复。
在HC-3处理前,单个囊泡中的乙酰胆碱分子数为127,847±7332;HC-3处理后,该数值降至36,800±2532。清除抑制剂后,单个囊泡中的乙酰胆碱分子数恢复至75,470±5880。人脊髓类器官中单囊泡释放的ACh分子数为45,109±2933。相比之下,单囊泡中储存的ACh分子数为139,895±13352,释放分数约为32%。
应用深度学习模型显示,在人类脊髓类器官中,简单峰的比例为66%,平台峰占12%,上升峰占3%,下降峰占11%。复杂峰(平台型、上升型和下降型)释放的乙酰胆碱分子数量显著高于简单峰。
基于这些发现,推测单囊泡释放过程中的动力学变化可能与神经退行性疾病及其他神经疾病的发生机制密切相关(图4)。
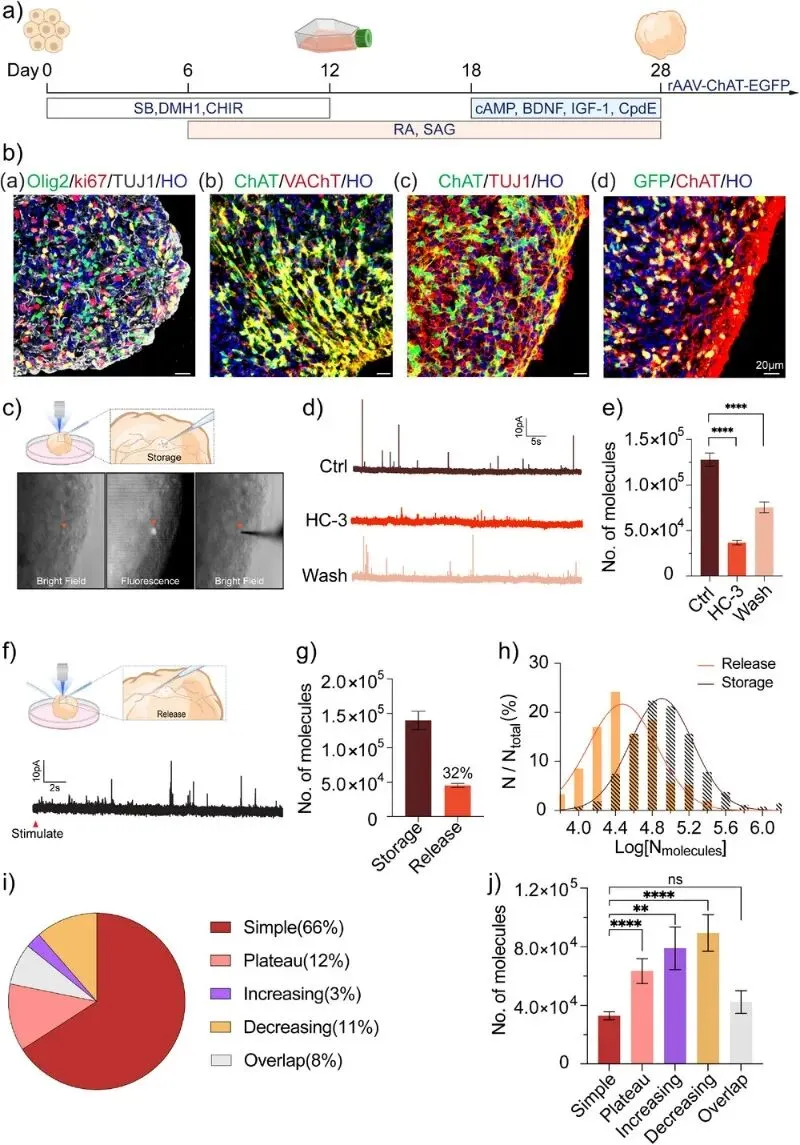
图4 人脊髓类器官ChAT+神经元IVIEC测得单囊泡ACh约12.8万分子,释放约4.5万分子,释放分数32%;1D-CNN同样识别五型分泌,复杂峰动力学参数显著增大,表明融合孔调控在人源细胞同样存在。
5、利用M@E@CF纳米传感器平台研究唐氏综合征胆碱能神经元中的乙酰胆碱储存与释放
应用M@E@CF纳米传感器对唐氏综合征(DS)模型小鼠的胆碱能神经元进行单囊泡分析。结果显示,与对照组相比,DS神经元囊泡内ACh储存量及单次释放量均显著降低,但释放比例反而升高。这表明神经元可能通过提高释放效率进行代偿。
动力学分析发现,DS神经元的ACh释放过程显著加速。机制上,ACh储存减少可能与ChAT蛋白表达下降有关;而释放动力学加速则可能与突触前SNARE蛋白(如STX1A、SNAP-25)表达下调导致的融合孔不稳定有关。
该研究首次在单囊泡水平揭示了DS胆碱能神经元的递质储存与释放缺陷,为理解其突触功能障碍提供了新视角。
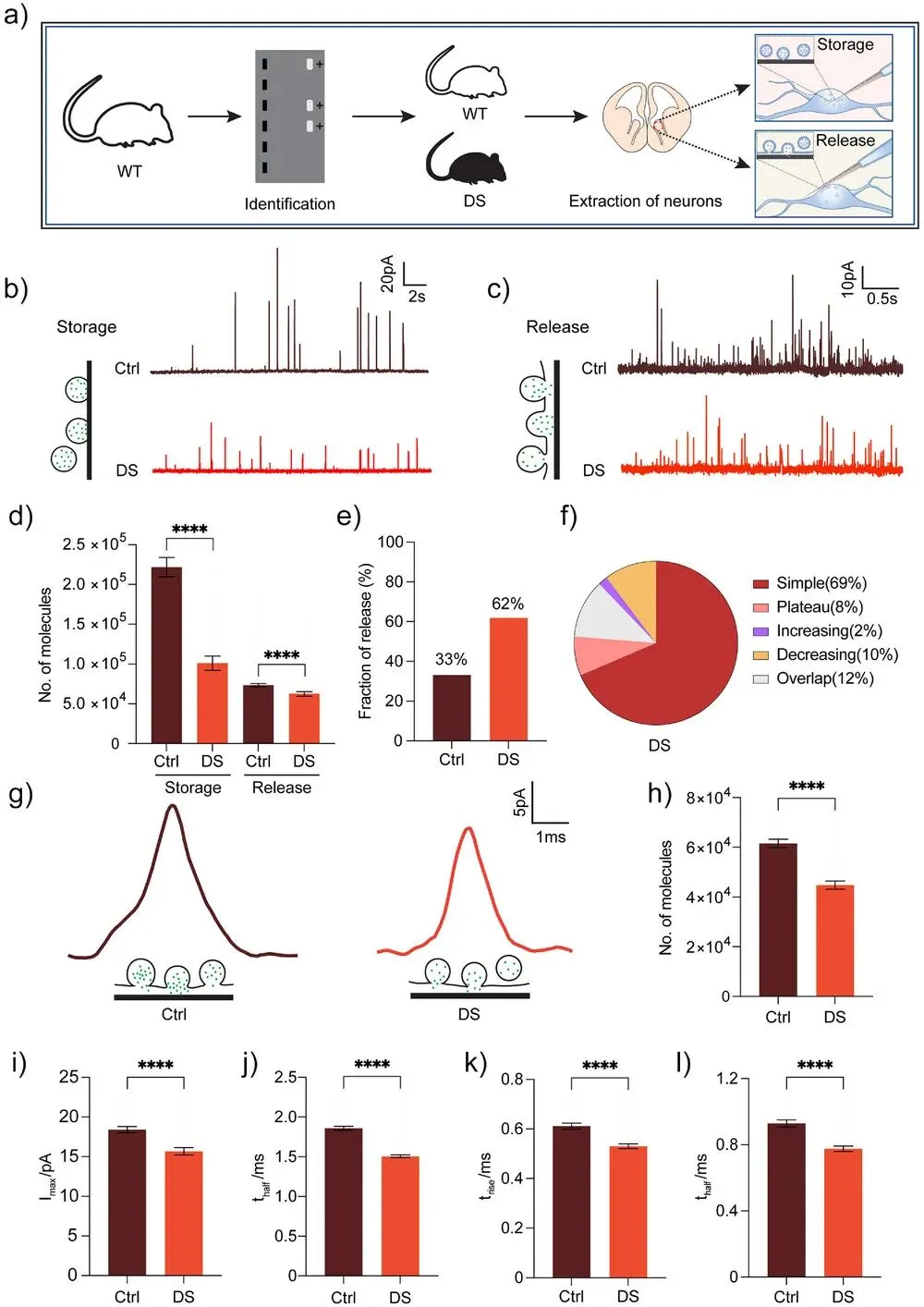
图5 唐氏综合征模型MGE神经元单囊泡ACh储存降至10万、释放降至6.2万分子,但释放比例升至62%;简单峰动力学参数t1/2、trise、tfall均显著缩短,Western显示ChAT与SNARE蛋白下调,提示合成与释放机制双重受损。
小结
该研究基于M@E@CF纳米传感器开发了一种高时空分辨率的电化学生物传感器,成功实现了在小鼠胆碱能神经元及人脊髓类器官中单细胞水平的ACh储存与胞吐的定量检测。
此外,自主研发的1D-CNN深度学习模型实现了对ACh胞吐模式的分类,揭示了具有显著差异的神经递质含量和动力学参数的释放模式。
这些发现表明,ACh胞吐受复杂的融合孔动力学调控。该方法应用于DS模型时,揭示了单囊泡ACh储存与释放的同时下调,这种下调通过释放分数的增加得以代偿,从而维持突触可塑性。
该技术不仅为探究胆碱能系统功能的分子机制提供了新颖的化学工具,而且从根本上加深了对ACh介导的突触可塑性调控的理解,为神经系统疾病机制研究和药物发现开辟了新途径。
参考文献
Zhu W, Zhang Y, Yu H, Wang D, Zhang X, Du X, Wu S, Li B, Zhang Y, Xin H, Guo X, Liu Y. A Novel Acetylcholine Nanosensor for Single Vesicle Storage and Sub-Quantal Exocytosis in Living Neurons and Organoids. Angew Chem Int Ed Engl. 2026 Jan 10:e20854. doi: 10.1002/anie.202520854.
“

”
添加客服小助理,获取原文PDF
往期推荐







