
背景介绍:砷元素在历史上扮演了双刃剑的角色,既曾被用作药物与颜料,又以其毒性闻名。现代科学中,含砷-碳键的有机砷化合物在药物开发(如抗癌药)、催化剂配体及功能材料等领域具有独特价值。然而,传统合成方法高度依赖剧毒的无机砷试剂(如三氧化二砷),且通常涉及多步骤反应和敏感的金属有机试剂,步骤繁琐、官能团耐受性差且极具危险性,严重限制了有机砷化合物的广泛应用。因此,迫切需要开发一种更安全、高效且可持续的合成新策略,直接利用自然界的砷资源构建有机砷化合物。
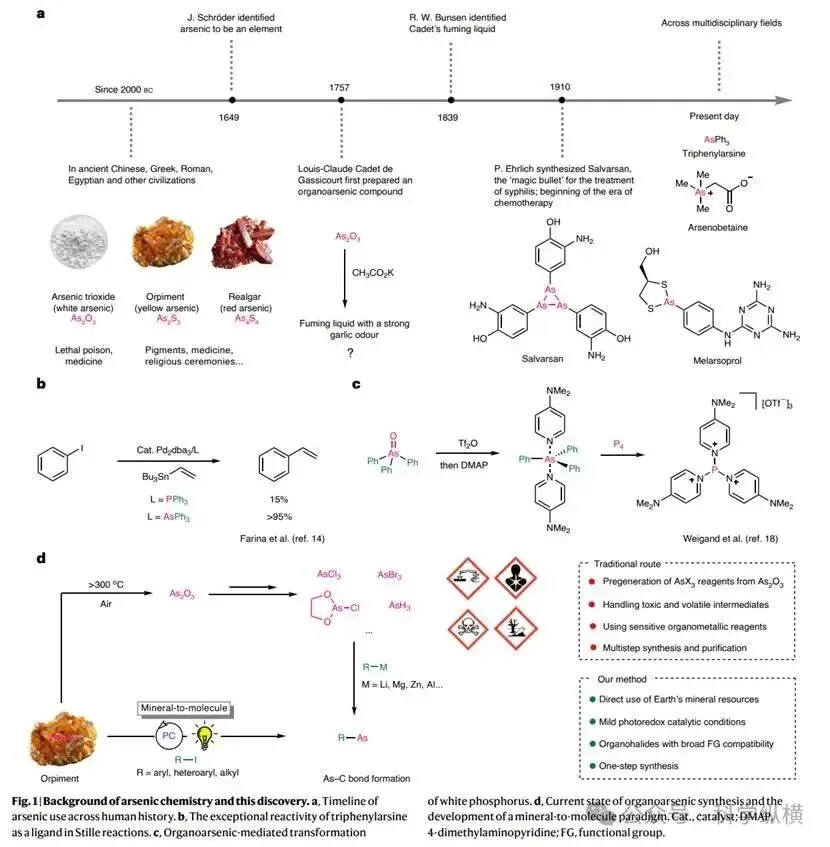
研究思路:受自然界生物体通过光甲基化作用将无机砷转化为有机砷的启发,本研究提出了一种创新的“矿物至分子”合成范式。核心思路是利用可见光驱动的光氧化还原催化,将天然存在的低毒性砷硫化物矿物(主要是雌黄,As₂S₃)直接转化为各类有机砷化合物。该策略旨在绕开所有有毒的砷中间体,通过与有机碘化物反应,一步构建官能团化的有机砷,从而实现合成过程的绿色化、安全化与原子经济性。
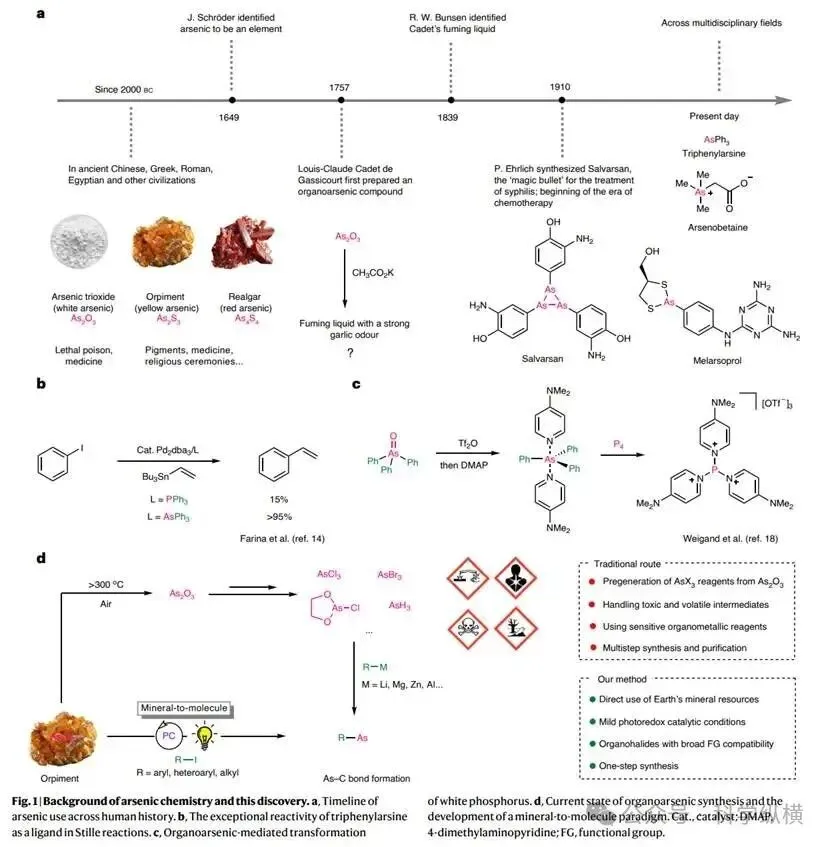
条件优化:研究团队以雌黄和碘苯为模型底物,对反应条件进行了系统优化。结果表明,在蓝光照射下,使用铱光催化剂PC3和三乙胺作为添加剂,在混合溶剂(Et₃N:PhH:MeCN)中于45°C反应,能以最佳产率获得目标产物三苯基胂。优化过程确认了几个关键因素:反应严格依赖于C-I键,溴苯或氯苯无效;三乙胺不可或缺;矿物形态至关重要,雌黄效果最好,而单质砷或三氧化二砷则几乎不反应;反应对氧气浓度、溶剂含水量等条件变化不敏感,展现出良好的操作稳定性。
底物拓展:该反应展现出广泛的底物适用性。对于芳基和杂芳基碘化物,无论是带有给电子基团(如甲基、甲氧基)、吸电子基团(如酯基、氰基、三氟甲基),还是卤素(氟、氯、溴)的底物,都能顺利转化为相应的三芳基胂或三杂芳基胂。研究还成功将反应拓展至烷基碘化物,在稍作调整的条件下,可以高效合成烷基取代的胂硫化物,并能兼容芳香环、环烷基、醚、卤素及噻吩等多种结构单元。然而,二级和三级烷基碘化物在该体系中不反应。
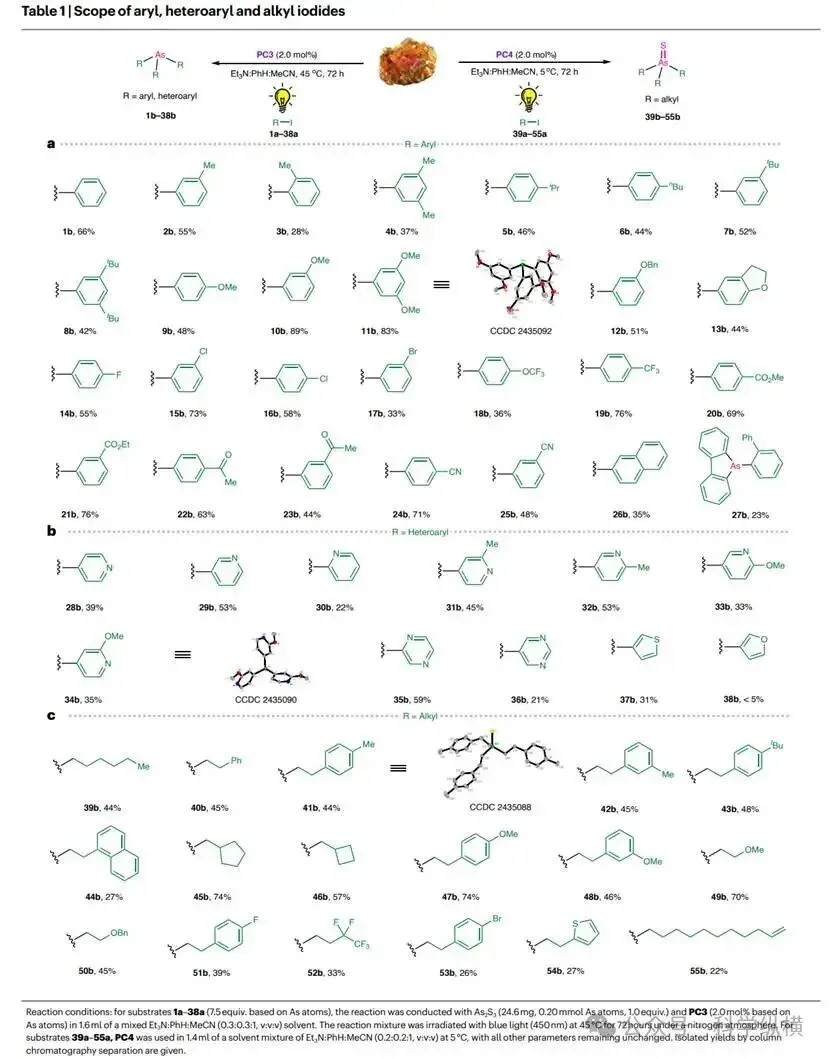
应用研究:该方法具有良好的合成应用潜力。反应可进行克级规模放大而不显著降低产率。所得有机砷产物可方便地进行后续转化,例如氧化为胂氧化物、季铵盐化合成鎓盐前体、制备砷锂试剂用于进一步的碳-砷键构筑等。这些有机砷化合物可作为配体,方便地与铑、铱、钌等金属络合,形成潜在的催化体系。此外,该方法为安全合成含砷功能材料(如砷基金属有机框架的前体)提供了更优路径,避免了使用剧毒试剂(如AsCl₃)的风险。
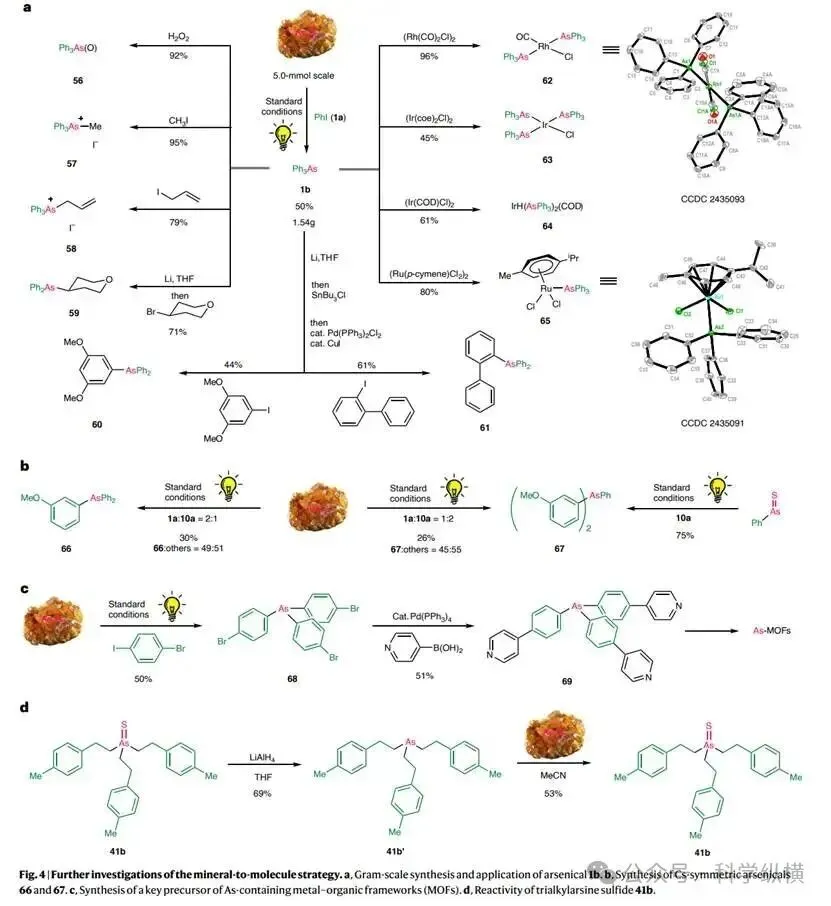
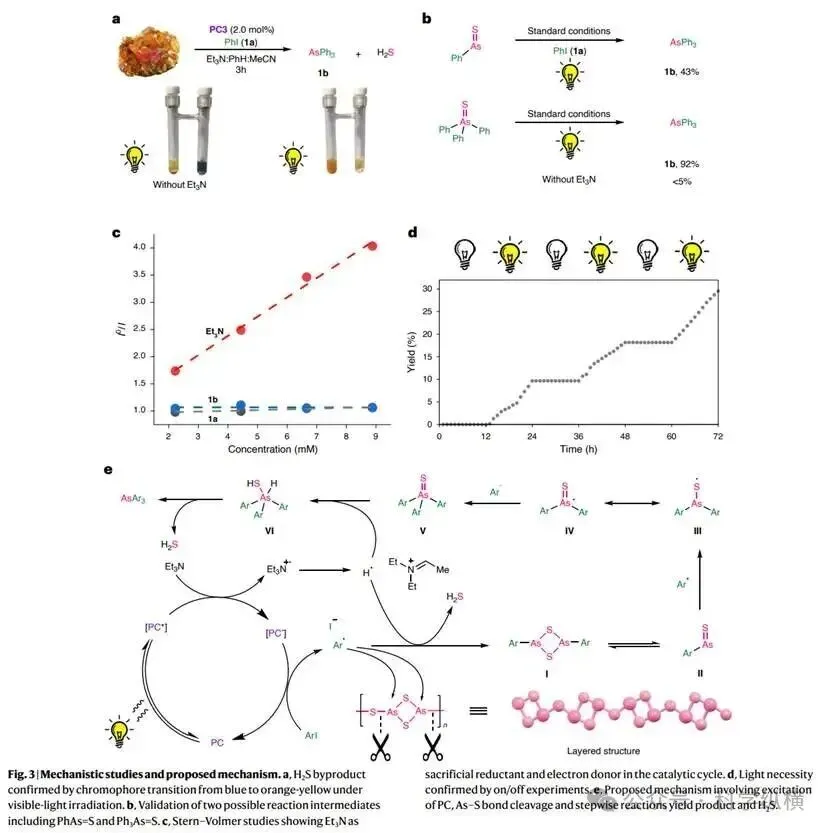
机理研究:通过一系列机理实验,研究人员阐明了反应的可能路径。关键证据包括:使用H₂S响应型显色剂证实反应过程中有H₂S副产物生成;验证了苯基胂硫化物(PhAs=S)作为关键中间体的可行性;荧光淬灭实验表明激发态光催化剂优先被三乙胺淬灭。基于此,提出了详细的催化循环:三乙胺作为牺牲还原剂和电子供体,在光催化剂作用下,芳基碘化物被还原产生芳基自由基。芳基自由基选择性进攻雌黄矿物中较长的As-S键,引发一系列砷-硫键的断裂、自由基重组和砷中心的逐步官能团化,最终形成三芳基胂并释放H₂S。
总结:本工作开创性地利用光氧化还原催化技术,实现了从天然雌黄矿物到高价值有机砷化合物的直接、一步法合成。该方法彻底摒弃了传统工艺中的剧毒砷中间体,反应条件温和,底物范围宽广,官能团兼容性好,且所有原料均商业可得,具有出色的实用性与可扩展性。这项“矿物至分子”的范式不仅为有机砷化学提供了一条安全、可持续的新道路,也为如何将地球矿物资源直接转化为功能分子建立了战略蓝图。
文献详情:
- 作者: Yandong Wang, Chengzhi Ge, Frank Glorius, Zhuangzhi Shi
- 题目: Mineral-to-molecule arsenic transfer via photoredox catalysis
- 期刊: Nature Chemistry
- DOI: 10.1038/s41557-026-02064-2