科研 |南京大学:体重指数和腰臀比的蛋白质组学特征及其在糖尿病发病中的作用(国人佳作)
 点击蓝字“蛋白质组”,轻松关注不迷路
点击蓝字“蛋白质组”,轻松关注不迷路

生科云网址:https://www.bioincloud.tech/
编译:微科盟,编辑:微科盟Emma、江舜尧。
微科盟原创微文,欢迎转发转载。
导读
目前人们尚不清楚腹部脂肪分布的血浆蛋白质组与体重指数(BMI)的差异有多大,以及这种差异是否具有临床意义。我们通过比较BMI和腰臀比(WHR)血浆蛋白质组学特征的差异,探讨BMI和WHR特异性蛋白质与糖尿病发病的关系。研究对象为4203名无糖尿病史的受试者(年龄57.2±6.0岁,男性37.8%)。我们采用PROSEEK邻近延伸法检测136例患者的血浆蛋白。我们使用基于两步迭代的重采样方法优化内部的可重复性,然后进行β系数比较,在基线时确定体重指数和腰臀比特异的蛋白质。我们通过Cox比例风险回归分析研究与糖尿病发病的关系。本研究的主要观察指标是平均随访20.3±5.9年所发生的糖尿病事件。我们剔除21个与BMI和WHR无显著相关性的重叠蛋白后,发现10个具有内部重复性的蛋白具有BMI特异性,22个具有WHR特异性 (调整后的错误发现率p<0.05)。在WHR特异性蛋白中,18个经过多因素调整后仍与糖尿病风险相关,而没有一种BMI特异性蛋白显示与糖尿病风险相关。腹部脂肪分布与血浆蛋白质组的一些独特特征有关,这些特征可能与肥胖以外的糖尿病风险有关。
原名:Proteomic Profiles of Body Mass Index and Waist-to-Hip Ratio and their Role in Incidence of Diabetes译名:体重指数和腰臀比的蛋白质组学特征及其在糖尿病发病中的作用期刊:The Journal of Clinical Endocrinology & Metabolism通讯作者:徐标 & Gunnar Engström
通讯作者单位:南京大学医学院附属鼓楼医院心脏科 & 瑞典马尔默大学临床科学系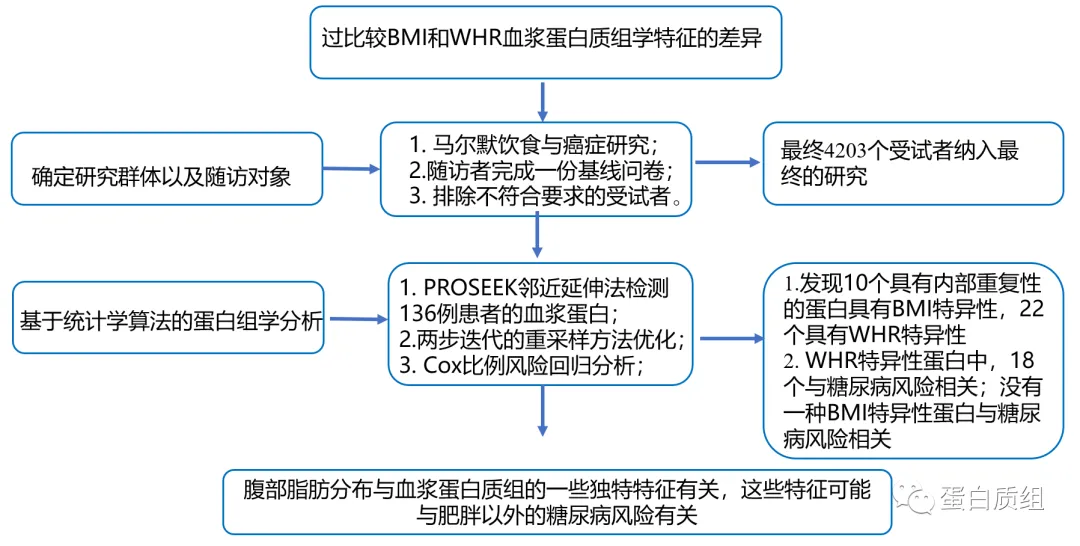
本研究共纳入4203人,平均年龄为57.2±6.0岁,其中男性占37.8%。男性的BMI为25.8±3.2kg/m2,女性为25.2±4.0kg/m2;男性的WHR为0.94±0.06,女性为0.78±0.05。BMI与WHR呈中度相关(男性r=0.58,p<0.0001;女性r=0.35,p<0.0001)。补充资料显示了参与者不同BMI与WHR四分位数的基线特征。WHR随着饮酒的增加而增加,而BMI随着年龄的增长而增加,随着吸烟而下降。其他心脏代谢危险因素在BMI或WHR四分位数中显示出类似的增加趋势(p<0.0001)。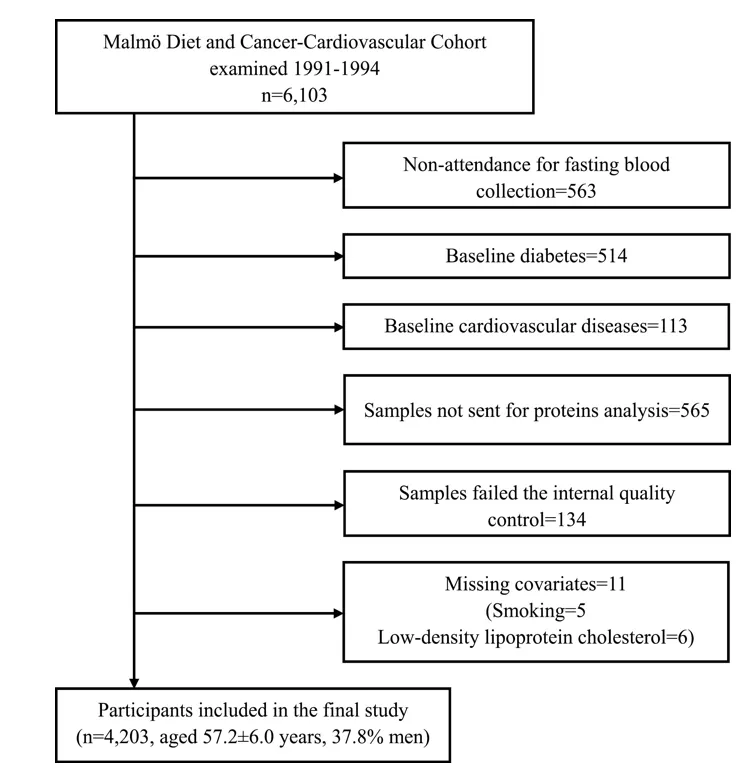
经过平均20.3年±5.9年的随访,其中619名参与者发展为糖尿病。如表1所示,WHR和糖尿病之间的关联比BMI和糖尿病之间的关联相对更强。BMI和WHR每改变1个标准差,调整后的风险率(HR)分别为1.31(95%CI 1.22~1.42,p<0.0001)和1.52(95%CI 1.33~1.72,p<0.0001)。表1 糖尿病发病率与BMI或WHR的性别四分位数相关(n=4203)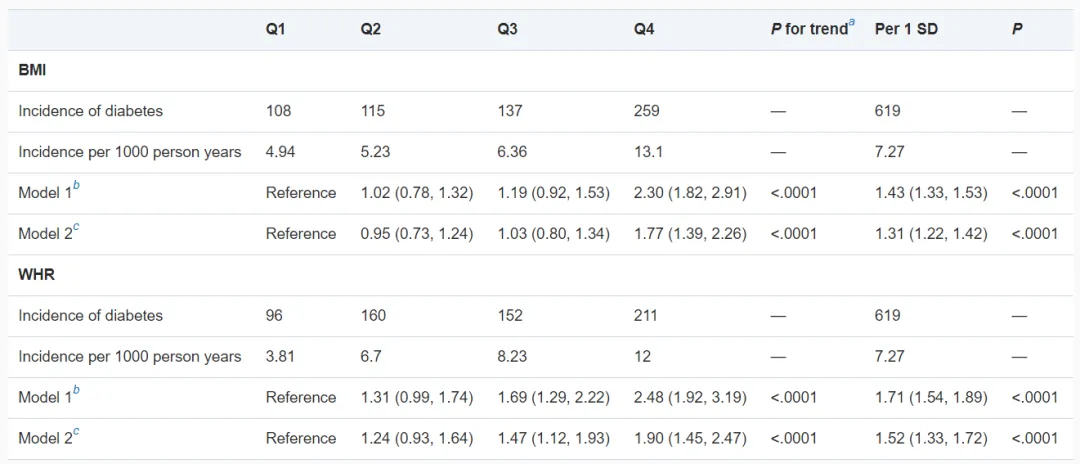
BMI,身体质量指数;SD,标准偏差;WHR,腰臀比。†根据年龄、性别、吸烟、高酒精消耗量、收缩压、低密度脂蛋白和抗高血压药物调整的危险比率(95%CI)。在应用两步迭代的重采样方法(TSIR)之前,血浆蛋白分别与BMI和WHR之间的关系,以及BMI和WHR之间的相互调整分别体现在补充材料中。我们通过TSIR法确定了59个和45个内部重复的血浆蛋白,并分别与BMI或WHR相关,其中包括21个重叠蛋白。其中38个蛋白质与BMI有关,但与WHR无关;24个蛋白质与WHR率有关,但与BMI无关。如表2所示,在这些蛋白质中,F检验证实有10种是BMI特异的,其中3种与BMI呈正相关。此外,22种蛋白被鉴定为WHR的特异性蛋白,除了原癌基因酪氨酸蛋白激酶Src外,所有这些蛋白都显示出正相关。表2 特定于BMI或WHR的内部重复性蛋白(n=4203)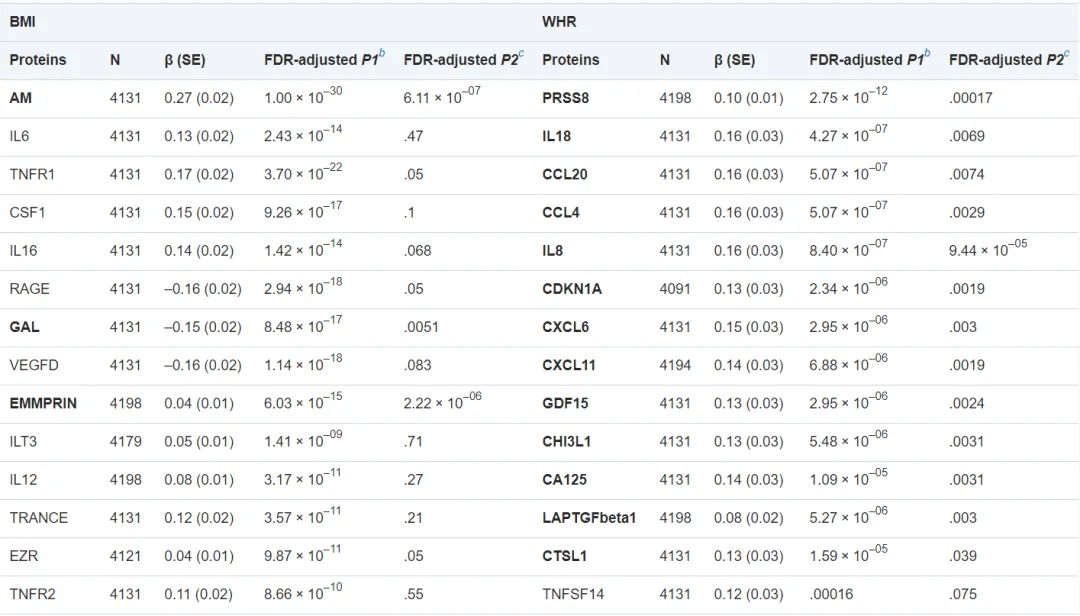
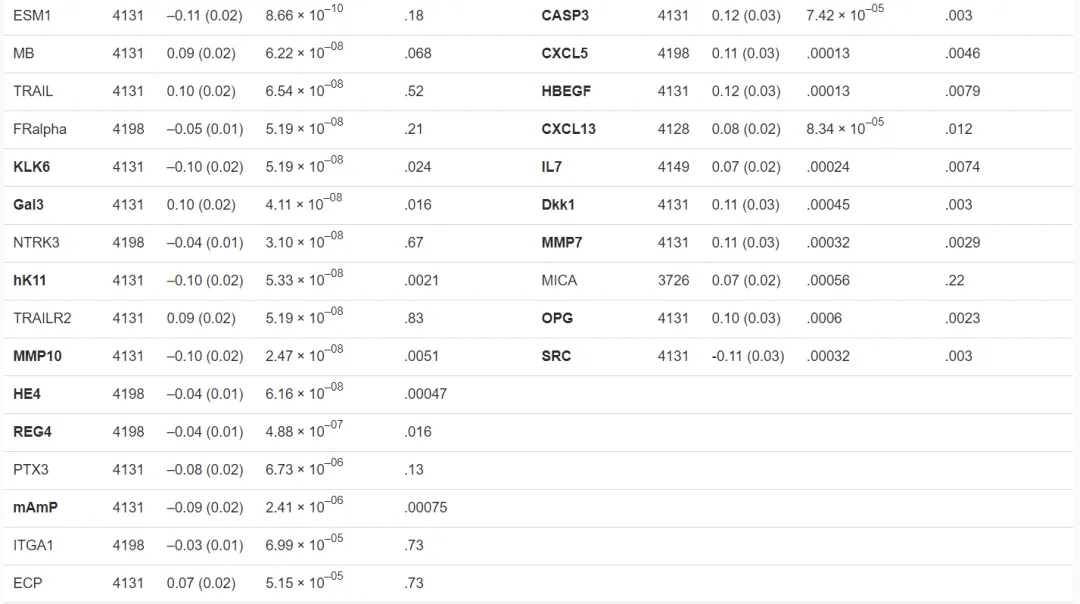
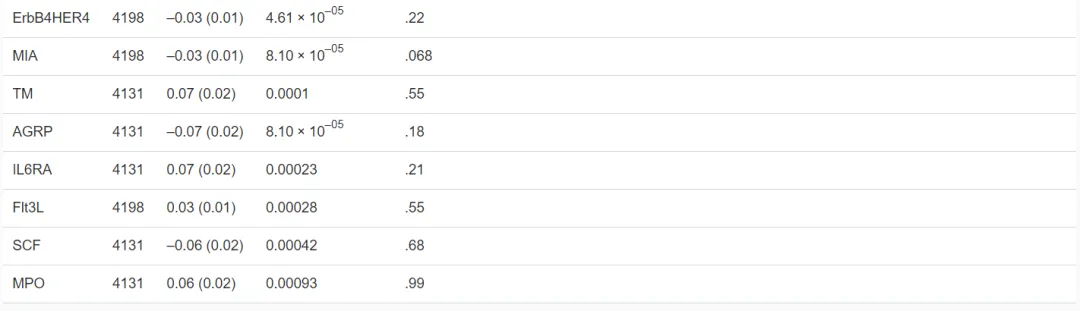
AgRP,Agouti相关蛋白;AM,肾上腺髓质素;BMI,体重指数;CA125,卵巢癌相关肿瘤标志物CA 125;CASP3,半胱氨酸蛋白酶-3;CCL20,C-C基序趋化因子20;CCL4,C-C基序趋化因子4;CDKN1A,细胞周期蛋白依赖性激酶抑制因子1;CHI3L1,几丁质酶-3样蛋白1;CSF1,巨噬细胞集落刺激因子1;CTSL1,组织蛋白酶L1;CXCL11,C-X-C基序趋化因子11;CX13,C-X-C基序趋化因子13;CCL5,C-X-C基序趋化因子5;CX6,C-X-C基序趋化因子6;Dkk1,Dickkopf相关蛋白1;ECP,嗜酸性粒细胞阳离子蛋白;EMMPRIN,细胞外基质金属蛋白酶诱导物;ErbB4HER4,受体酪氨酸蛋白激酶erB-4;ESM1,内皮细胞特异性分子1;EZR,埃兹蛋白;FDR,错误发现率;Flt3L,FMS样酪氨酸激酶3配体;FRAlpha,叶酸受体;GAL,甘丙肽;Gal3,半乳糖凝集素-3;GDF15,生长/分化因子15;HBEGF,肝素结合性表皮生长因子; HEE4,附睾分泌蛋白E4;hK11,激肽释放酶-11;IL-12,白介素12;IL-16,白介素16;IL-18,白介素18;IL6,白介素6;IL6RA,白介素6受体亚单位α;IL7,白介素7;IL8,白介素8;ILT3,免疫球蛋白样转录因子3;ITGA1,整合素α-1;KLK6,激肽释放酶-6;MAMP,膜结合氨基肽酶P;MB,肌红蛋白;MIA,黑色素瘤衍生的生长调节蛋白;MICA,MHC I类多肽相关序列A;MMP10,基质金属蛋白酶-10;MMP7,基质金属蛋白酶-7;MPO,髓过氧化物酶;NTRK3,NT-3生长因子受体;OPG,骨保护素;PRSS8,前列腺素;PTX3,五角蛋白相关蛋白PTX3;RAGE,晚期糖基化终产物受体;REG4,再生胰岛衍生蛋白4;SCF,干细胞因子;SE,标准误差;SRC,原癌基因酪氨酸蛋白激酶Src;TM,血栓调节蛋白;TNFR1,肿瘤坏死因子受体1;TNFR2,肿瘤坏死因子受体2;TNFSF14,肿瘤坏死因子配体超家族成员14;TRAIL,肿瘤坏死因子相关的凋亡诱导配体和受体2;TRAILR2,肿瘤坏死因子相关的凋亡诱导配体和受体2;TRANCE,肿瘤坏死因子相关的细胞因子;VEGFD,血管内皮生长因子D;WHR,腰臀比。
*表示蛋白质与BMI相关。BMI或WHR特异性蛋白质以粗体突出显示。†BMI或WHR的线性回归在同一模型中相互调整,并校正了年龄、性别、吸烟、高饮酒量、收缩压、低密度脂蛋白和降压药物等因素。本研究以FDR调整后的p<0.05为截断点。‡采用F检验比较β系数所反映的BMI或WHR绝对值在多变量线性回归中是否有显著差异。以FDR调整后的p<0.05作为截断点。我们通过正交筛选,发现所有BMI特异性蛋白之间显示出弱到中等的相关性(最大Spearman相关性|r|=0.61)。在WHR特异性蛋白中,肝素结合的EGF样生长因子和细胞周期蛋白依赖性激酶抑制物1分别与Dickkopf相关蛋白1(DKK1,r=0.82)和半胱氨酸蛋白酶-3(r=0.83)高度相关,且在TSIR方法中与WHR相关的次数更多。根据蛋白互作网络分析(PPI)分析,WHR特异蛋白的最重要模块包括9个节点和68个边(模块1)。所包含的基因都是那些编码趋化因子、趋化因子受体或白介素类的基因。我们观察到与BMI特异性蛋白对应的基因之间的相互作用相对松散。与WHR特异性蛋白相对应的基因主要集中在细胞外空间、趋化因子活性、细胞-细胞信号、趋化因子介导的信号通路、炎症反应和中性粒细胞趋化。与BMI特异蛋白相对应的基因主要集中在细胞外空间、丝氨酸型内肽酶活性和蛋白分解。KEGG途径富集分析表明,与WHR特异蛋白对应的基因主要参与细胞因子-细胞因子受体的相互作用。然而,我们没有发现显著丰富的BMI特异性蛋白的KEGG通路。在与肥胖和胰岛素抵抗高度相关的组织中,脂肪组织是大多数BMI或WHR特异性蛋白质的主要产生场所。不同转录产物的表达水平在皮下脂肪和内脏脂肪之间可能有很大差异。与皮下脂肪相比,那些编码已知炎症蛋白的蛋白更有可能在内脏脂肪中表达(例如CCL4、CCL20、CXCL8、IL18和CXCL6),而编码的蛋白(例如C-C基序趋化因子4和20[CCL4、CCL20]、白细胞介素8和18[IL8、IL18]和C-X-C基序趋化因子6[CXCL6])往往是WHR特有的蛋白质。4. BMI和WHR特异性蛋白与糖尿病发病率的关系如表3所示,在10种BMI特异性蛋白中,只有两种(即肾上腺髓质素和半乳糖凝集素-3)在调整潜在混杂因素后与糖尿病的风险增加相关(模型1)。在对WHR进行额外调整后,我们发现没有一个相关性仍然显著。值得注意的是,在模型1中,22个WHR特异蛋白中有19个与糖尿病正相关。增加的BMI作为协变量对相关性的影响很小。我们观察到18种蛋白质的显著HR(模型2)。在敏感性分析中,我们在执行了更严格的错误风险率(FDR)校正(包括136次多次测试)后,蛋白质与糖尿病的相关性的重要性与模型2中的总体一致。在模型2中仍然显著的蛋白质在火山图中用红色标记。在蛋白质水平和糖尿病风险之间的相关性中,没有统计学意义的性别差异(交互作用的P值均>0.05)。表3 BMI或WHR特异的蛋白与糖尿病发病率的相关性(n=4203)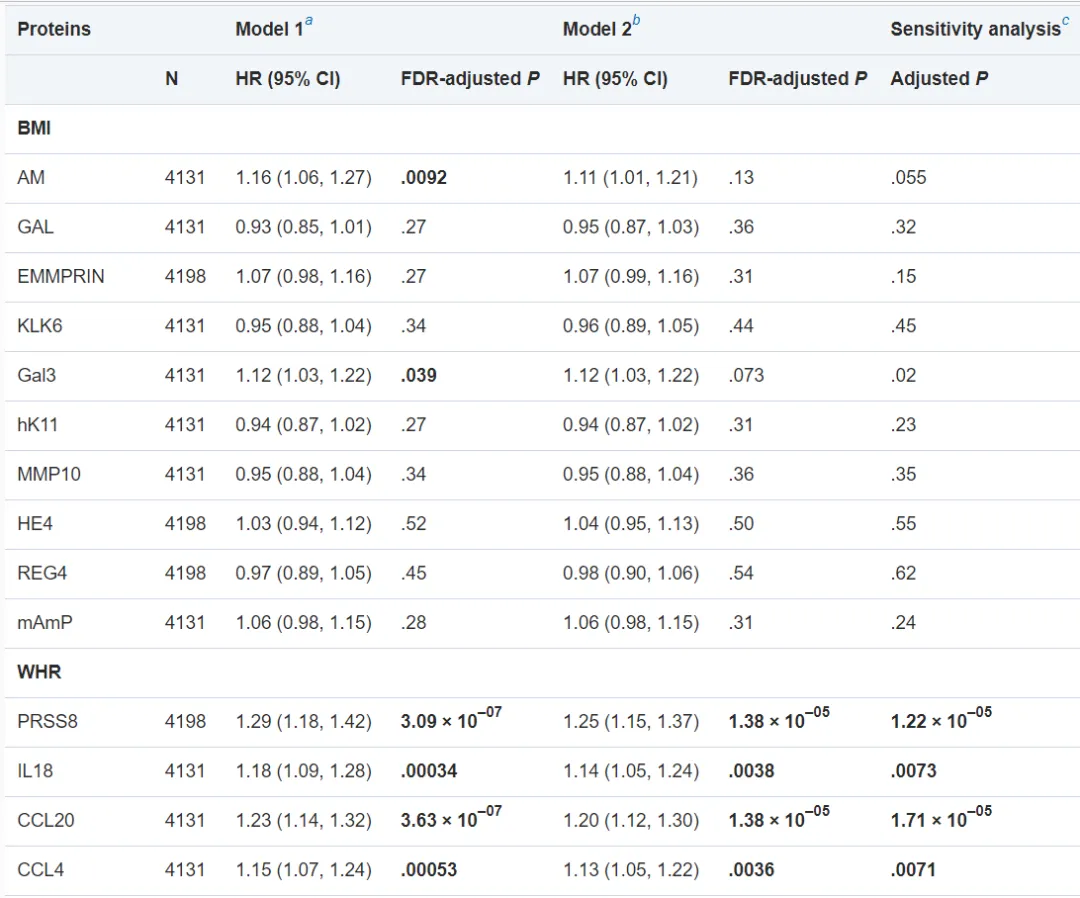
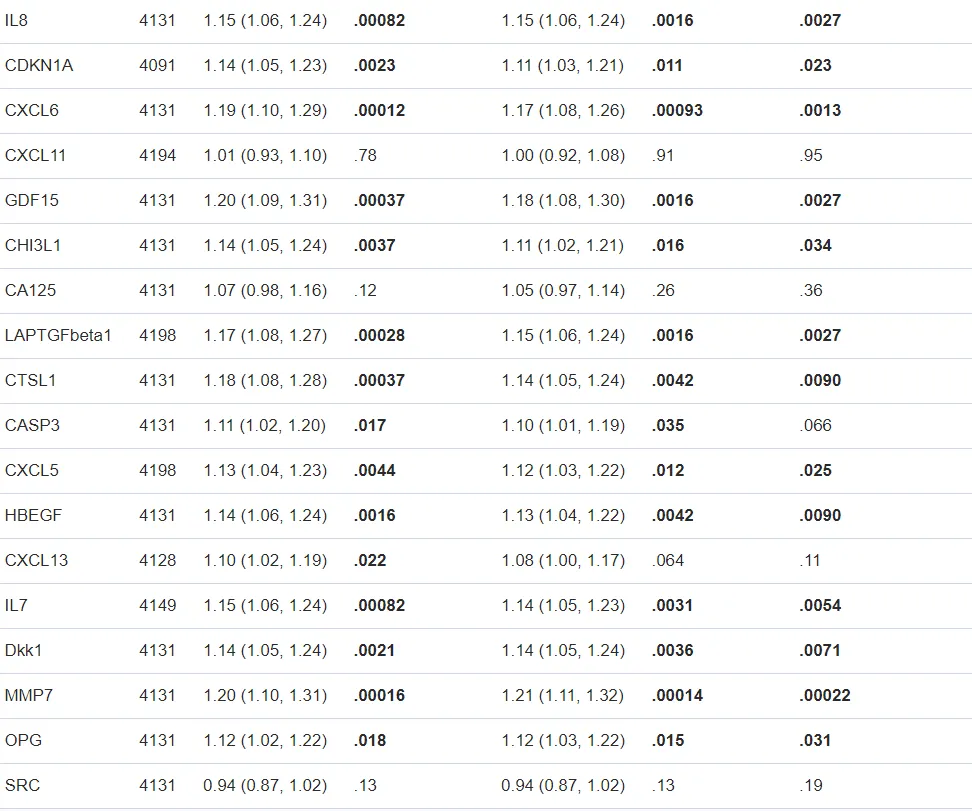
AgRP,Agouti相关蛋白;AM,肾上腺髓质素;BMI,体重指数;CA125,卵巢癌相关肿瘤标志物CA 125;CASP3,半胱氨酸蛋白酶-3;CCL20,C-C基序趋化因子20;CCL4,C-C基序趋化因子4;CDKN1A,细胞周期蛋白依赖性激酶抑制因子1;CHI3L1,几丁质酶-3样蛋白1;CSF1,巨噬细胞集落刺激因子1;CTSL1,组织蛋白酶L1;CXCL11,C-X-C基序趋化因子11;CX13,C-X-C基序趋化因子13;CCL5,C-X-C基序趋化因子5;CX6,C-X-C基序趋化因子6;Dkk1,Dickkopf相关蛋白1;ECP,嗜酸性粒细胞阳离子蛋白;EMMPRIN,细胞外基质金属蛋白酶诱导物;ErbB4HER4,受体酪氨酸蛋白激酶erB-4;ESM1,内皮细胞特异性分子1;EZR,埃兹蛋白;FDR,错误发现率;Flt3L,FMS样酪氨酸激酶3配体;FRAlpha,叶酸受体;GAL,甘丙肽;Gal3,半乳糖凝集素-3;GDF15,生长/分化因子15;HBEGF,肝素结合性表皮生长因子; HEE4,附睾分泌蛋白E4;hK11,激肽释放酶-11;IL-12,白介素12;IL-16,白介素16;IL-18,白介素18;IL6,白介素6;IL6RA,白介素6受体亚单位α;IL7,白介素7;IL8,白介素8;ILT3,免疫球蛋白样转录因子3;ITGA1,整合素α-1;KLK6,激肽释放酶-6;MAMP,膜结合氨基肽酶P;MB,肌红蛋白;MIA,黑色素瘤衍生的生长调节蛋白;MICA,MHC I类多肽相关序列A;MMP10,基质金属蛋白酶-10;MMP7,基质金属蛋白酶-7;MPO,髓过氧化物酶;NTRK3,NT-3生长因子受体;OPG,骨保护素;PRSS8,前列腺素;PTX3,五角蛋白相关蛋白PTX3;RAGE,晚期糖基化终产物受体;REG4,再生胰岛衍生蛋白4;SCF,干细胞因子;SE,标准误差;SRC,原癌基因酪氨酸蛋白激酶Src;TM,血栓调节蛋白;TNFR1,肿瘤坏死因子受体1;TNFR2,肿瘤坏死因子受体2;TNFSF14,肿瘤坏死因子配体超家族成员14;TRAIL,肿瘤坏死因子相关的凋亡诱导配体和受体2;TRAILR2,肿瘤坏死因子相关的凋亡诱导配体和受体2;TRANCE,肿瘤坏死因子相关的细胞因子;VEGFD,血管内皮生长因子D;WHR,腰臀比。
*表示蛋白质与BMI相关。BMI或WHR特异性蛋白质以粗体突出显示。†BMI或WHR的线性回归在同一模型中相互调整,并校正了年龄、性别、吸烟、高饮酒量、收缩压、低密度脂蛋白和降压药物等因素。以FDR调整后的p<0.05为截断点。‡采用F检验比较β系数所反映的BMI或WHR绝对值在多变量线性回归中是否有显著差异。以FDR调整后的p<0.05作为截断点。目前的观察性研究已经确定了分别与BMI或WHR相关的血浆蛋白。WHR特异性蛋白,与糖尿病风险的增加呈正相关。从蛋白质组学的角度,我们首次证明,与一般肥胖相比,腹部脂肪分布可能具有一些独特的病理特征,这可能解释了它具有增加糖尿病风险的能力。此前,其他几项研究已经将蛋白质组学与肥胖联系起来。Ferreira等人使用生物统计学方法确定肥胖的判别蛋白质生物标志物(BMI≥为30 kg/m2)。Folkersen等人使用孟德尔随机化分析,发现了几种蛋白质与BMI或WHR相关的因果证据。此外,Pang等人也提出了自己的观点。他们报道称,只有部分与BMI相关的蛋白可以预测心血管疾病的风险。然而,这些研究中都没有聚焦于不同肥胖测量方法的独特蛋白质组学特征及其在糖尿病中的作用。在我们的研究中,WHR与BMI只有中等程度的相关性。同时,与以前的观察结果一致的是,WHR与 BMI对糖尿病的预测互不影响,我们清楚地发现WHR与肥胖相关风险的不同和独特方面,这与BMI不同。以前的全基因组关联研究(GWAS)已经揭示了BMI和WHR的不同遗传基础。此外几项研究表明,BMI和身体脂肪分布与循环蛋白质的联系不同。通常只有少数几个研究良好的蛋白质被研究过,如脂联素、C反应蛋白、白介素6和肿瘤坏死因子α。与以前的研究不同,我们主要关注BMI或WHR特异的蛋白质。我们还研究了更广泛的蛋白质谱,并采用了TSIR方法来确保识别出的蛋白质的内部重复性。更重要的是,我们进一步调查了已识别的蛋白质是否可以驱动不同的代谢风险,这在以前还没有被探索过。在我们的TSIR方法中,我们发现与BMI和WHR相关的蛋白质之间有显著的重叠。大多数重叠蛋白是与BMI呈正相关的顶级蛋白(例如瘦素[LEP]、脂肪酸结合蛋白、脂肪细胞[FABP4]和IL1受体拮抗剂蛋白[IL1ra])或WHR(例如组织蛋白酶D[CTSD]、CCL3、组织型纤溶酶原激活物[tPA])。LEP和FABP4是脂肪细胞生物学中公认的脂肪因子。已知IL1ra和CCL3与肥胖相关的炎症有关。CTSD是一种溶酶体天冬氨酸蛋白酶,可被体重增加激活,导致脂肪细胞死亡。作为一种丝氨酸蛋白酶,TPA水平在肥胖中也会增加,这可能是由于对肥胖相关代谢应激引起的纤维蛋白溶解系统的代偿反应。BMI和WHR仍然有一些蛋白质组特征,这并不令人惊讶,因为它们都能衡量肥胖。然而,肥胖也是一种异质性疾病。在本研究中,BMI和WHR都有各自独特的蛋白质。大多数这些蛋白质主要在脂肪组织中表达,但在皮下和内脏脂肪中的表达水平不同。这表明,BMI和WHR的差异性蛋白质谱部分原因可能是由于内脏脂肪和皮下脂肪中蛋白质表达的差异。BMI和WHR特异的蛋白质似乎参与了不同的生物过程。我们的结果表明,蛋白降解是与BMI特异性蛋白相关的主要生物学过程。BMI特异性蛋白主要是蛋白水解酶(如激肽释放酶-6、激肽释放酶-11、基质金属蛋白酶[MMP10]和膜结合氨基肽酶P)或对蛋白分解活性有重要调节作用的蛋白(如细胞外基质金属蛋白酶诱导物和附睾分泌蛋白E4)。与这一发现一致的是,先前的数据表明,肥胖症患者的蛋白分解系统(如泛素-蛋白酶体系统和自噬)发生了变化,肥胖症患者的蛋白分解增加可能与肌肉分解代谢等结局有关。相反,WHR特异性蛋白主要参与细胞-细胞信号、趋化因子活性以及炎症和免疫反应。与在PPI网络中观察到的BMI特异性蛋白之间的松散连接不同,WHR特异性蛋白似乎紧密联系在一起,趋化因子、趋化因子受体和白细胞介素2形成了最重要的模块。总而言之,这些结果支持了肥胖症中存在异质性这一结论。与BMI相比,高WHR更容易与炎症征兆同时发生。即使在多变量调整后,大多数WHR特异的蛋白仍然可以预测糖尿病的风险。据推测,WHR相关的炎症信号可能至少部分解释或反映了为什么WHR除了BMI外还会增加代谢风险。炎症是肥胖和糖尿病之间的关键联系。在预测糖尿病的WHR特异性蛋白中,已有几种蛋白已被证明与脂肪炎症和糖尿病相关的发病机制有关(IL18、IL8、CCL20、CCL4、CXCL6)。相反,生长/分化因子15的表达增加可能是一种抗炎的代偿机制,但不足以降低炎症相关的糖尿病风险。一些蛋白质可能参与了与脂肪生成或炎症相关的途径,如典型的Wnt-β-catenin途径(如Dkk1和MMP7)或其下游的转录因子,过氧化体增殖物激活的受体γ(如组织蛋白酶L1和骨保护素),它在调节炎症、脂肪生成、胰岛素合成和分泌以及胰腺β细胞增殖方面发挥关键作用。然而,我们观察到的关联可能具有因果关系,或者蛋白质升高可能只是反映了先前存在的炎症状态和糖尿病风险。相比之下,几乎没有任何一种BMI特异性蛋白可以预测糖尿病风险。一种可能的解释是,一些与BMI相关的蛋白质可能导致糖尿病风险,这些蛋白质是BMI和WHR所共有的(例如E-选择素)。此外,尽管一些糖尿病风险相关蛋白与BMI相关,而与WHR无关,但它们与BMI和WHR的相关性没有显著差异。这些蛋白质(如晚期糖基化终产物受体)仍然被排除在外,因为我们使用了相对严格的筛选策略,旨在聚焦于特定的蛋白质。本研究的优势包括前瞻性设计、高频率的长期随访和大量的蛋白质测定。此外,TSIR方法的采用显著提高了内部效度。然而,外部验证队列的缺乏是一个主要的限制,这使得我们无法直接将任何特定的蛋白质转化到临床环境中去。我们的研究还有其他几个需要考虑的局限性。首先,我们需要对已知或可能参与肿瘤或心血管疾病有关的蛋白进行靶向蛋白质组分析。因此,其他重要的蛋白质可能被遗漏了。其次,BMI和WHR均存在测量误差。尽管两者通常随着时间的推移而缓慢变化,但这些人体测量方法可能在长期随访期间发生了变化。第三,虽然我们在基线时排除了所有的糖尿病人群,并且绝大多数的糖尿病事件可以被假设为2型糖尿病,但仍有可能在成人患者中存在少数潜在的自身免疫性糖尿病患者。第四,尽管糖尿病在之前已经登记过,但不同时间段的登记使用了不同的参数,糖尿病发病率的定义也没有标准化。第五,分析不同蛋白质的样本量在3478到4198个受试者之间,这可能会限制蛋白质之间的直接比较。最后,由于流行病学设计的性质,即使我们在对潜在混杂因素进行广泛调整后,也不能排除残留混杂因素。综上所述,目前的研究表明,与一般肥胖相比,腹部脂肪分布携带一种独特的蛋白质组特征,有引起糖尿病发生的风险。这些发现可能有助于人们描述肥胖的特定代谢表型或风险机制,并提出更好的策略来预防与腹部脂肪分布相关的代谢紊乱。https://doi.org/10.1210/clinem/dgac140
《蛋白质组》是微科盟旗下专注于学术知识免费分享平台,内容主要包括分享蛋白组学最新文献,新闻,干货知识,视频课程和学术直播讲座。蛋白质组仅用于学术成果分享与交流,不涉及商业利益。
也严禁他人将本公众号的内容用于商业运营。 点击蓝字“蛋白质组”,轻松关注不迷路
点击蓝字“蛋白质组”,轻松关注不迷路