IF30.9!南京鼓楼医院团队七图荣登《Cell》子刊!“国自然”热点拿下双一区TOP!
- 2026-05-30 18:16:47
点击上方蓝字,了解更多精彩内容

脂肪组织与大脑之间存在着怎样的对话?为什么肥胖者明明体内leptin水平很高,却无法有效抑制食欲?南京鼓楼医院团队的研究揭示,脂肪细胞释放的“快递小囊”——细胞外囊泡,正是维持大脑对leptin敏感性的关键。当这一信号中断,便会导致leptin抵抗与体重失控。更值得关注的是,研究团队还开发出能精准递送“增敏”分子至中枢的工程化囊泡,为肥胖治疗提供了全新思路。
↓关注生信树,获取更多科研洞察↓
如果你也想用同款思路发文,快关注我们,私信进行咨询吧!


标题:脂肪细胞衍生的细胞外囊泡是中枢瘦素敏感性和能量稳态的关键调节因子
发表期刊:Cell Metabolism
发表时间:2026年1月6日
影响因子:30.9/Q1
肥胖,以脂肪组织中过量脂肪积累为特征,与代谢和心血管疾病风险显著增加以及寿命较短相关。然而,开发有效的肥胖管理干预策略仍然具有挑战性。
研究方法
本研究通过动物模型、测序及示踪技术发现,脂肪细胞囊泡携带特定miRNA靶向下丘脑,通过抑制瘦素信号负调控因子维持瘦素敏感性;利用工程化囊泡递送这些miRNA可逆转肥胖小鼠的瘦素抵抗。
👨🔬明确现象与因果关系:
首先通过构建脂肪组织特异性囊泡(Ad-EVs)分泌抑制的小鼠模型,观察其对能量代谢的影响,确立Ad-EVs在维持能量平衡中的必要性。
📝验证功能与作用路径:
将正常小鼠来源的Ad-EVs输注给肥胖小鼠,验证其抗肥胖效果;
同时通过给瘦素缺陷(ob/ob)和瘦素受体缺陷(db/db)小鼠输注Ad-EVs,证实其作用是依赖于完整的瘦素信号通路。
🔎追踪机制与分子靶点:
利用荧光示踪技术定位Ad-EVs在中枢神经系统的靶向区域(如下丘脑ARC核团);
并通过小RNA测序对比正常与肥胖状态下的囊泡内容物,筛选出差异表达的miRNA;
接着,通过分子生物学实验验证这些miRNA直接靶向瘦素信号的负调控因子(如SOCS3、PIAS3)。
🧬干预转化与应用验证:
基于发现的靶向膜蛋白(SIRPα和MCAM),设计并改造工程化囊泡,使其携带特定的增敏miRNA,并通过静脉注射实现中枢神经系统的精准递送,最终在肥胖小鼠模型中验证其逆转瘦素抵抗和减轻体重的治疗效果。
你也想尝试这方面的选题?你也想get同款数据库,却不知道该如何下手?不要再犹豫了,快来联系生信树团队!我们为你提供专业的团队服务,数据分析,思路设计统统不再是问题!
研究结果

0
1
AT-EVs调节能量平衡
为了确定AT-EVs是否在能量稳态中发挥假设作用,我们通过向Cas9转基因小鼠的脂肪组织中注射携带针对Rab27小指导RNA(gRNA)的AAVs,建立了脂肪组织特异性的Rab27敲除(Rab27 KO)小鼠模型。Rab27是一种对小囊泡分泌至关重要的小型GTP酶(图1A)。
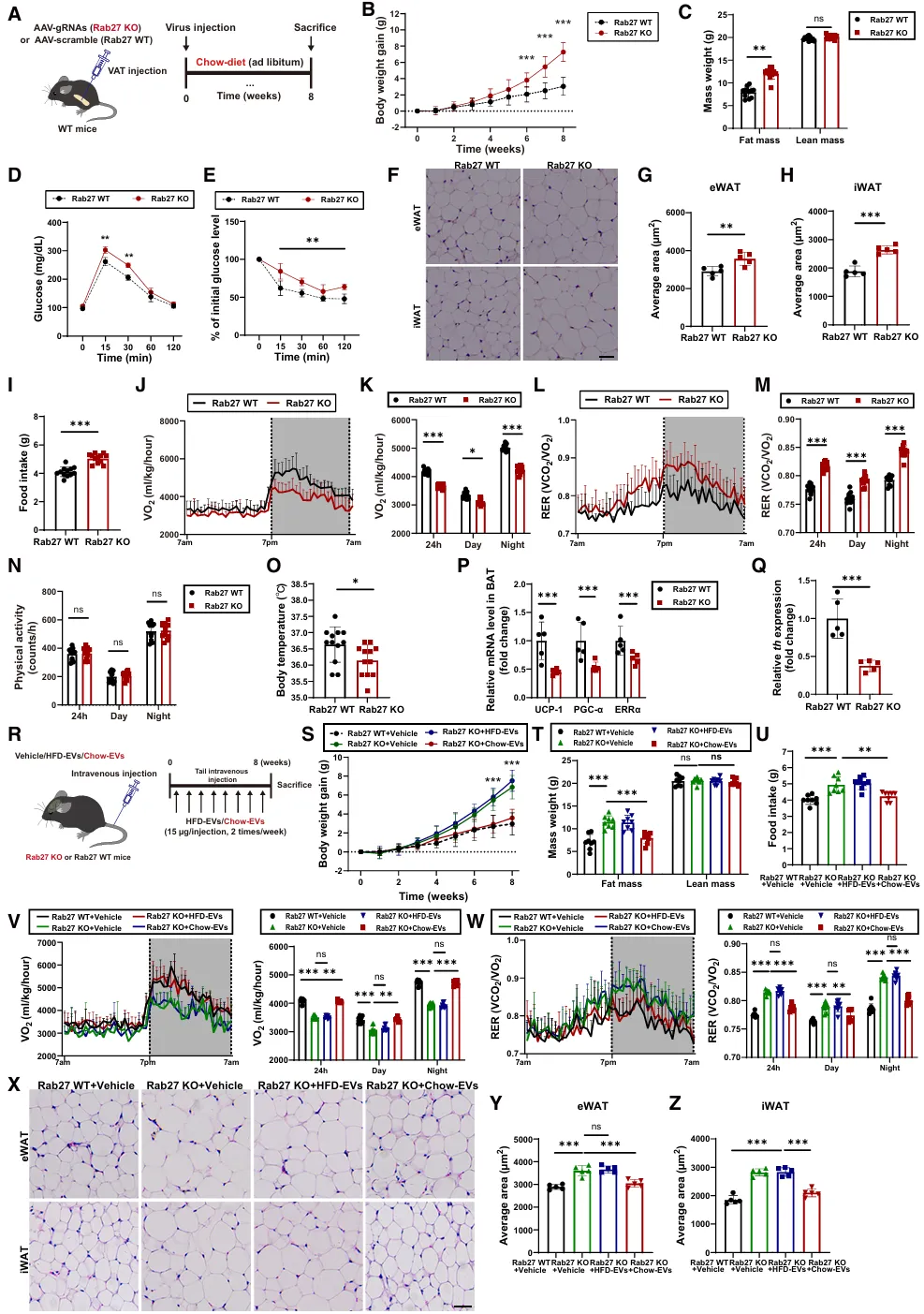
图1 特异性抑制AT-EVs会导致能量平衡受损
与Rab27野生型小鼠相比,Rab27敲除小鼠在普通饲料喂养条件下表现出体重和脂肪质量显著增加,而瘦体重没有变化(图1B和1C)。
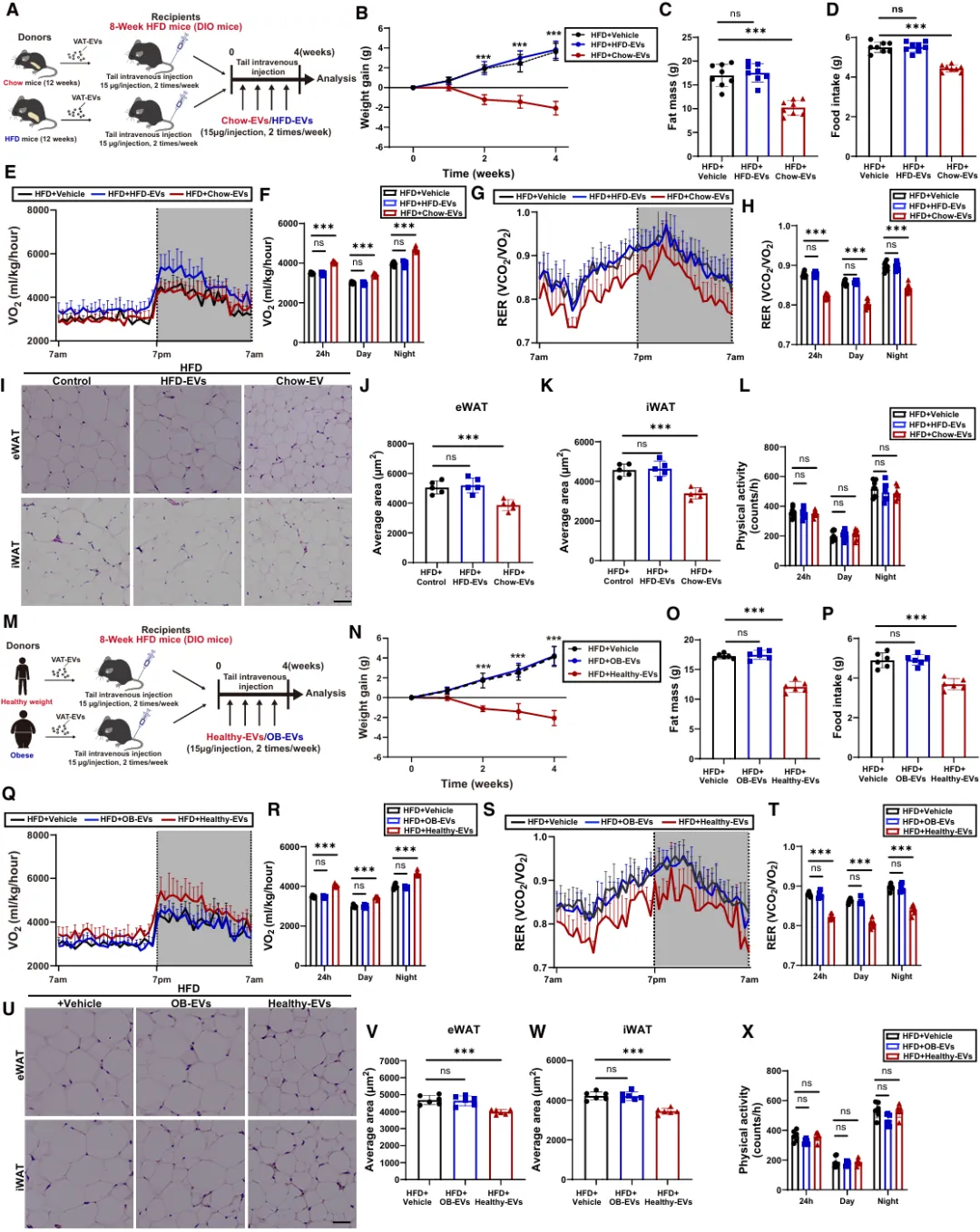
图2 健康的EVs可以减轻肥胖
此外,为了确定其对肥胖的潜在影响,对DIO小鼠进行了静脉注射喂食EVs或高脂饮食EVs(图2A)。
0
2
AT-EVs 对调节下丘脑瘦素-黑色素皮质素信号通路至关重要
我们研究了AT-EVs在瘦素相关效应机制中的作用。我们观察到,在禁食和再喂食状态下,Rab27 KO小鼠和Rab27 WT小鼠的WAT瘦素基因表达及血浆瘦素水平没有差异(图3A和3B)。
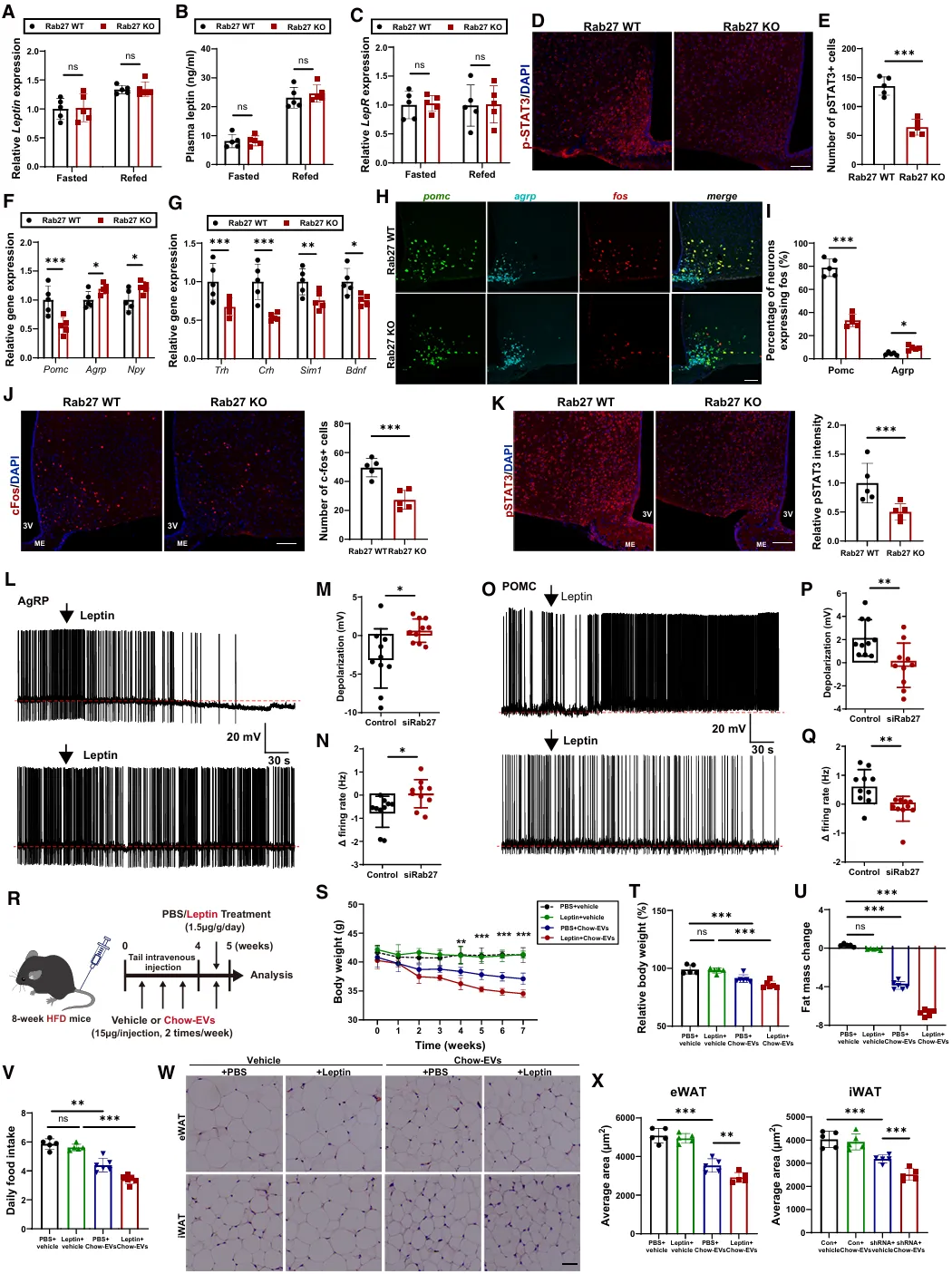
图3 AT-EVs 对调节下丘脑瘦素-黑色素皮质素信号通路至关重要
鉴于瘦素对能量平衡的调节作用主要是通过下丘脑LepR神经元介导的,我们评估了AT-EVs对中枢瘦素信号的调节作用。在禁食和再喂食条件下,Rab27 KO小鼠与Rab27 WT小鼠在下丘脑LepR基因表达上未观察到差异(图3C)。
0
3
脂肪组织来源的外泌体通过直接作用于下丘脑瘦素-黑色素皮质素回路来调节能量稳态
为了确定AT-EVs是否可以直接作用于下丘脑,我们使用了一种脂肪特异性的EV追踪方法。首先,通过向CD63FlagEGFP-mCherryf/f小鼠的脂肪组织中注射表达Cre重组酶的AAV进行体内AT-EV追踪和筛选(图4A)。
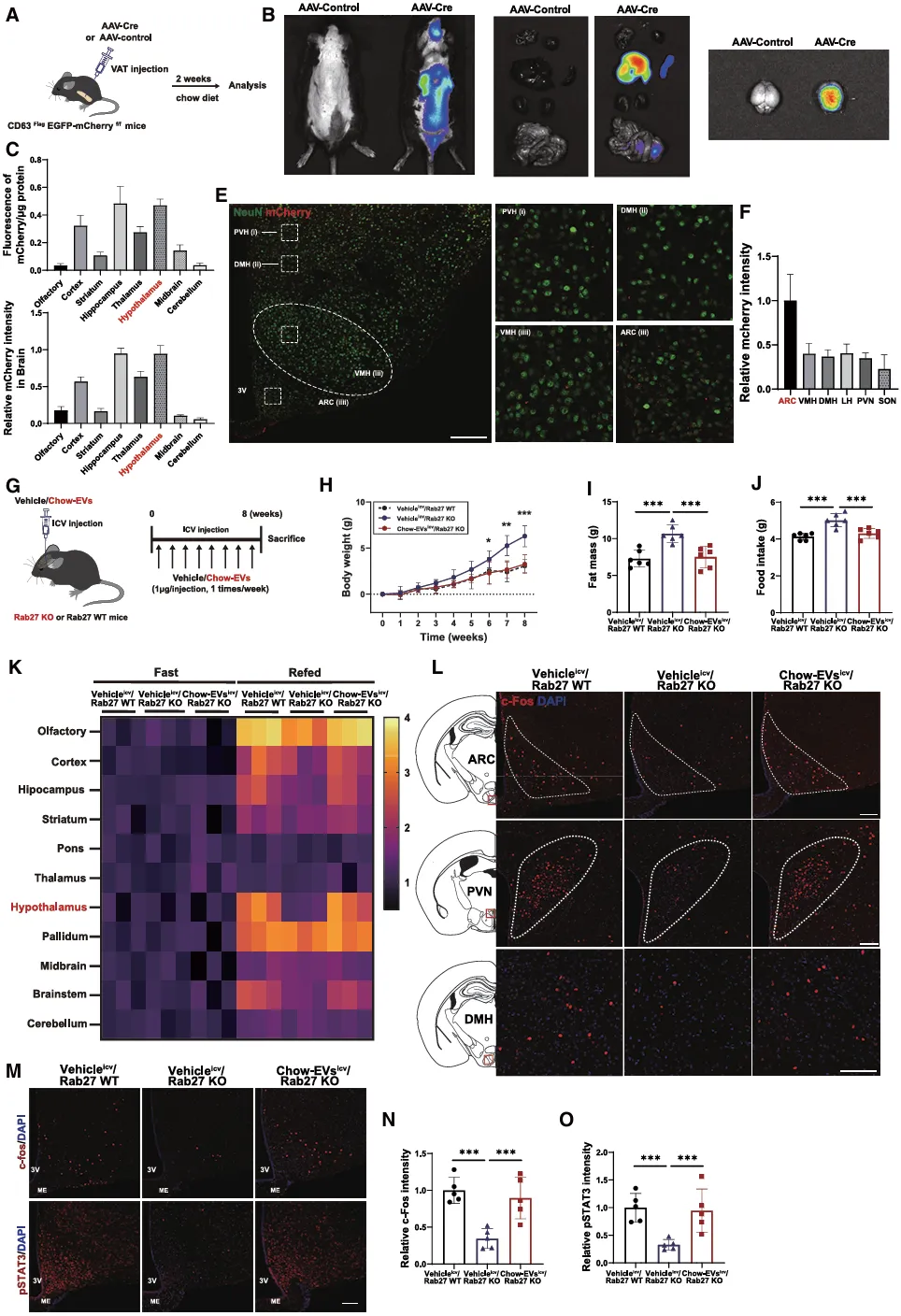
图4 AT-EVs直接作用于中枢神经系统以调节能量稳态
这些小鼠在经过修饰的CD63蛋白上游携带了floxp-floxp终止密码子,CD63是一种在EV膜中丰富存在的蛋白。AAV注射4周后,我们分析了不同器官的荧光强度,并观察到大脑中mCherry荧光显著积累(图4B)。
从AAV-siDicer、AAV随机对照或对照小鼠提取的AT-EVs通过静脉注射方式给予饮食诱导肥胖小鼠(图5A–5C)。
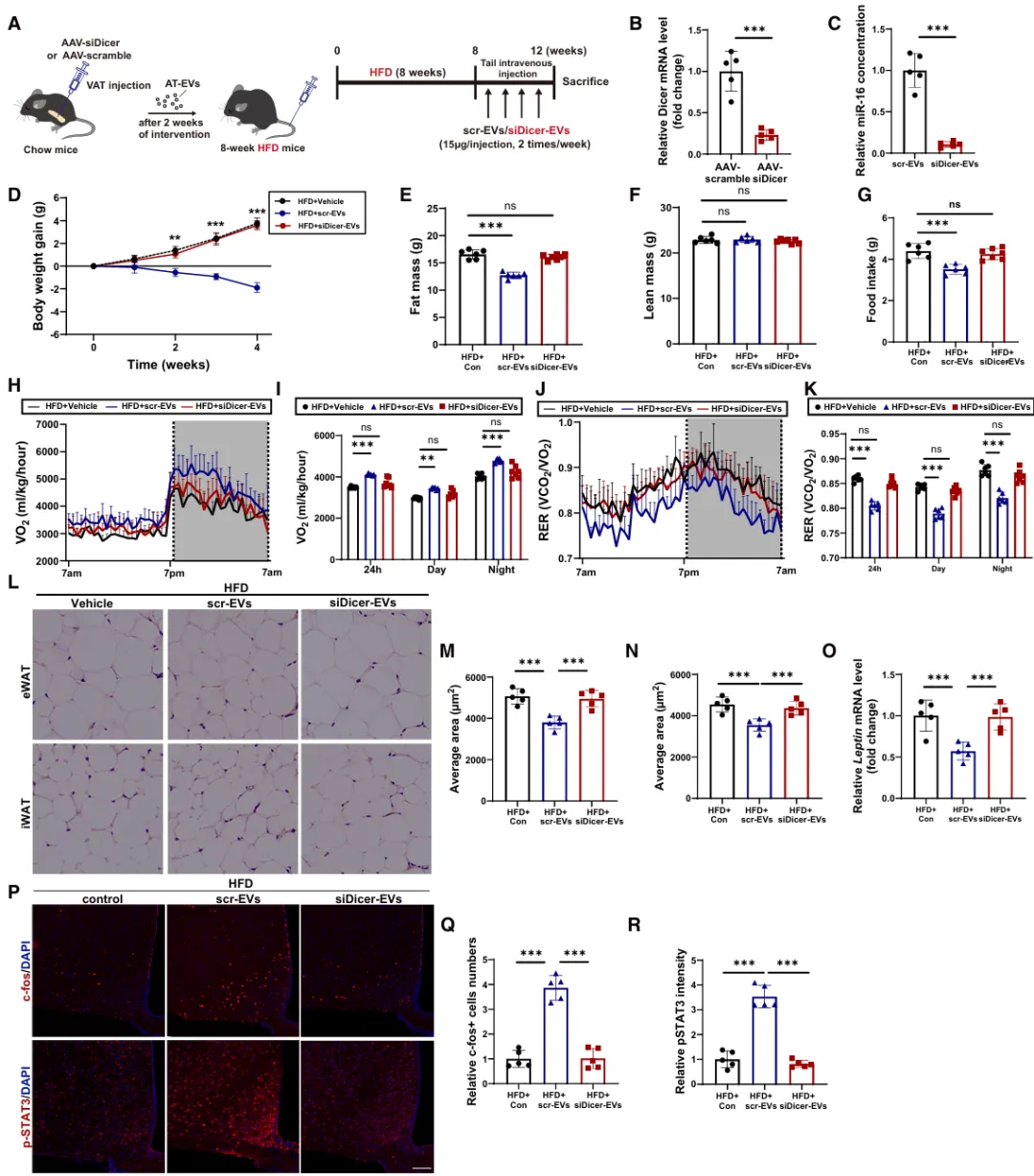
图5 miRNAs促进AT-EVs在调节能量稳态中的作用
在SiDicer-EV处理组和载体处理的DIO小鼠之间,没有观察到体重、脂肪量、每日摄食量、能量消耗、脂肪细胞大小或瘦素mRNA水平的差异(图5D–5O)。
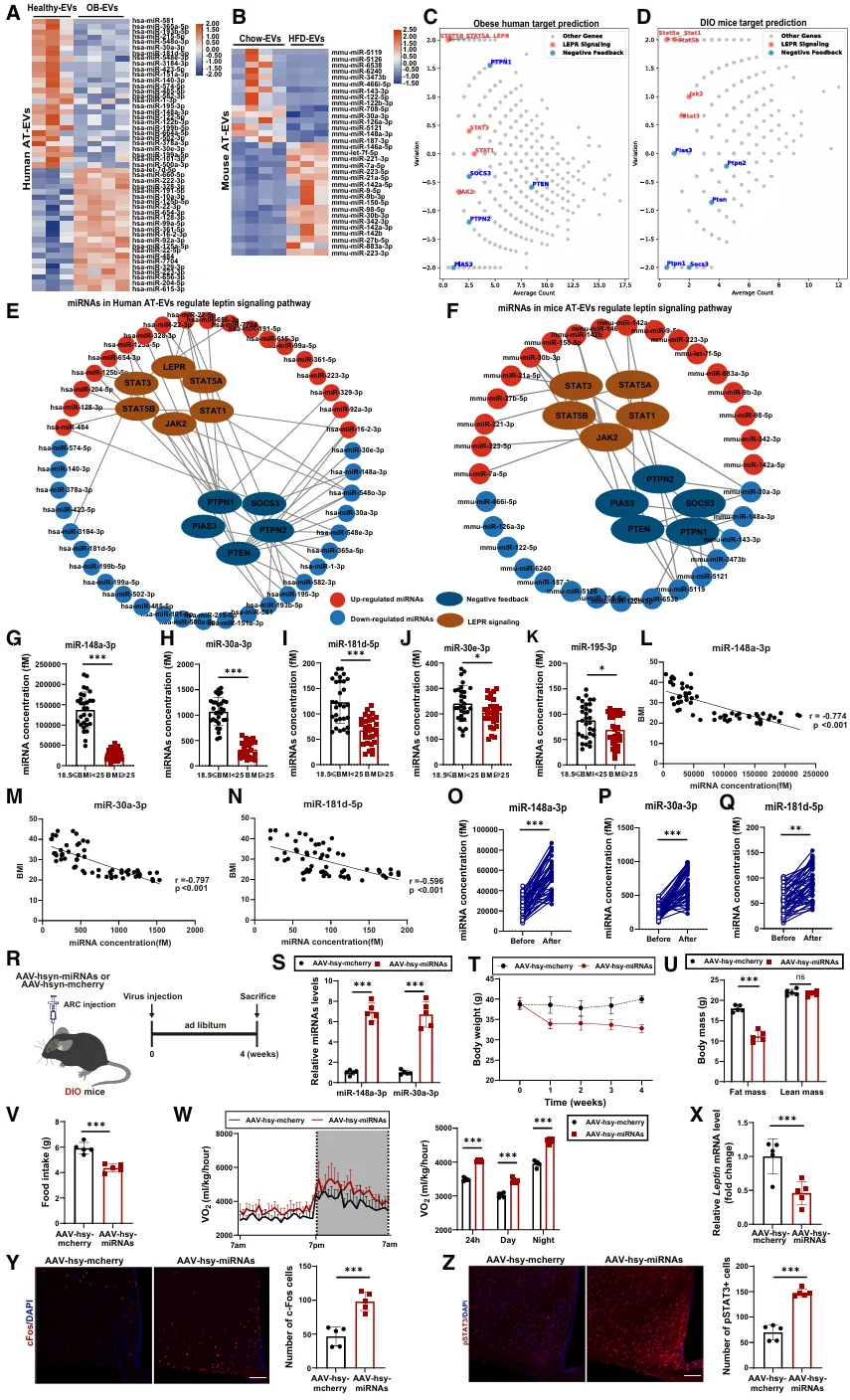
图6 miRNA文件在健康EV中富集,作为瘦素增敏剂
为了识别在AT-EVs中负责瘦素敏感化的miRNAs,使用深度RNA测序分析了健康EVs和OB-EVs中的miRNA谱。与健康EVs相比,OB-EVs中有28种miRNAs下调,19种miRNAs上调(图6A)。
为了开发具有增强中枢神经系统靶向能力的工程化EV,将3T3-L1细胞转染了携带编码SIRPα和MCAM的质粒的慢病毒或其对照,并从分化的LV-SM转染3T3-L1脂肪细胞或LV-control转染3T3-L1脂肪细胞中提纯EVs(图7A)。
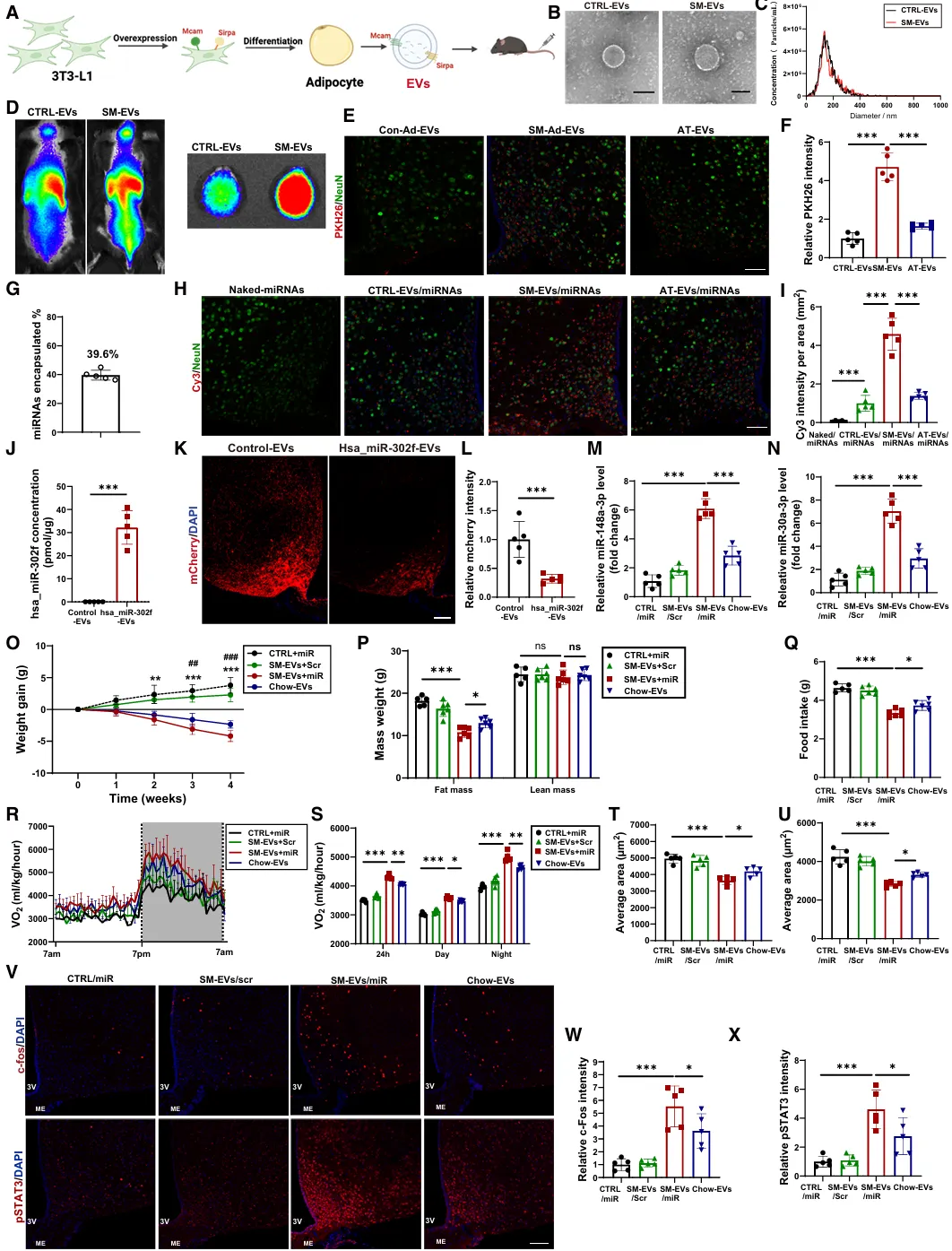
图7 使用工程化外泌体靶向中枢神经系统递送瘦素敏感的miRNA可缓解肥胖
体外荧光成像显示,注射了l SM-EV的小鼠中中枢神经系统的PKH26荧光显著高于注射了对照EV和AT-EV的小鼠,确认了它们在提高EV中枢神经系统靶向性方面的适用性(图7D)。PKH26荧光信号在下丘脑中富集(图7E和7F)。
文章小结

本研究首次揭示脂肪细胞囊泡通过其携带的特定miRNA靶向下丘脑、维持瘦素敏感性的关键作用,并基于此机制开发了可中枢靶向递送miRNA的工程化囊泡,成功逆转肥胖小鼠瘦素抵抗,为肥胖治疗提供了新策略。
如果你也想用同款思路进行数据分析、思路复现,那就快来联系小树吧!


长按扫描二维码
添加好友
了解更多信息
微信号:ACVC7777
往期推荐
IF42.5!海军军医大学长征医院团队荣登《Cell》!五图一表拿下双一区TOP!




