IF52.7!院士增选有效候选人,南京医科大学校长连发2篇“国自然”高分!
- 2026-05-17 14:54:31


先天性心脏病(CHD)是常见出生缺陷及婴儿死亡主因,胆固醇对胚胎发育关键。母体胆固醇水平与子代CHD风险关系不明,他汀类药物研究结果存争议,其通过Hedgehog信号通路调控心脏发育的机制及遗传与环境因素交互作用待阐明。
由南京医科大学校长胡志斌教授、沈洪兵院士领衔的研究团队在《Signal Transduction And Targeted Therapy》上发表的题为“母体胆固醇缺乏易导致先天性心脏病风险”的文章,旨在探究母体胆固醇水平与子代先天性心脏病(CHD)风险之间的关系。
文献解读

研究方法
数据来源
研究对象:5041个家庭 trio(母亲-父亲-子代)组成的前瞻性出生队列(江苏出生队列)。
暴露评估:检测母亲孕中期(20-28周)和孕晚期(28-36周)血清总胆固醇水平。
结局评估:通过胎儿超声心动图和产后随访诊断子代CHD。
动物模型验证
药物干预模型:给ICR雌性小鼠饲喂胆固醇吸收抑制剂(依折麦布)或合成抑制剂(阿托伐他汀),建立母体低胆固醇模型。
基因编辑模型:通过CRISPR/Cas9构建Cyp51I383V knock-in小鼠,模拟人类CYP51A1基因突变。
干预实验:对突变小鼠进行母体高胆固醇饮食(HCD)干预,评估CHD预防效果。
机制研究
分子层面:单细胞RNA测序、Western blot、qRT-PCR检测Hedgehog信号通路关键分子(Gli1、Shh)及心脏转录因子(GATA4)。
细胞层面:免疫荧光染色分析心肌细胞增殖、纤毛形成。
表观调控:CUT&Tag实验验证Gli1对Gata4启动子的直接结合。

近期前沿热点:虚拟细胞、虚拟敲除🌟
专注于生信分析,包含选题设计方案

文献计量学:方案合理,价格公道👍
主要结果
人群研究发现U型关联
研究首先在一个包含5041个家庭的前瞻性出生队列中发现,母体血清胆固醇水平与子代CHD风险呈U型关联。在妊娠中、晚期,胆固醇水平最低(T1组)的母亲,其子代患CHD的风险显著升高(RR分别为1.52和1.73)【图1b-d】。这表明胆固醇过低或过高都可能增加风险,但低胆固醇的影响更为明确。
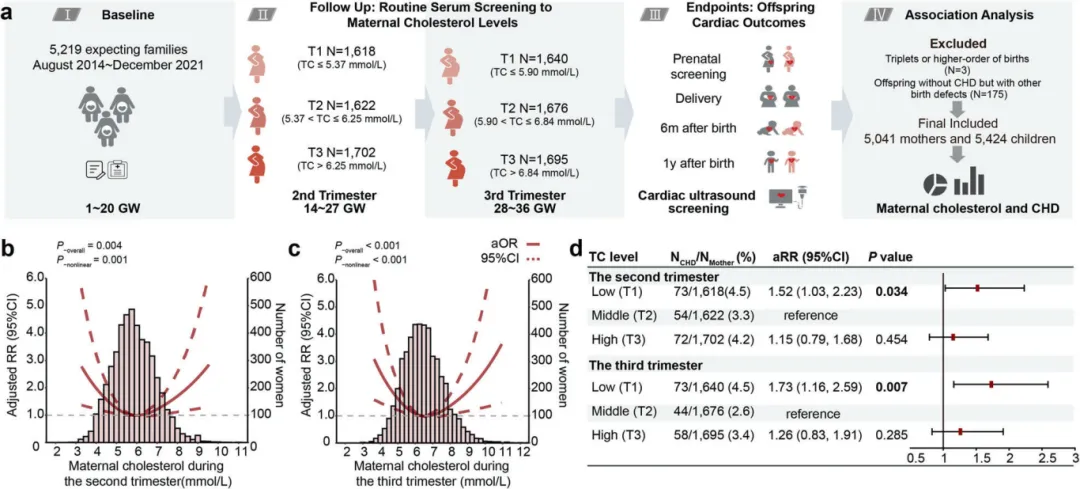
图1.母体胆固醇水平与先天性心脏病(CHD)发病率的关联性研究
为了验证因果关系,研究者在小鼠模型中使用了两种降胆固醇药物。结果显示,用药母鼠的血清胆固醇显著降低,其子代胚胎心脏的胆固醇含量也相应下降。
最重要的是,子代小鼠的CHD发病率从对照组的2.3%显著升高至14.2%(依折麦布组)和17.4%(阿托伐他汀组),最常见的亚型是室间隔缺损,直接证明母体胆固醇缺乏足以导致子代心脏畸形。
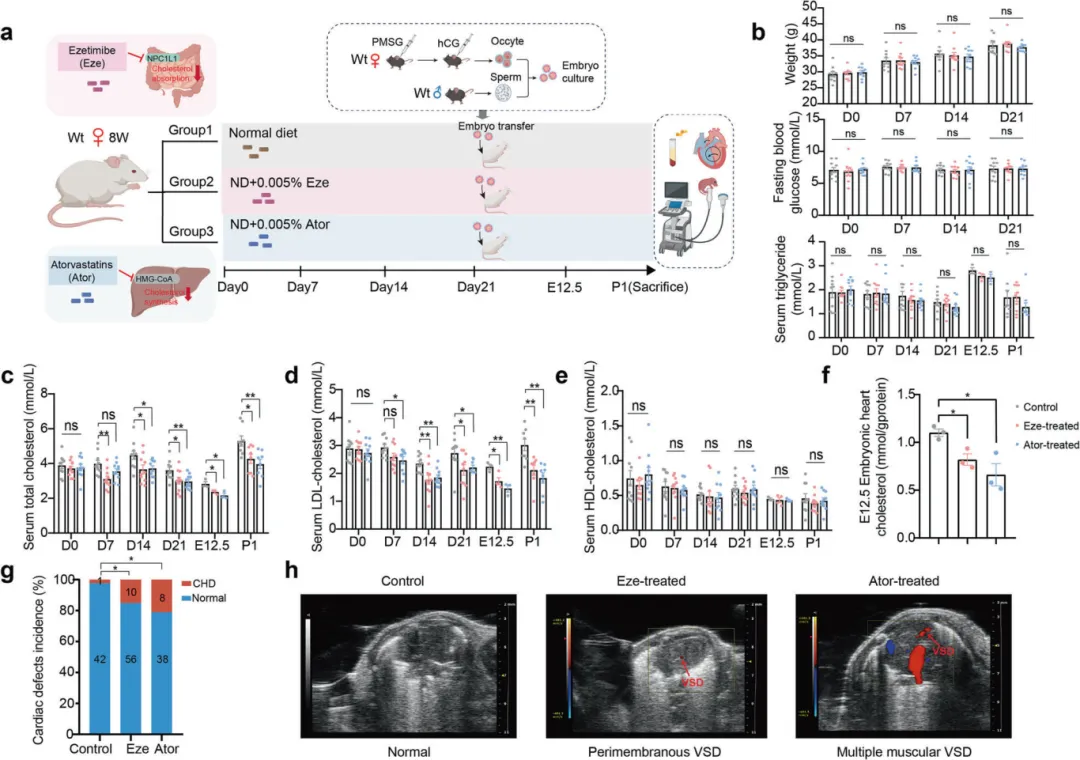
图2.母体低胆固醇小鼠模型子代冠心病(CHD)风险增加的验证
为了模拟临床常见的遗传易感背景,研究者从队列CHD患者中鉴定出一个反复出现的CYP51A1基因功能突变(I383V)【图3a-b】。该基因是胆固醇合成的关键酶。
突变小鼠胚胎心脏的胆固醇水平急剧下降,并且约32%的纯合突变新生儿出现心脏结构缺陷,如房间隔缺损、室间隔缺损和心肌变薄,证实该突变通过干扰胆固醇合成导致CHD【图3c-i】。
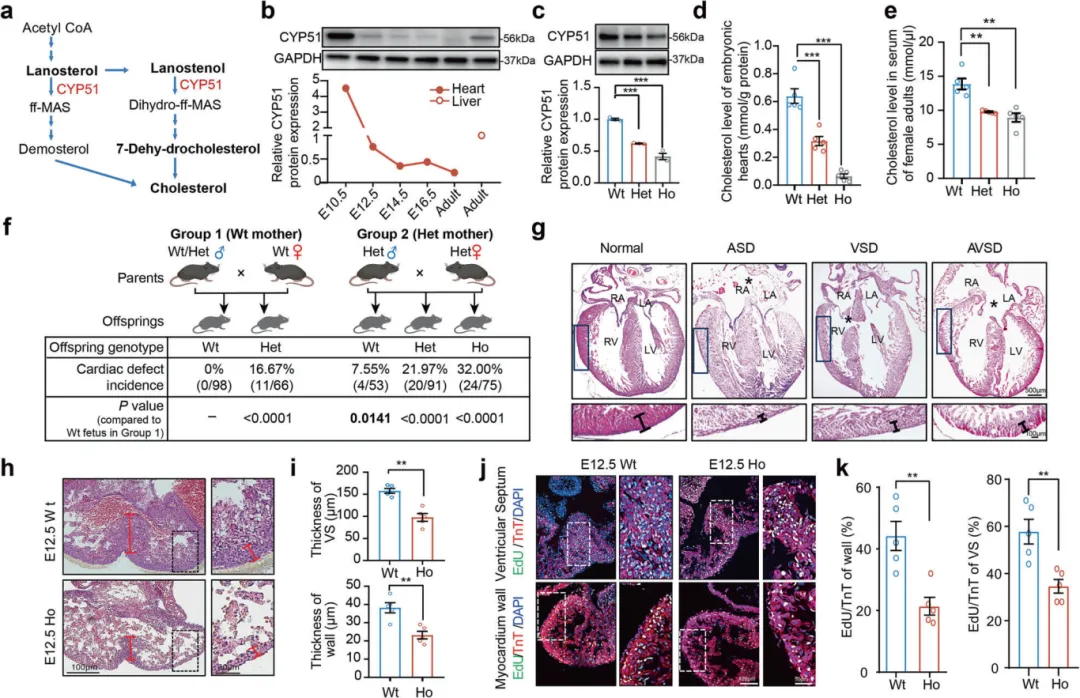
图3.Cyp51I383V突变体导致胆固醇合成障碍,引发心脏发育异常
通过单细胞RNA测序等技术,他们发现突变小鼠心脏中的Hedgehog(Hh)信号通路活性显著降低。这个通路在胚胎发育,包括心脏发育中至关重要。其关键效应分子GLI1的蛋白和mRNA水平都下降了【图4a-d】。
进一步分析显示,Hh通路的下游核心心脏转录因子GATA4的表达也显著降低【图4e-f】。
免疫荧光染色证实,突变心脏的心肌壁和室间隔中GATA4阳性的心肌细胞数量减少,这可能是导致室间隔发育缺陷的直接原因【图4g-j】。
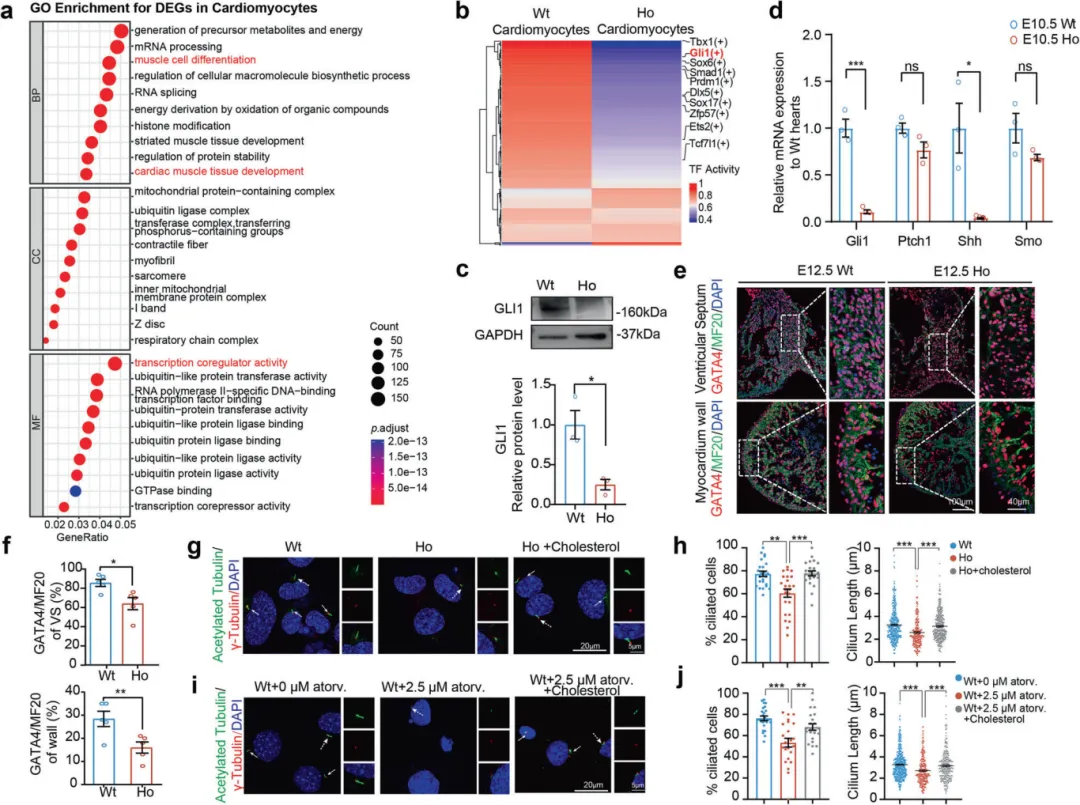
图4.由Cyp51I383V变异引起的胆固醇缺乏导致Hedgehog通路活性受损及纤毛发生异常
这项研究最令人鼓舞的发现是,这种遗传或药理学因素导致的CHD风险是可干预的。对携带Cyp51突变母鼠进行高胆固醇饮食喂养后,其突变子代胚胎心脏的胆固醇水平得到恢复。
更重要的是,子代CHD的发生率从26.5%大幅降低至5.8%【图5a-c】。同时,心肌细胞增殖、GATA4表达等指标也得到挽救【图5d-i】,证明通过母体饮食补充胆固醇是一种潜在的预防性策略。
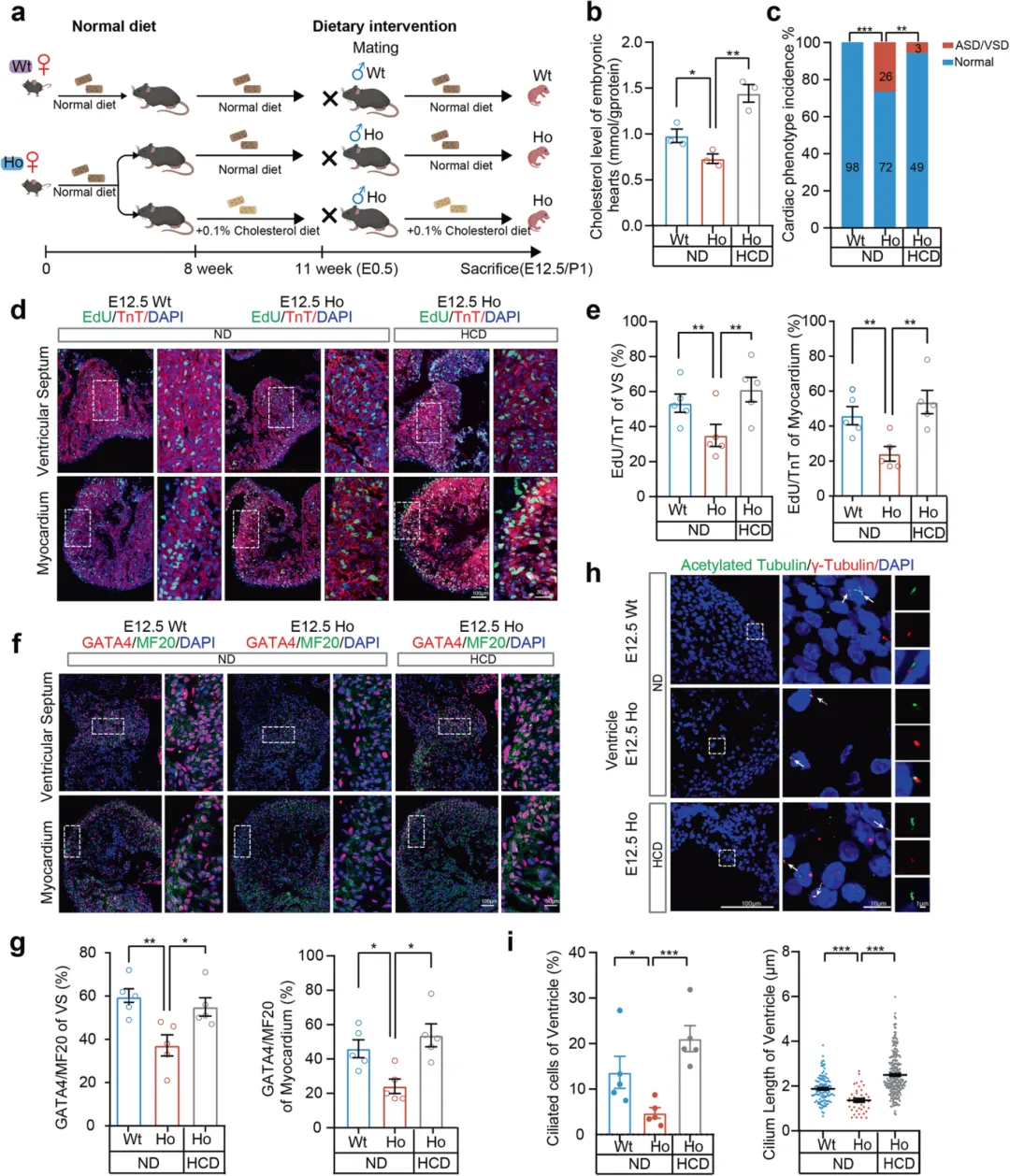
图5.对Cyp51I383V突变携带母鼠进行高胆固醇饮食预处理可降低子代冠心病(CHD)风险
文章小结
本研究系统证明母体胆固醇缺乏通过抑制Hedgehog信号和纤毛形成,增加子代CHD风险,而母体胆固醇补充可有效逆转这一过程。这些发现为CHD的预防提供了全新思路,提示孕期胆固醇监测和个性化营养干预可能成为降低CHD负担的重要策略。
如果你也想用“国自然热点+多组学”进行研究,需要生信分析,复现高分思路,那就快来后台联系吧~精彩生信,助力每一个科研梦想!





