南京中医药大学 | ds-HMGB1:化疗性周围神经痛的新型生物标志物与治疗靶点
- 2026-05-17 09:21:47

导读:
本研究以奥沙利铂诱导的周围神经病变(OIPN)为模型,围绕背根神经节(DRG)神经免疫交互展开研究,先通过动物实验证实 DRG 中双硫键型高迁移率族蛋白 1(ds-HMGB1)是 OIPN 机械痛的关键介质,再经单细胞转录组测序定位其来源为 DRG 小胶质样组织驻留巨噬细胞(M-TRMφs),进而解析其生成、释放及作用机制:PDIA3 催化 HMGB1 氧化为 ds-HMGB1,GSDMD 介导的焦亡促进其释放,释放的 ds-HMGB1 结合 C2 型感觉神经元 TLR4,经 NF-κB 通路上调 TRPV1 引发痛觉敏化;后续通过基因敲低、药物抑制验证 PDIA3/GSDMD/ds-HMGB1/TLR4 轴的干预有效性,且不影响奥沙利铂抗肿瘤效果,最后在临床患者中证实血清 ds-HMGB1 与 OIPN 疼痛程度正相关,明确其作为生物标志物和治疗靶点的临床价值。
首次明确 DRG 小胶质样组织驻留巨噬细胞是 OIPN 中 ds-HMGB1 的核心来源,解析了 PDIA3 催化氧化、GSDMD 焦亡释放的 ds-HMGB1 生成释放双机制;证实 ds-HMGB1-TLR4-TRPV1 轴是 DRG 神经免疫交互的关键通路,且干预该通路可缓解疼痛而不影响奥沙利铂抗肿瘤效果,同时发现血清 ds-HMGB1 可作为 OIPN 疼痛的生物标志物。
化疗诱导的周围神经病变(CIPN)是奥沙利铂等化疗药的常见副作用,以痛觉超敏、麻木为主要表现,严重影响患者生活质量甚至导致化疗中断。背根神经节(DRG)作为外周感觉中继站,是 CIPN 的关键靶点,其神经免疫微环境的交互作用参与痛觉发生,但具体机制尚未明确。高迁移率族蛋白 1(HMGB1)的双硫键亚型(ds-HMGB1)是促炎活性亚型,可激活 TLR4 介导神经炎症,但 DRG 中 ds-HMGB1 的细胞来源、氧化生成及释放机制,以及其与感觉神经元的作用靶点仍不清楚。目前 CIPN 治疗手段有限,阿片类药物疗效一般且副作用大,亟需挖掘非阿片类、不影响化疗效果的治疗靶点,同时寻找可预测 CIPN 严重程度的生物标志物。
构建小鼠 OIPN 模型,通过行为学实验检测机械痛和冷痛敏化程度;利用蛋白质印迹、免疫荧光定位 DRG 中 HMGB1 及亚型的表达与细胞分布;采用单细胞 RNA 测序解析 DRG 细胞类型及基因表达特征,定位 ds-HMGB1 来源和关键调控分子;通过磁珠分选分离 DRG M-TRMφs 和神经元,验证细胞特异性的分子表达;利用 AAV 靶向敲低技术实现 M-TRMφs 或神经元中目标基因的特异性沉默,结合 PDIA3、GSDMD、TLR4 等靶点的特异性抑制剂,验证通路干预效果;构建荷瘤小鼠模型,验证干预手段对奥沙利铂抗肿瘤效果的影响;收集结直肠癌奥沙利铂化疗患者血清,检测 ds-HMGB1 水平并分析其与 NCI-CTCAE 疼痛分级、VAS 评分的相关性,同时结合 ELISA、免疫印迹等技术检测炎症因子水平。
奥沙利铂处理后小鼠 DRG 中 ds-HMGB1 显著升高,且与机械痛敏化正相关,靶向敲低 DRG HMGB1 可缓解机械痛;单细胞测序证实 ds-HMGB1 主要来源于 DRG M-TRMφs,该细胞中 PDIA3 通过形成二硫键催化 HMGB1 氧化为 ds-HMGB1,GSDMD 介导的焦亡是 ds-HMGB1 释放的主要方式,抑制 PDIA3 或 GSDMD 可降低 ds-HMGB1 水平并缓解 OIPN 机械痛;ds-HMGB1 可特异性结合 DRG C2 型感觉神经元的 TLR4,激活 NF-κB 通路上调 TRPV1 表达,引发痛觉敏化,敲低或抑制 TLR4 可显著缓解疼痛;荷瘤小鼠实验证实 GSDMD 抑制剂双硫仑不影响奥沙利铂的抗肿瘤效果;临床患者中,奥沙利铂化疗后血清 ds-HMGB1 水平显著升高,且其含量及占总 HMGB1 比例与 OIPN 疼痛严重程度、慢性化程度正相关,是优于总 HMGB1 的生物标志物。
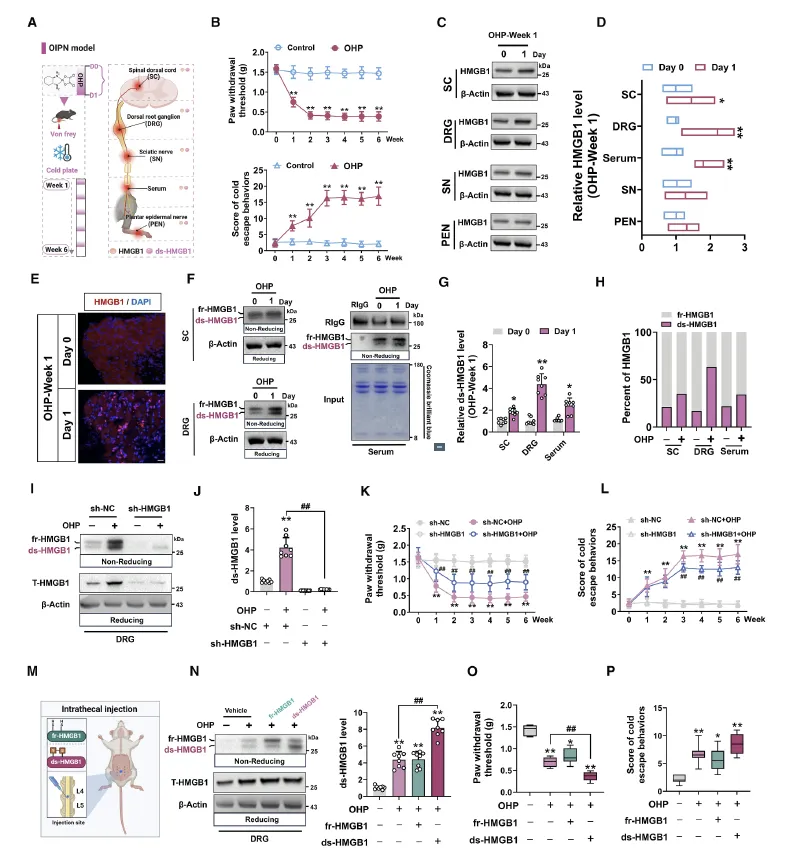
Figure 1:该图以奥沙利铂诱导的周围神经病变(OIPN)小鼠模型为研究对象,系统验证了背根神经节(DRG)中双硫键型高迁移率族蛋白 1(ds-HMGB1)是介导 OIPN 机械痛敏化的关键分子。首先通过行为学实验证实奥沙利铂处理后小鼠出现显著的机械痛和冷痛敏化,且 DRG 中总 HMGB1 及 ds-HMGB1 的升高程度远高于脊髓、血清等其他组织,ds-HMGB1 在 HMGB1 中的占比也在 DRG 中最高。通过 DRG 靶向 AAV 敲低 HMGB1,可显著降低 DRG 内 ds-HMGB1 水平并缓解机械痛敏化,而对冷痛的改善仅局限于急性期;向 DRG 鞘内注射纯化的 ds-HMGB1 会加重机械痛敏化,注射还原型 HMGB1 则无此效果,进一步证实 DRG 局部的 ds-HMGB1 是驱动 OIPN 急性机械痛的核心因子。
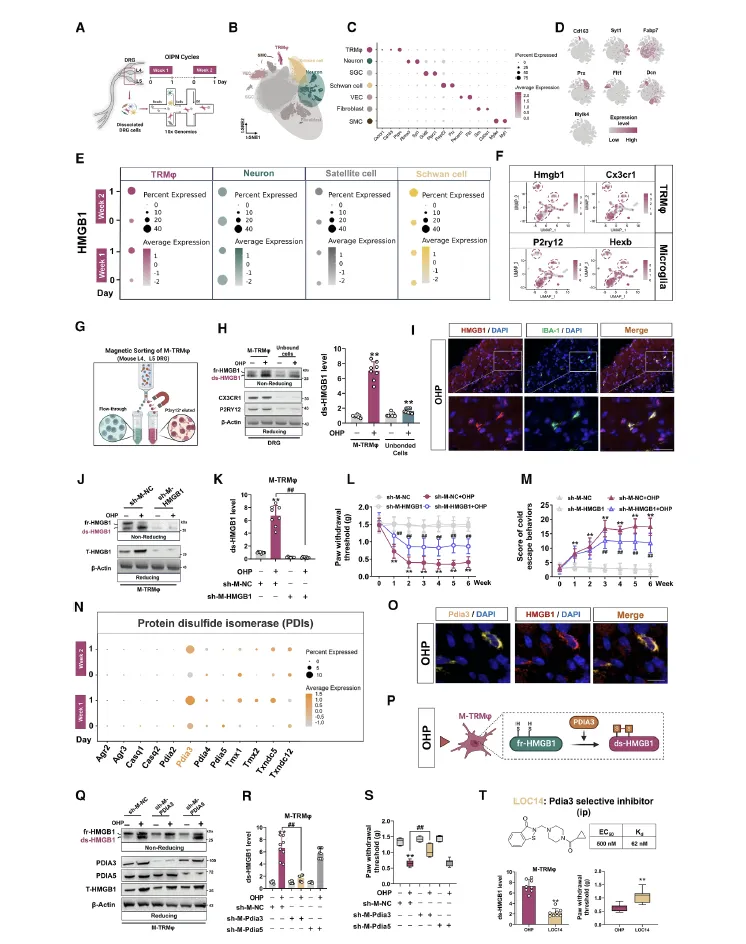
Figure 2:该图明确了 DRG 中 ds-HMGB1 的核心细胞来源为小胶质样组织驻留巨噬细胞(M-TRMφs),并解析了其生成的关键分子机制为 PDIA3 介导的氧化修饰。通过单细胞 RNA 测序发现,奥沙利铂处理后 DRG 中 HMGB1 的表达升高主要集中在 M-TRMφs 中,该细胞同时高表达小胶质细胞标志物,免疫荧光和磁珠分选实验也证实 HMGB1 及 ds-HMGB1 主要定位于 M-TRMφs。特异性敲低 M-TRMφs 中的 HMGB1 可降低 DRG 内 ds-HMGB1 水平并缓解机械痛敏化,抑制巨噬细胞的米诺环素也可降低 ds-HMGB1 并改善疼痛。进一步通过单细胞测序和免疫荧光发现,M-TRMφs 中 PDIA3 在 OIPN 急性期显著上调且与 HMGB1 共定位,PDIA3 可催化 HMGB1 形成二硫键生成 ds-HMGB1,靶向敲低或药物抑制 M-TRMφs 中的 PDIA3,能有效降低 ds-HMGB1 水平并缓解奥沙利铂诱导的机械痛敏化。
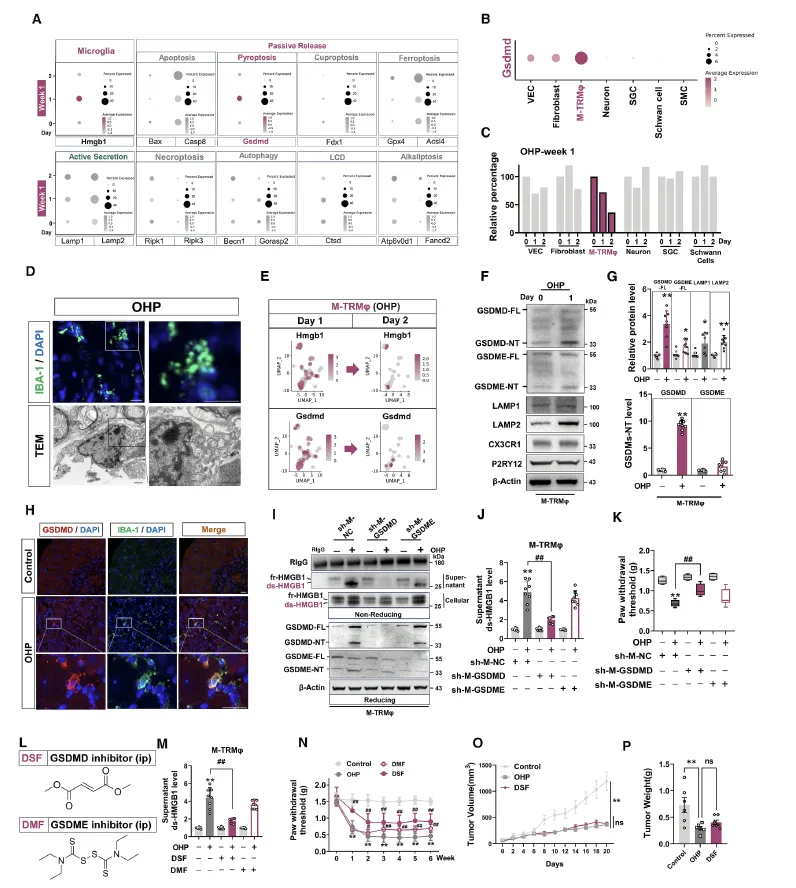
Figure 3:该图阐明了 DRG 中 M-TRMφs 释放 ds-HMGB1 的核心方式为 GSDMD 介导的焦亡,且抑制该过程可缓解疼痛同时不影响奥沙利铂的抗肿瘤效果。通过单细胞测序分析 M-TRMφs 中 HMGB1 的释放通路,发现奥沙利铂处理后焦亡相关分子 GSDMD 显著上调,而溶酶体介导的分泌通路无明显变化,且 M-TRMφs 的数量随奥沙利铂处理减少,符合焦亡的细胞特征。免疫荧光和电镜实验证实 M-TRMφs 在 OIPN 中出现焦亡的典型形态学改变,GSDMD 及其活化的 N 端片段在该细胞中高表达。特异性敲低 M-TRMφs 中的 GSDMD 可显著减少 ds-HMGB1 的胞外释放并缓解机械痛敏化,而敲低另一焦亡分子 GSDME 则效果微弱;GSDMD 的特异性抑制剂双硫仑可有效降低 ds-HMGB1 释放并改善疼痛,且在荷瘤小鼠模型中,双硫仑与奥沙利铂联用不会削弱奥沙利铂对肿瘤的抑制作用,证实该干预靶点的临床应用安全性。
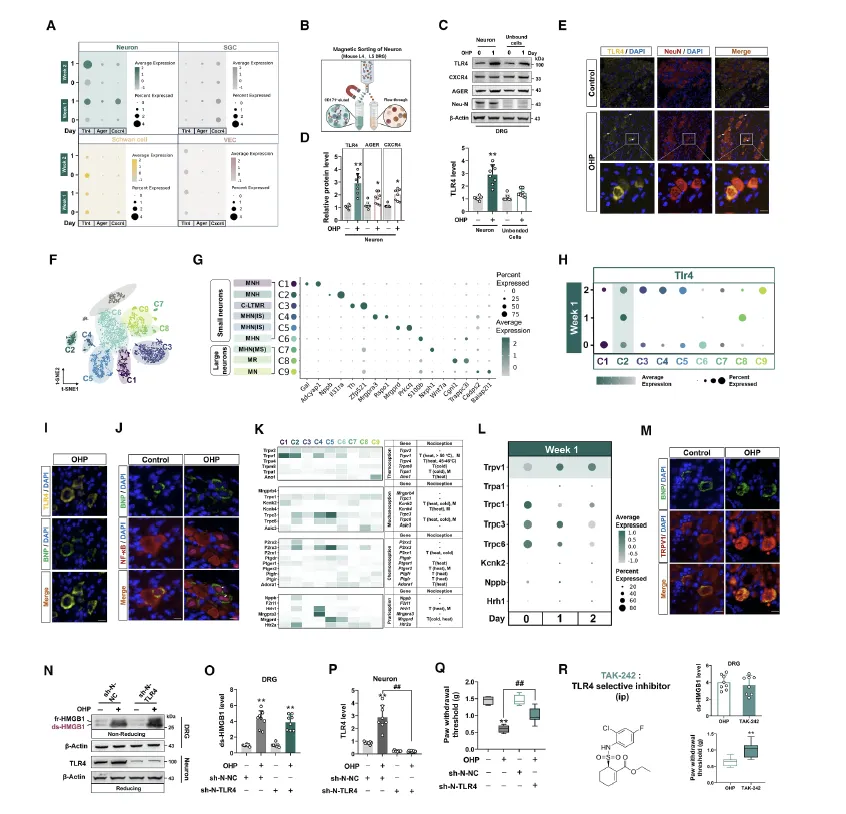
Figure 4:该图解析了 ds-HMGB1 引发痛觉敏化的下游作用机制,即通过结合 DRG 中 C2 亚型感觉神经元的 TLR4,激活 NF-κB 通路并上调 TRPV1,进而放大疼痛信号。通过单细胞测序、磁珠分选和免疫荧光实验发现,奥沙利铂处理后 DRG 神经元中 TLR4 表达显著升高,且 TLR4 特异性富集在 C2 亚型感觉神经元上,其他 HMGB1 受体则无明显变化。ds-HMGB1 与 C2 神经元的 TLR4 结合后,会触发 NF-κB 的核转位,而 C2 神经元恰好高表达机械痛相关的离子通道 TRPV1,且奥沙利铂处理后 TRPV1 的表达随 OIPN 进程呈时间依赖性上调,免疫荧光证实 TRPV1 与 C2 神经元标志物共定位。特异性敲低 DRG 神经元中的 TLR4,或使用 TLR4 抑制剂 TAK-242,均可显著降低 TRPV1 的表达并缓解奥沙利铂诱导的机械痛敏化,而敲低其他 HMGB1 受体则无此效果,同时在雌性小鼠模型中也验证了该通路的一致性,证实 ds-HMGB1-TLR4-TRPV1 轴是介导神经元痛觉敏化的核心通路。
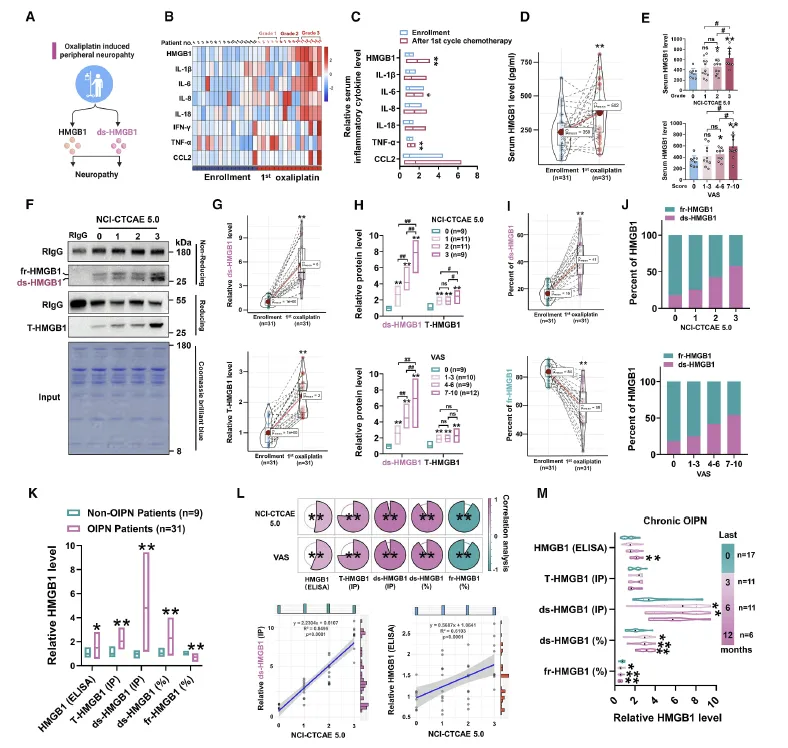
Figure 5:该图通过临床患者样本验证了血清 ds-HMGB1 与奥沙利铂诱导的周围神经病变(OIPN)疼痛严重程度及慢性化程度密切相关,明确其可作为 OIPN 的潜在生物标志物。研究收集了结直肠癌患者奥沙利铂化疗前后的血清样本,发现化疗后出现 OIPN 的患者血清 HMGB1 水平显著升高,且疼痛程度越严重(按 NCI-CTCAE 分级和 VAS 评分),血清 HMGB1 升高越明显。进一步检测发现,患者血清中升高的主要是 ds-HMGB1,其占总 HMGB1 的比例在 OIPN 患者中显著高于无神经病变的患者,且该比例与疼痛分级、VAS 评分呈强正相关。此外,在发生慢性 OIPN 的患者中,血清 ds-HMGB1 水平及占比与慢性神经痛的严重程度的相关性,远高于总 HMGB1,证实 ds-HMGB1 是比总 HMGB1 更优的、可用于评估 OIPN 疼痛严重程度和慢性化的临床生物标志物。
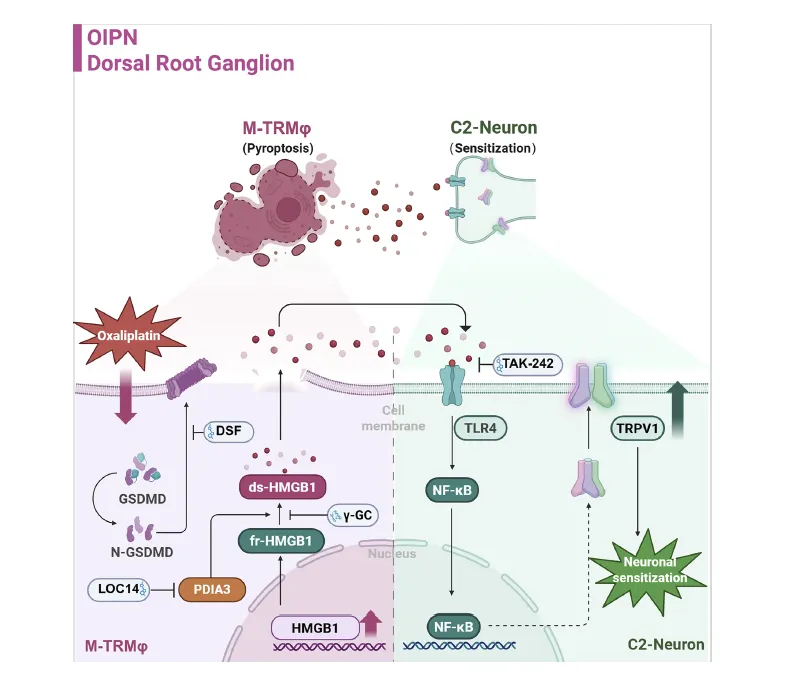
Figure 6:该图为该研究的核心机制示意图,系统性整合了 DRG 中 M-TRMφs 源性 ds-HMGB1 介导奥沙利铂诱导周围神经痛的完整分子通路,直观呈现了 “巨噬细胞 - 神经元” 的神经免疫交互调控轴。奥沙利铂作用于 DRG 后,诱导 M-TRMφs 中 PDIA3 上调,PDIA3 催化胞内 HMGB1 氧化形成二硫键,生成具有促炎活性的 ds-HMGB1;同时奥沙利铂触发 M-TRMφs 发生 GSDMD 介导的焦亡,使胞内的 ds-HMGB1 大量释放至胞外;释放的 ds-HMGB1 特异性结合邻近 C2 亚型感觉神经元表面的 TLR4,激活神经元内的 NF-κB 信号通路,进而上调痛觉相关离子通道 TRPV1 的表达,增强 C2 神经元的伤害性感受兴奋性,最终引发并放大机械痛敏化,形成 OIPN 的核心病理环路。同时示意图也标注了该通路中的关键干预靶点,包括 PDIA3 抑制剂 LOC14、GSDMD 抑制剂 DSF、TLR4 抑制剂 TAK-242 及 γ-GC 等,为 OIPN 的临床干预提供了明确的分子靶点方向。
本研究阐明了 DRG 中 M-TRMφs 源性 ds-HMGB1 介导奥沙利铂诱导周围神经痛的核心机制:PDIA3 催化 HMGB1 氧化生成 ds-HMGB1,GSDMD 介导的焦亡促进其释放,释放的 ds-HMGB1 结合 C2 神经元 TLR4 并经 NF-κB 通路上调 TRPV1,形成 “巨噬细胞 - 神经元” 的神经免疫调控轴,驱动痛觉敏化。靶向抑制 PDIA3、GSDMD 或 ds-HMGB1/TLR4 轴,可有效缓解 OIPN 疼痛且不影响奥沙利铂抗肿瘤疗效。临床患者血清 ds-HMGB1 与 OIPN 疼痛程度密切相关,可作为疾病诊断和严重程度评估的生物标志物,而 PDIA3、GSDMD、ds-HMGB1、TLR4 等为 CIPN 提供了新的非阿片类治疗靶点。
研究仅基于奥沙利铂诱导的 CIPN 模型,结果能否推广至其他化疗药或非化疗性神经痛仍需验证;干预该通路仅部分缓解疼痛,提示存在其他并行机制,需探索多靶点联合治疗策略。未来需在人类 DRG 组织中验证该机制,开发高灵敏度的 ds-HMGB1 检测方法,推进 PDIA3、GSDMD 等靶点的药物研发并开展临床转化研究。

国家杰青一对一答疑视频
医学省自然申请答疑,立项的关键条件是哪一些?从哪些方向可以杀出重围
临床型博士如何准备国青标书?没有预实验怎么办?专家一对一解答规划
中医药科研研究