南京大学谢然《JACS》:一种用于时空可控、蛋白质选择性及体内聚糖编辑的光激活糖酶平台
- 2026-05-25 21:54:25



本文开发的GLOBE(Glycoenzyme Light-mediated Optical control for Biosurface Editing)平台,通过在糖酶活性中心或附近位点特异性引入光笼非天然氨基酸(如邻硝基苄基酪氨酸ONBY),实现了糖酶活性的光控激活,从而能在时空分辨率下对细胞表面聚糖进行精准编辑。该平台具有时空精准性,可通过365 nm紫外光或上转换纳米颗粒(UCNPs)介导的980 nm近红外光激活,实现微米级空间分辨率和分钟级时间分辨率的聚糖编辑;同时具备蛋白质选择性,结合MUC1靶向适配体能够实现特定蛋白质(如MUC1)表面聚糖的选择性氧化,有效避免脱靶反应。此外,该平台还支持多酶级联与体内应用,不仅可扩展至唾液酸酶等多种糖酶,构建正交光响应级联反应(如唾液酸去除后增强半乳糖氧化),还能通过UCNPs克服紫外光组织穿透限制,成功在小鼠肿瘤模型中实现体内聚糖编辑。

研究问题:细胞表面聚糖通过动态且空间复杂的结构参与细胞通讯、免疫 surveillance 等关键生物学过程,但其时空精准调控(如特定细胞、微域或时间窗口的聚糖编辑)仍面临挑战。
研究难点:现有方法(如配体靶向糖酶、金属离子抑制)依赖组成型活性酶,难以实现亚细胞水平的时空控制;遗传密码扩展(GCE)与光笼非天然氨基酸(UAAs)虽为光控蛋白活性提供工具,但此前未实现细胞表面蛋白质选择性聚糖编辑,且紫外光组织穿透能力有限。
文献综述:(1)糖酶编辑现状:化学酶法、抗体-糖酶偶联等策略实现了蛋白质选择性聚糖编辑,但缺乏时空控制;(2)光控蛋白技术:光笼UAAs通过GCE可实现蛋白质活性的光控激活,但此前仅用于胞内酶(如O-GlcNAc转移酶),未扩展至细胞表面糖酶;(3)局限性:现有光控策略依赖紫外光,难以应用于深层组织;且糖酶活性调控需平衡光笼效率与酶活恢复,位点选择难度大。

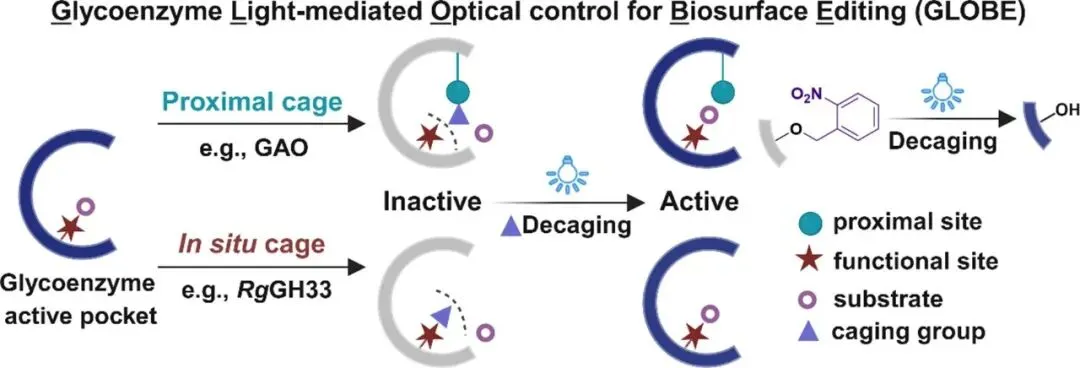
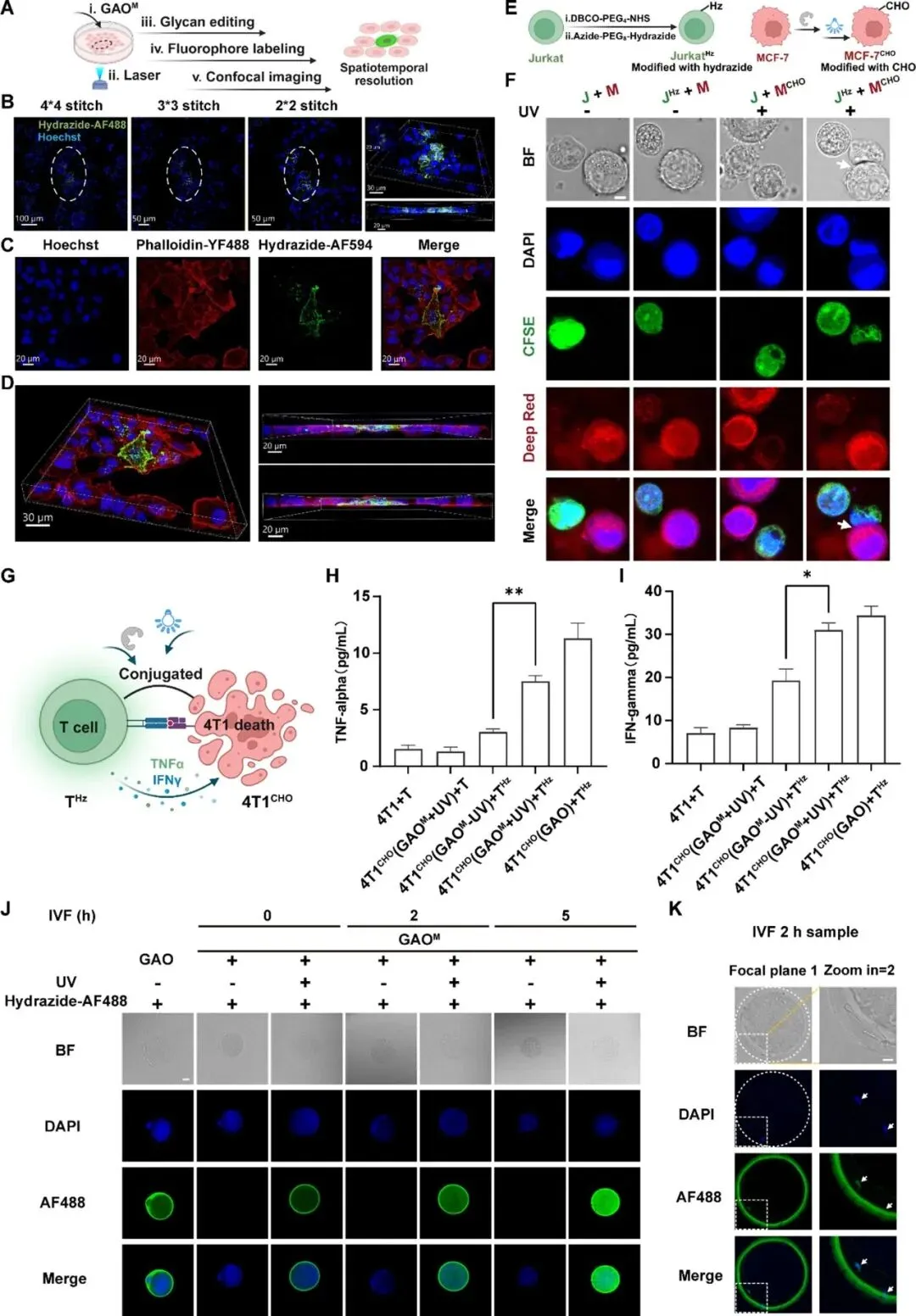
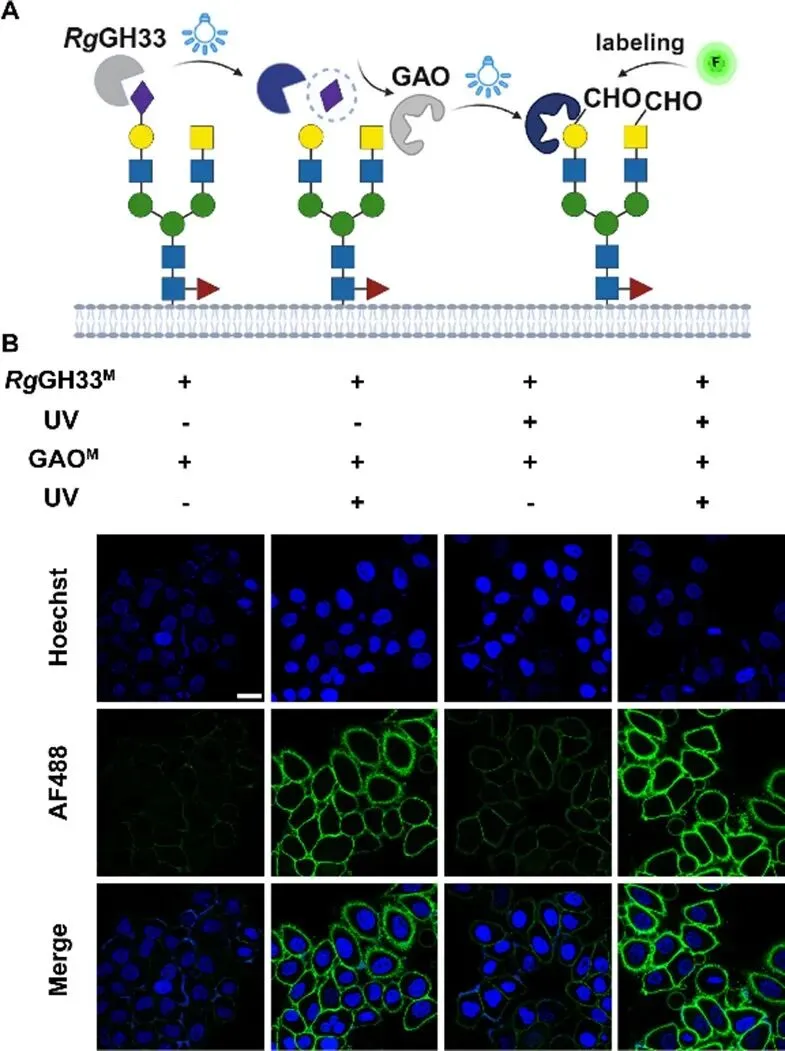
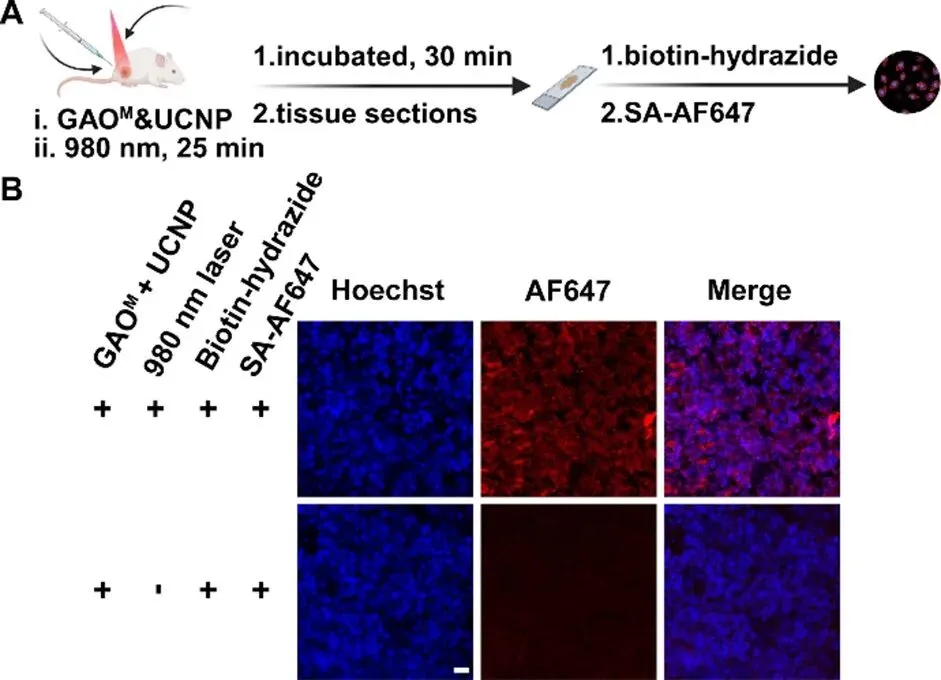
图7。(A)实验流程示意图。(B)体内糖编辑后皮下肿瘤组织切片的共聚焦荧光显微镜图像。 BALB /c小鼠经瘤内注射 GAOM 和 UCNP 后,接受980nm激光照射。肿瘤组织经解剖后冷冻切片,依次与生物素-酰肼和链霉亲和素-AF647孵育。细胞核通过Hoechst33342染色显示(蓝色信号)。比例尺:10 μm。

GLOBE平台通过光笼UAA的位点特异性引入,为细胞表面聚糖的时空精准编辑提供了模块化框架:
技术突破:实现了糖酶的光控激活(如GAO、唾液酸酶RgGH33),结合适配体靶向可实现蛋白质选择性编辑,并通过UCNPs辅助实现体内深层组织应用 。
应用价值:可用于研究聚糖动态(如受精过程中卵母细胞表面聚糖重塑)、调控细胞-细胞相互作用(如T细胞-肿瘤细胞结合),并为疾病治疗(如光控前药释放)提供新思路 。
局限性与展望:光笼位点选择依赖结构设计,紫外光穿透限制仍需改进;未来可通过AI辅助位点预测、长波长光笼开发及纳米载体递送,进一步拓展其在基础研究与临床中的应用 。

欢迎投稿/进科研交流群,添加好友时请备注:姓名-单位-研究方向:加VX:Winter_9798或点击下方公众号发送关键词:“进群”,扫二维码即可进群。
(关注点赞,好运不断!点个在看,你最好看)
点击发光材料及应用小助手,可以让基于公众号的知识库【AI智能体】
为您实时答疑
原文DOI: https://doi.org/10.1021/jacs.5c21919



