最新!南京大学国家杰青&优青&中国青年科技奖Nat Synth-合成生物学-解锁NTF2酶的隐藏技能:亚胺催化助力复杂大环化合物的生物合成
- 2026-05-28 17:19:23
(点击页面左下角阅读原文,直达文献页面)
一、中文标题
核转运因子2样酶催化亚胺介导的大环化的结构和机制研究(Structural and mechanistic insights into iminium-catalysed macrocyclization by nuclear transport factor 2-like enzymes)
二、发表单位及通讯作者
主要单位:南京大学(模式动物研究所、医药生物技术国家重点实验室等)
通讯作者:张博(Bo Zhang)、戈惠明(Hui Ming Ge)
三、科学问题
NTF2样酶如何通过亚胺中间体催化线性聚酮底物发生立体选择性串联迈克尔加成和Knoevenagel缩合,从而形成15元大环内酯骨架?
四、发表时间
时间:2026年1月29日
链接:https://doi.org/10.1038/s44160-025-00989-z

五、摘要
大环化是天然产物生物合成中构建刚性结构的关键步骤。本研究通过基因组挖掘发现了一类NTF2样酶(AkaM/ManM),它们催化一种新颖的串联反应:先立体选择性迈克尔加成形成四氢呋喃环,再通过Knoevenagel缩合完成15元碳环大环化。晶体结构结合突变分析表明,保守的赖氨酸残基与底物醛基形成亚胺中间体,而天冬氨酸作为广义碱介导质子转移。通过捕获不同反应状态的复合物结构,揭示了底物从线性到预环化构象的动态变化过程。该机制拓展了NTF2样酶的催化功能库,并为基于亚胺催化的生物催化设计提供了新思路。
六、研究背景
大环化是将线性前体转化为环状产物的关键策略,能显著增强天然产物的结构刚性和生物活性。尽管五元或六元环的形成相对容易,但构建超过12元的大环面临构象熵的挑战。自然界已演化出多种大环化机制,例如硫酯酶介导的大环内酯/内酰胺形成、细胞色素P450催化的氧化偶联、自由基SAM酶参与的环化等。然而,仍有大量未知的环化机制等待发掘。
Akaelide(AKA)和mangromicin(MAN)是从链霉菌和勒克瓦氏菌中分离的15元碳环聚酮化合物,其结构中包含独特的β-酮-δ-内酯单元。与典型的I型聚酮合酶产生的内酯不同,AKA和MAN为全碳环骨架,提示其生物合成涉及非典型环化机制。基因簇分析显示,aka和man簇均编码四个巨型I型PKS以及一组保守的后修饰酶,其中包括两个P450和一个NTF2样蛋白。NTF2样蛋白最初被认为仅参与核转运,但后续研究发现其具有异构酶、脱水酶、环化酶等多种催化功能,如SnoaL催化蒽环类六元环形成,XiaE参与吡喃环构建等。然而,NTF2样蛋白能否催化大环化尚不清楚。
本研究旨在揭示AKA生物合成中NTF2样酶(AkaM/ManM)催化大环化的分子机制,并通过结构生物学和生化手段阐明其催化机理。
七、研究结果
结果1、基因簇鉴定与异源表达
通过构建细菌人工染色体文库,从Streptomyces sp. NPS554中获得包含完整aka基因簇的BAC克隆pHG8301,并在异源宿主S. albus J1074中成功表达出AKA(1),证实了该基因簇的功能。基因失活实验表明,P450基因akaP1的缺失导致中间体2积累,而akaM的缺失则导致化合物6a/6b积累。回补实验证实AkaP1/ManP1和AkaM/ManM功能保守。
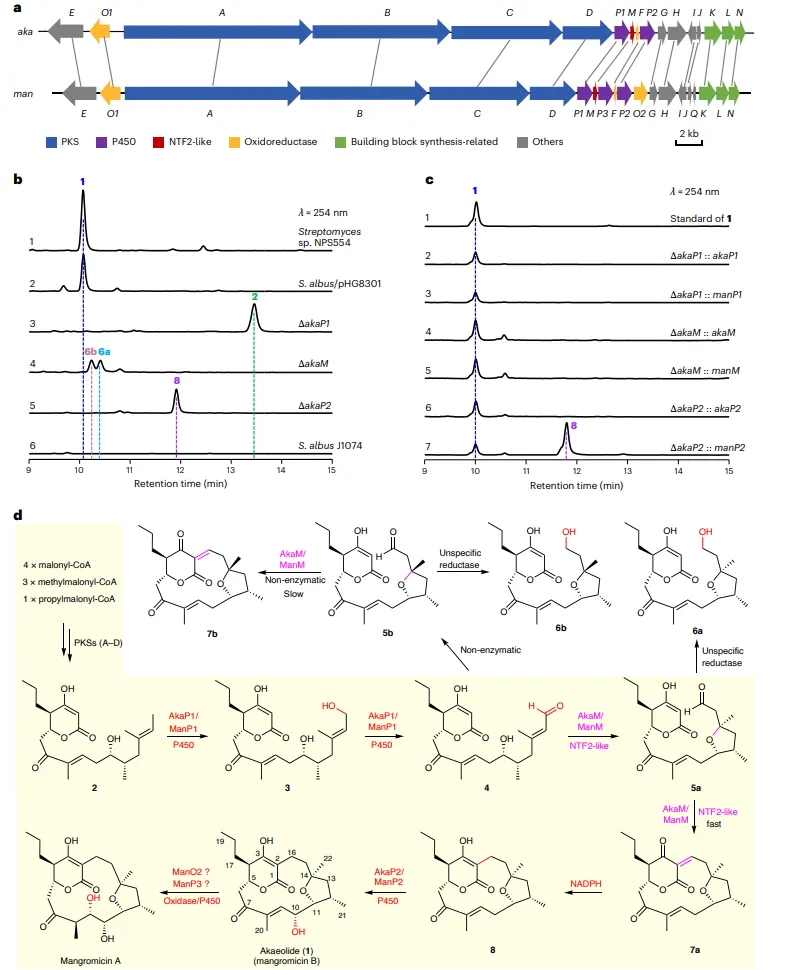
图1 生物合成
结果2、AkaP1催化末端甲基氧化
体外酶活实验显示,AkaP1在铁氧还蛋白和NADPH存在下,将2依次氧化为羟基化产物3和醛基产物4/4a。高分辨HPLC分析表明,4/4a可自发发生非酶促迈克尔加成,生成非对映异构体5a和5b。同位素标记实验证实NADPH可将5a还原为8。
结果3、AkaM催化串联环化
纯化的AkaM可高效地将5a转化为单一产物7a(大环化产物),而对非对映体5b转化效率极低(催化效率相差2600倍)。当以4为底物时,AkaM催化生成5a和7a,证明其同时具有立体选择性迈克尔加成和Knoevenagel缩合活性。该双功能催化能力在NTF2样酶中属首次发现。
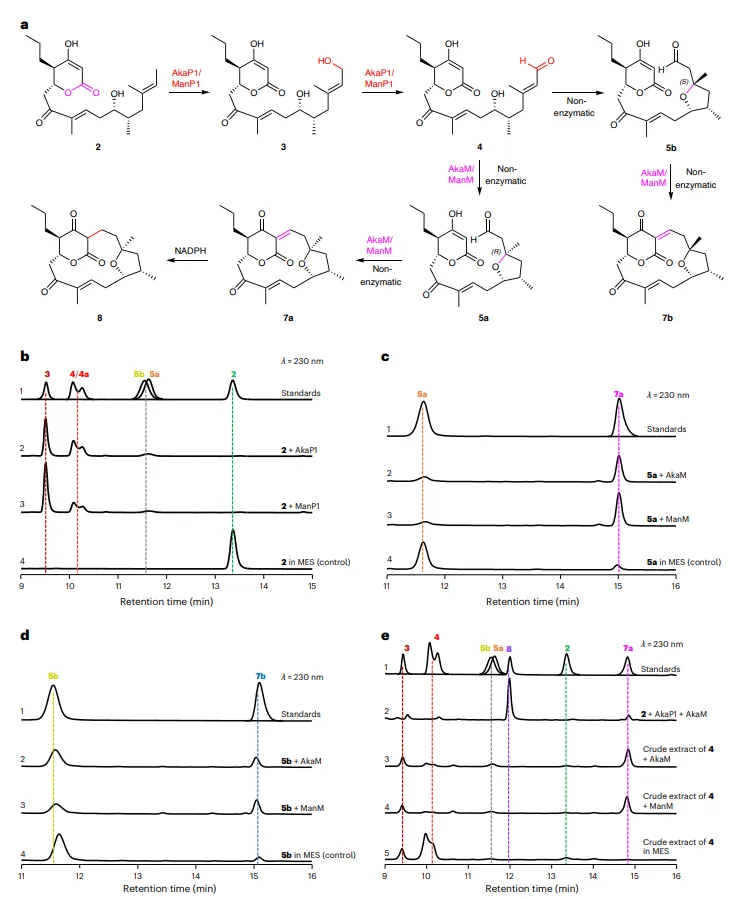
图2 反应测试
结果4、晶体结构揭示活性位点
解析了AkaM及其同源酶CatM、SacM、MicM的apo结构,以及CatM与底物模拟物6b、SacM与3/6b、CatM-W86A与6a的复合物结构。所有结构均呈现高度相似的桶状折叠,活性通道由疏水残基构成,保守残基(如K113、D101、W31等)位于通道底部。复合物结构中,6b的末端羟基与K113距离仅3.0 Å,暗示K113参与亚胺形成。
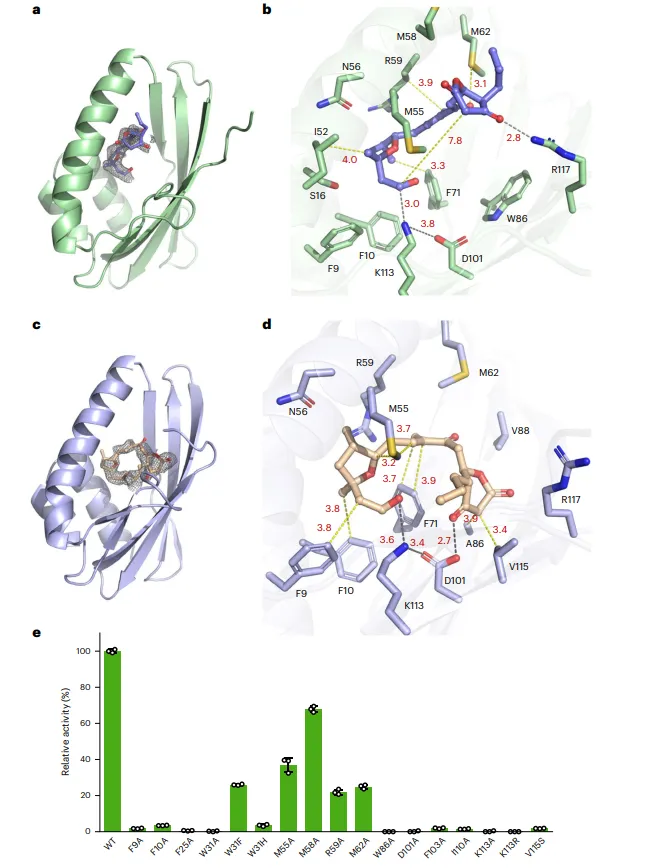
图3 晶体结构
结果5、亚胺中间体的捕获与验证
通过NaBH4还原捕获实验,在CatM与5a反应体系中检测到分子量增加376 Da的加合物,对应赖氨酸与底物形成的还原胺化产物。胰蛋白酶消化和质谱分析确证加合物位于K113。该加合物在K113A突变体中消失,证实K113是亚胺形成的关键残基。D101A突变不影响亚胺形成,但完全丧失催化活性,表明D101可能作为广义碱参与后续质子转移。
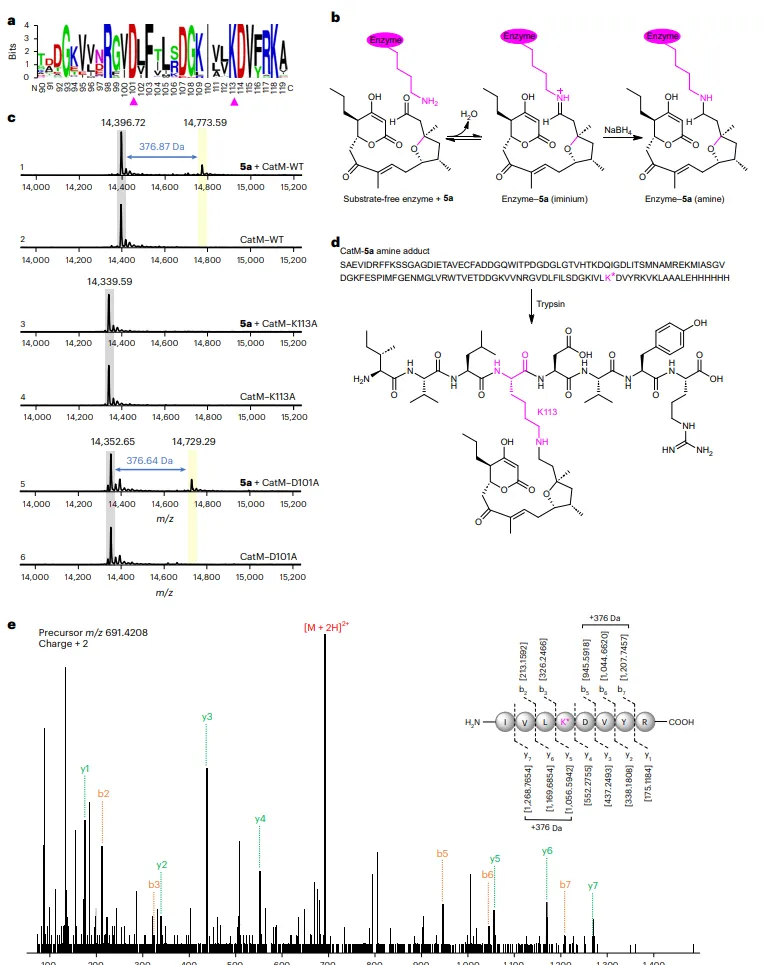
图4 鉴定
结果6、预环化构象的捕获
CatM-W86A与6a的复合物结构显示,底物构象进一步弯曲,末端与δ-内酯的距离缩短至6.4 Å,D101与δ-内酯形成2.7 Å氢键,并与K113的ε-氨基形成3.4 Å相互作用,提示该状态可能代表环化前的预组织构象。W86的位阻效应迫使底物采取正确构象,其突变导致活性丧失。
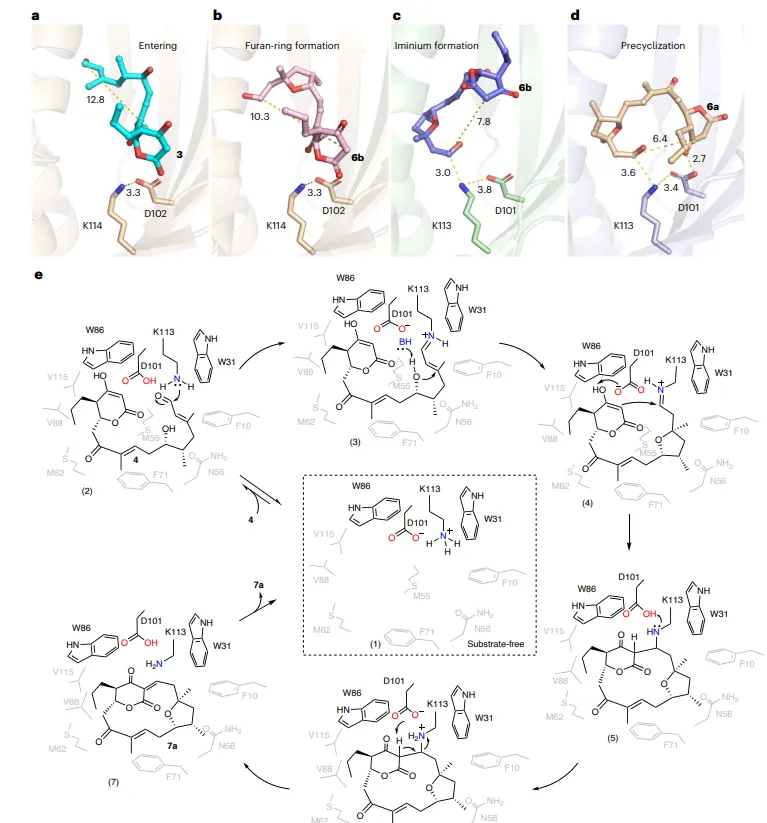
图5 构象捕获
结果7、机制总结
基于结构和生化数据,提出AkaM的催化机制:线性醛底物进入活性通道,K113的ε-氨基与醛基形成亚胺中间体(由W31通过阳离子-π相互作用稳定),随后D101作为广义碱启动迈克尔加成,形成四氢呋喃环;接着亚胺活化的中间体发生Knoevenagel缩合,最终释放大环产物。
结果8、基因组挖掘与功能验证
以AkaM为探针进行序列比对,发现127个同源蛋白,其中87个与I型PKS基因簇关联。选取四个同源酶(SacM、CatM、OliM、MicM)进行体外实验,证实它们均可催化类似反应,但效率各异,提示该类酶具有广泛的催化潜力。
八、讨论
本研究首次揭示了NTF2样酶通过亚胺中间体催化大环化的机制,将有机催化中的亚胺催化概念拓展至生物合成领域。通过捕获多个反应中间态的晶体结构,直观展示了酶如何通过空间约束和化学催化协同引导线性底物完成大环化。该机制不仅丰富了NTF2样酶的催化功能谱,也为工程化改造此类酶用于合成复杂大环化合物提供了结构基础。未来可通过定向进化提高其底物谱和立体选择性,应用于药物中间体的绿色合成。此外,基因组中大量未表征的同源酶提示自然界中存在更多新颖的环化反应等待发掘。
