南京医科大学附属苏州医院陈双庆教授团队研究成果(IF=7.5) | 基于MRI的放射基因组学标志物用于无创预测肝细胞癌中GPC3表达及肿瘤微环境
- 2026-05-09 09:24:22
这篇文章主要研究了如何利用MRI影像组学结合基因组学分析,无创预测肝细胞癌(HCC)中 GPC3 表达状态 及其相关肿瘤微环境特征。作者纳入多中心MRI队列,提取肿瘤及瘤周影像特征,建立机器学习模型,发现基于CE-T1WI和DWI的模型对GPC3预测具有较好性能。进一步结合TCGA和TCIA转录组数据进行放射基因组学分析,发现影像特征与缺氧、脂质代谢、HIF-1/PPAR通路密切相关,并筛选出10基因风险特征,可区分不同预后亚群。高风险患者表现出更强免疫浸润和更可能从免疫治疗中获益。总体上,这项研究提示MRI影像可以作为GPC3及肿瘤微环境的替代标志物,为肝癌精准分层和个体化治疗提供依据。

题目:基于MRI的放射基因组学标志物用于无创预测肝细胞癌中GPC3表达及肿瘤微环境
期刊:Journal of Translational Medicine(IF=7.5)
亮点思路整理
①无创预测GPC3表达:文章以MRI影像组学为切入点,尝试替代传统IHC检测,实现对肝细胞癌GPC3状态的术前无创预测,直接对应临床分层和GPC3靶向治疗需求。
②多中心+多模态增强可信度:研究纳入三中心MRI队列,并结合TCIA、TCGA数据,使用CE-T1WI与DWI及多种机器学习模型比较,结果显示联合序列模型表现最佳,说明多中心、多序列设计增强了模型稳健性。
③从“预测”走向“机制解释”:不仅停留在影像判别层面,还通过WGCNA和转录组分析,把影像特征与缺氧、脂质代谢及HIF-1/PPAR通路联系起来,解释了GPC3相关影像表型背后的生物学基础。
④连接预后与免疫治疗决策:作者进一步构建10基因风险特征,将患者分为高低风险组,并发现高风险组免疫浸润更强、预测免疫逃逸更低,提示该模型不仅能预测分子表达,还可能辅助预后判断和免疫治疗获益筛选。
主要结果
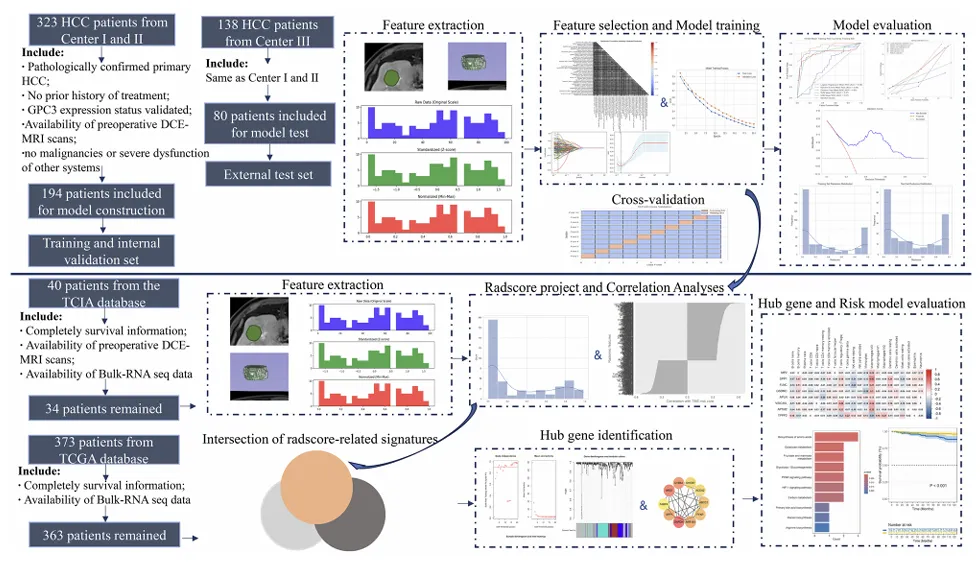
图1:整个研究的工作流程和注册过程。研究设计的示意图表示,说明多中心数据采集、DCE-MRI 分割和特征提取、多组学集成、预后模型开发和验证工作流程。关键步骤包括数据归一化、机器学习模型训练、WGCNA 模块分析以及生存和肿瘤微环境 TME 特征化。
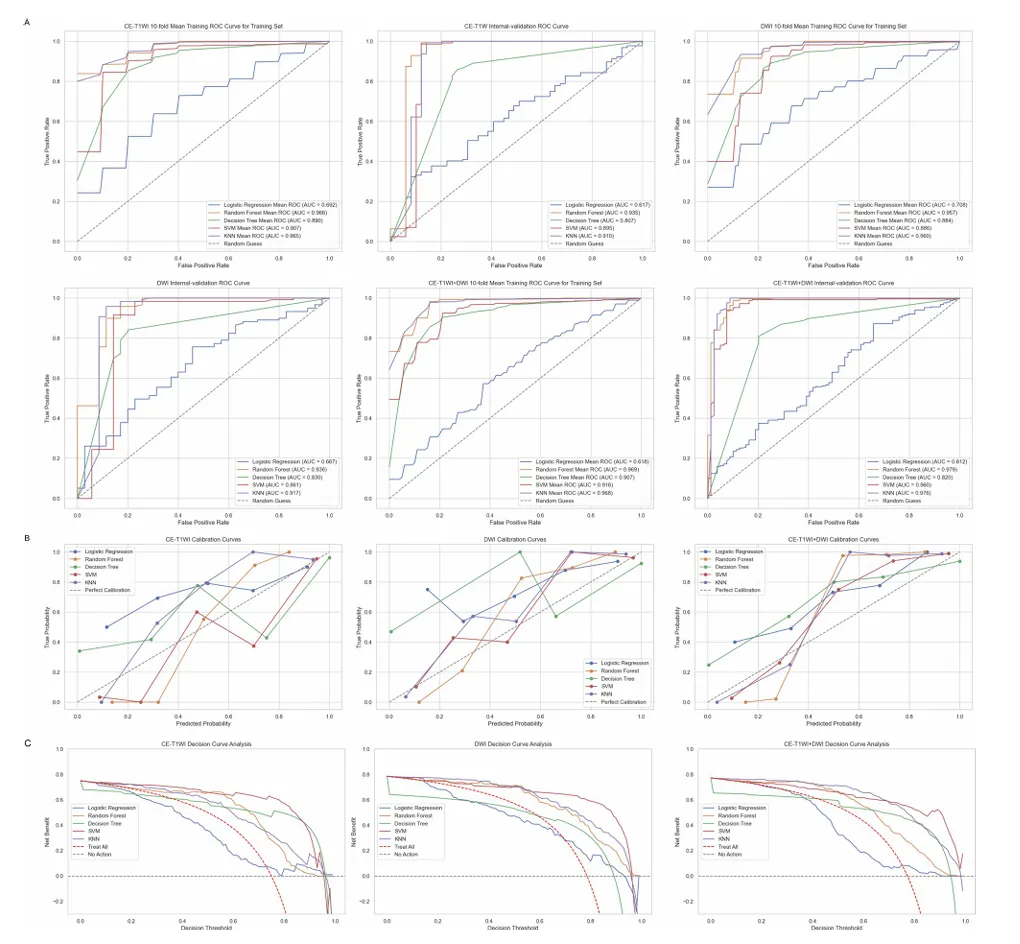
图 2 放射组学模型在交叉验证和内部验证集中的性能。(A) 各种分类器 (包括 LR、SVM、RF、KNN 和 dt) 的 ROC 曲线,分别在 CE-T1WI、DWI、集成序列的交叉验证和内部验证集中使用 10 倍交叉验证进行评估。(B) 校准曲线表明,集成序列中的 RF 模型与理想对角线紧密对齐,表现出优异的预测准确性。(C) DCA 表明,集成序列模型在临床相关决策阈值 (0.2-0.8) 上始终产生最高的净效益,优于 “治疗全部” 策略。
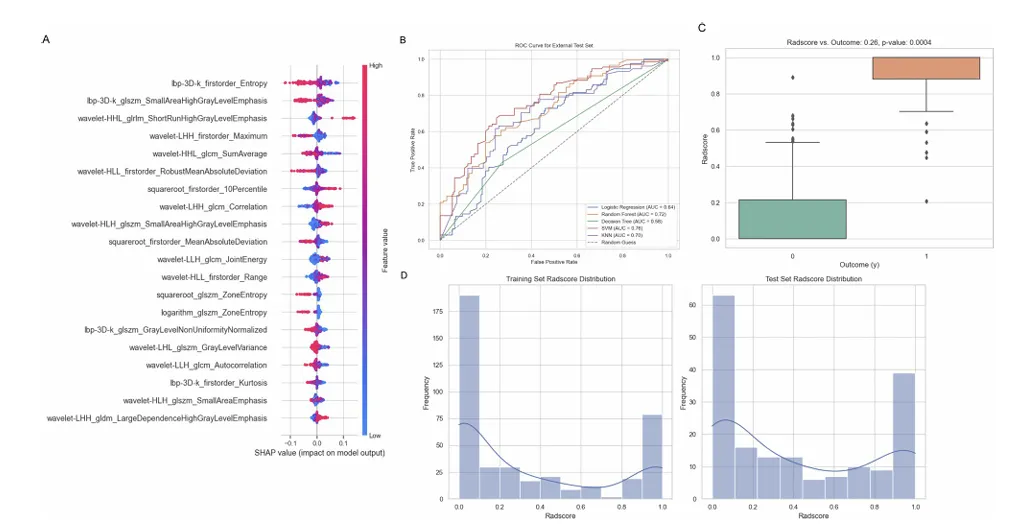
图 3 特征解释和外部验证。(A) Shap 分析确定了有助于 GPC3 预测的关键放射学特征。(B) 外部验证队列的 ROC 曲线,其中 SVM 表现最好 (AUC = 0.756),RF 表现出中等程度的泛化性 (AUC = 0.721)。(C) Spearman 相关性分析表明 radscore 与 GPC3 表达之间存在强相关性 (R = 0.78,p < 0.05)。(D) radscore 分布确认了高风险和低风险组的稳健分层。
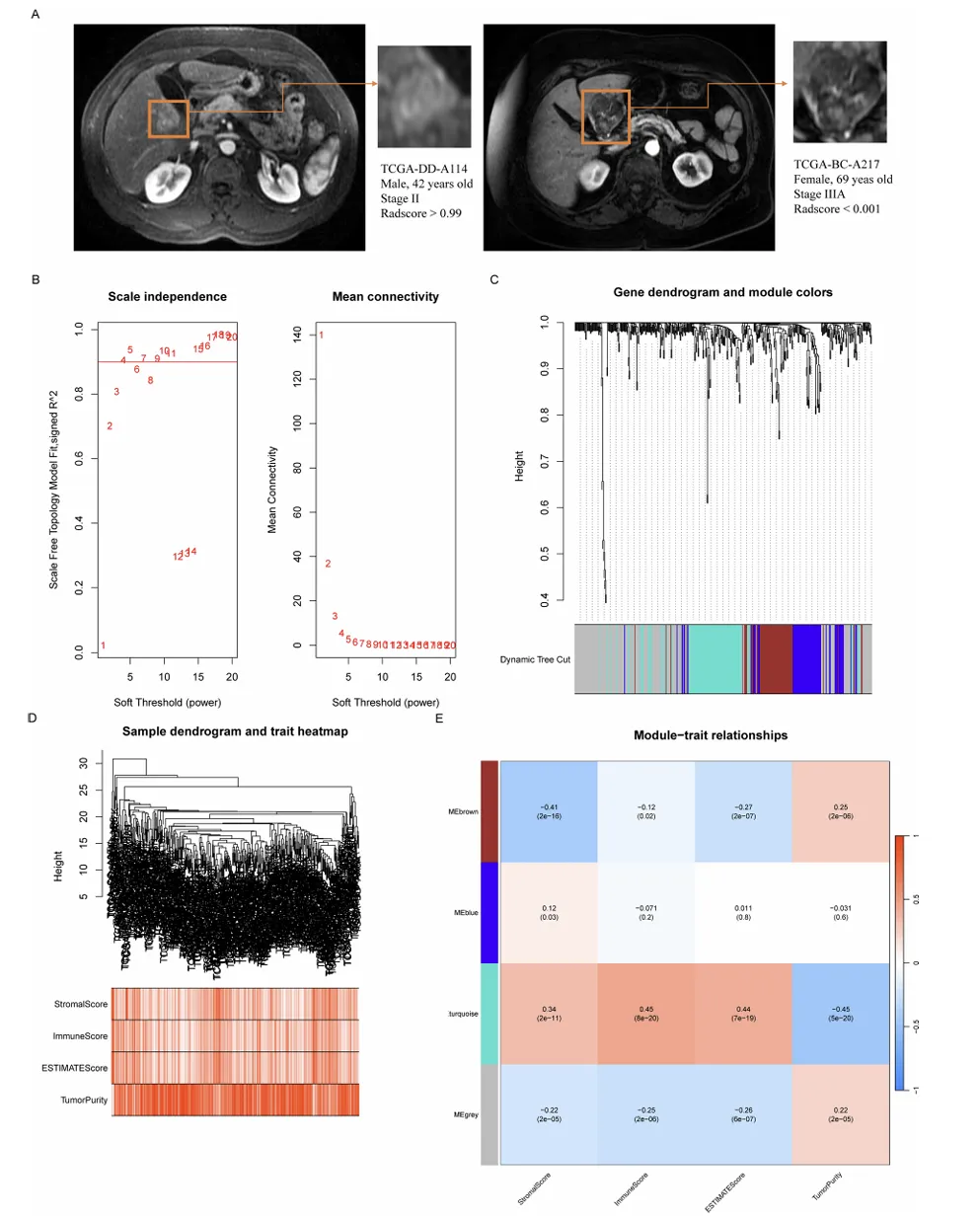
图 4 测试集中预测 K-M 曲线与实际 K-M 曲线的比较。5 年内的进展:a 对于测试集 (对数秩检验 p 值=0.5029,HR=0.85);b 不需要术后干预的患者 (Rényi 检验 p 值=0.4636,HR=1.48);c 需要术后干预的患者 (对数秩检验 p 值=0.0580,HR=0.56)。5 年内的死亡率:d 对于测试集 (Rényi 检验 p 值=0·2321,HR=1.10);e 不需要术后干预的患者 (Renyi 检验 p 值=0.3091,HR=1.76);f 需要术后干预的患者 (log 秩检验 p 值=0.5253,HR=0.81)。HR 风险比 (log 秩)。
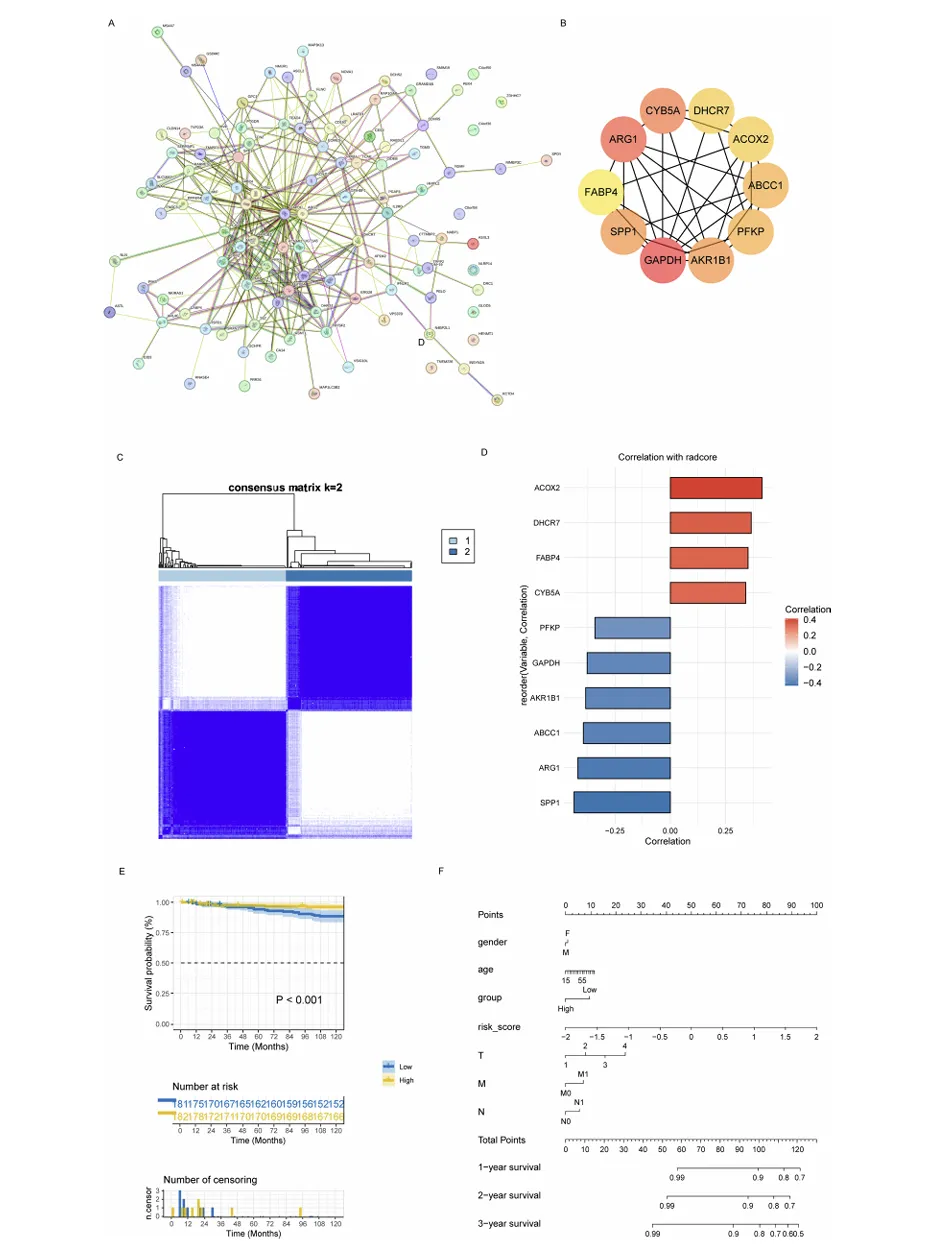
图 5 解释的病理特征。a 5 年进展和 5 年死亡的热点数量在患者和幻灯片水平的比较。P>D:5 年进展的热点数量超过 5 年死亡 (患者:101/125(80.8%);幻灯片:369/536(68.8%));P=D:5 年进展的热点数量与 5 年死亡相当 (患者:17/125(13.6%);幻灯片:114/536(21.3%));P<D:5 年进展的热点数量少于 5 年死亡 (患者:7/125(5.6%);幻灯片:53/536(9.9%))。b 测试集中 NSCLC 患者组织学类型的构成。c SCC 患者 WSI 上热点的分布,以及样本区域的扩大。红箭头:有丝分裂图;绿箭头:放大和奇异核。d NMA 亚型的实际和预测结果。现实:NMA 亚型患者的数量;预测:该亚型内具有风险热点的患者数量。MPA(e)、SPA(f)、LPA(g) 患者 WSI 上热点的分布,与样本区域的扩大。h APA 患者 WSI 上热点的分布。扩大的区域表现出小腺体 (上侧) 和大腺体 (下侧) 的特征。i 基质区域被确定为风险热点。jPPA 患者 WSIs 上的热点分布,以及样本区域的扩大。SCC 鳞状细胞癌、NMA 非粘液性腺癌、SPA 实体腺癌、MPA 微乳头腺癌、LPA 脂质性腺癌、APA 腺癌、PPA 乳头腺癌。
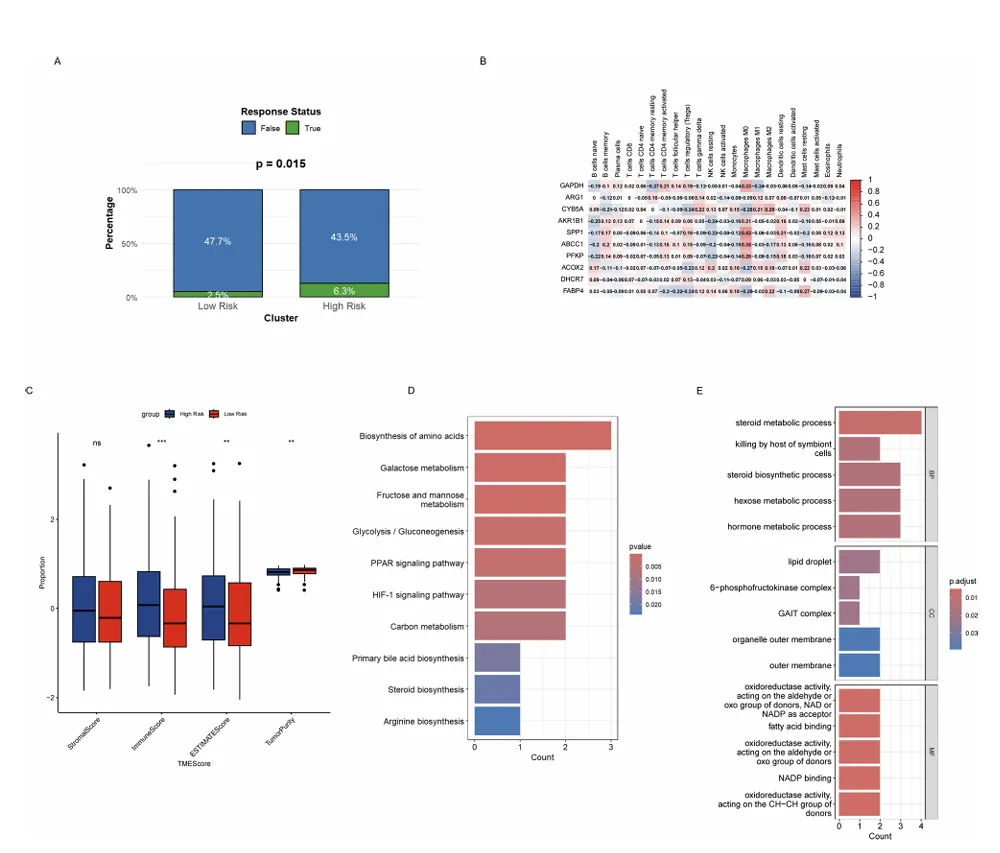
图 6 免疫相关反应和富集分析。(A) 潮汐评分 (显示高风险组具有较低的潮汐评分,这与更好的反应相关)。(B) 来自 CIBERSORT 分析的中心基因与 22 个肿瘤浸润性免疫细胞亚群之间相关性的热图。(C) 高风险组和低风险组之间的 StromalScore、ImmuneScore、ETIMATEScore 和 tumorPurity 的比较。(D) 中心基因的 KEGG 途径富集分析,突出显示参与代谢重编程的途径,如糖酵解/糖异生、HIF-1 和 PPAR 信号传导。(E) 进行富集分析,显示中心基因参与类固醇代谢和氧化还原酶活性等过程。
总结
这篇研究围绕肝细胞癌中GPC3的无创预测展开,构建了基于MRI影像组学的放射基因组学模型。作者利用多中心MRI数据,结合CE-T1WI和DWI序列,较好地预测了GPC3表达状态,并在外部队列中进行了验证。进一步结合TCGA/TCIA转录组数据,研究发现影像特征不仅与GPC3表达相关,还与缺氧、脂质代谢以及HIF-1、PPAR等通路激活密切相关。作者还建立了10基因风险特征,可区分不同预后亚群,并提示高风险患者可能具有更高免疫治疗获益。整体来看,这篇文章的价值在于将影像表型、分子机制、肿瘤微环境和临床治疗决策联系起来。
参考文献:
Gao Y, Liu D, Miao Y, Lou Z, Luo Z, Li Y, Cai H, Zhu Y, Chen S. Radiogenomic MRI biomarkers for noninvasive prediction of GPC3 expression and tumor microenvironment in hepatocellular carcinoma. J Transl Med. 2025 Dec 11;24(1):198. doi: 10.1186/s12967-025-07504-0. PMID: 41382212; PMCID: PMC12903299.
往期回顾
