南京农业大学吕凤霞 朱萍|重塑醛酮还原酶结合口袋以提升立体选择性和催化活性
- 2026-05-07 21:28:39

导语
生物修复策略被认为是一种有前景且环境友好的替代方法,可用于消除饲料和食品中的脱氧雪腐镰刀菌烯醇(DON)污染,但目前可用的直接且高效的酶催化解毒方法仍然较少。在本研究中,我们通过逐步基因挖掘的方法,从Devosia菌株A6-243中鉴定出一种具有DON降解能力的醛酮还原酶(AKR6D2)。研究发现,AKR6D2在还原3-酮基脱氧雪腐镰刀菌烯醇(3-keto-DON)的C3位羰基氧方面具有优异的热稳定性,但其立体选择性较差(生成3-表-脱氧雪腐镰刀菌烯醇(3-epi-DON)的对映体过量值为44.97%),从而限制了其实际应用。通过重塑AKR6D2的底物结合口袋,获得了突变体W21A/G53N,该突变体表现出显著提升的催化活性(提高330倍)和优异的立体选择性(3-epi-DON的对映体过量值>99%)。基于分子动力学模拟的分析结果,W21A/G53N-3-keto-DON的proR构象更有利于形成反应前态,从而生成R构型产物。本研究表明,经工程改造的AKR6D2是一种用于去除受污染食品和饲料中DON的高效生物催化剂。
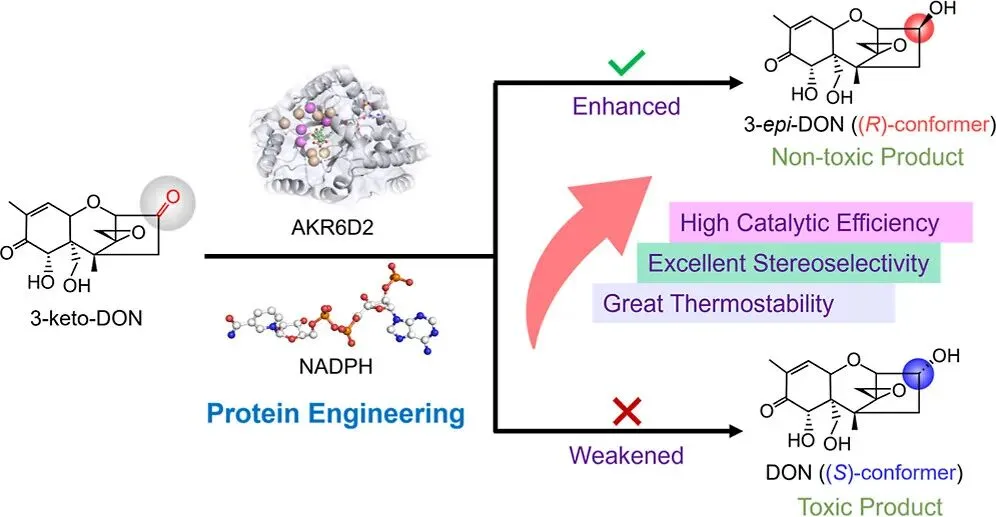

本研究旨在拓展脱氧雪腐镰刀菌烯醇(DON)降解酶资源,并为食品和饲料中DON污染的生物修复提供高效解决方案。研究者从 Devosia 菌株 A6-243 基因组中筛选出8个注释为醛酮还原酶(AKRs)的候选基因。考虑到底物3-keto-DON具有体积庞大的四环倍半萜结构,对酶活性口袋的空间要求较高,研究通过 AlphaFold 3 对蛋白三维结构进行预测,并结合 Autodock 分子对接对底物与辅酶 NADPH 的结合模式进行系统评估。基于底物结合口袋体积和结合能等关键参数,筛选出AKR1、AKR2、AKR5和AKR6作为潜在候选酶。进一步通过异源表达与HPLC分析验证其功能,结果显示仅AKR6D2具备有效催化3-keto-DON转化能力,可生成3-epi-DON及少量DON。随后对其酶学性质进行系统表征,发现该酶在40 °C、pH 6.5条件下活性最高,并在较宽pH范围及不同温度下表现出优异稳定性。此外,底物谱分析表明AKR6D2能够催化多种醛酮底物,但对体积较大的3-keto-DON活性较低,且立体选择性不足,表明其天然状态下尚不适用于工业应用。
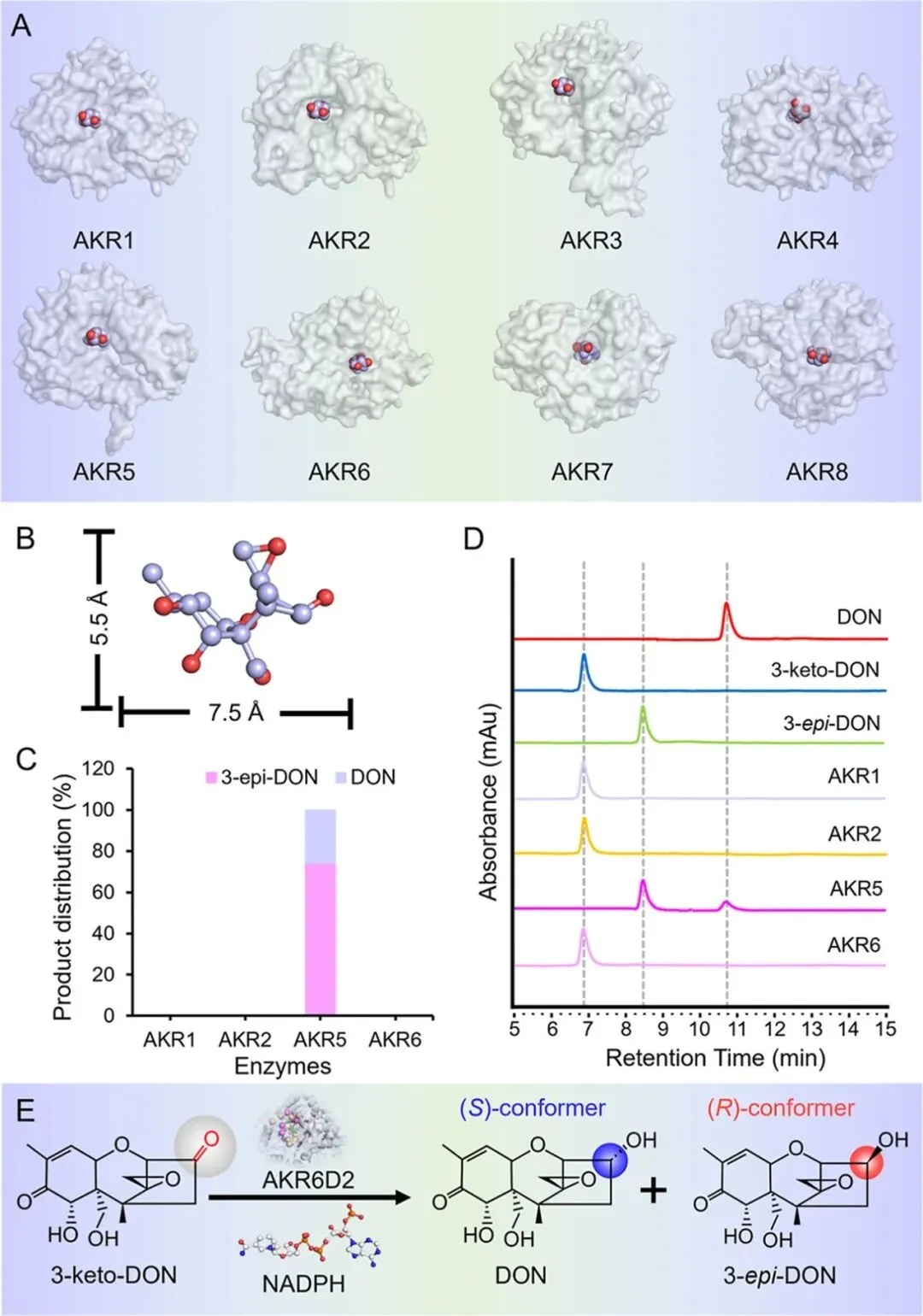
图1|候选酶筛选与功能验证。
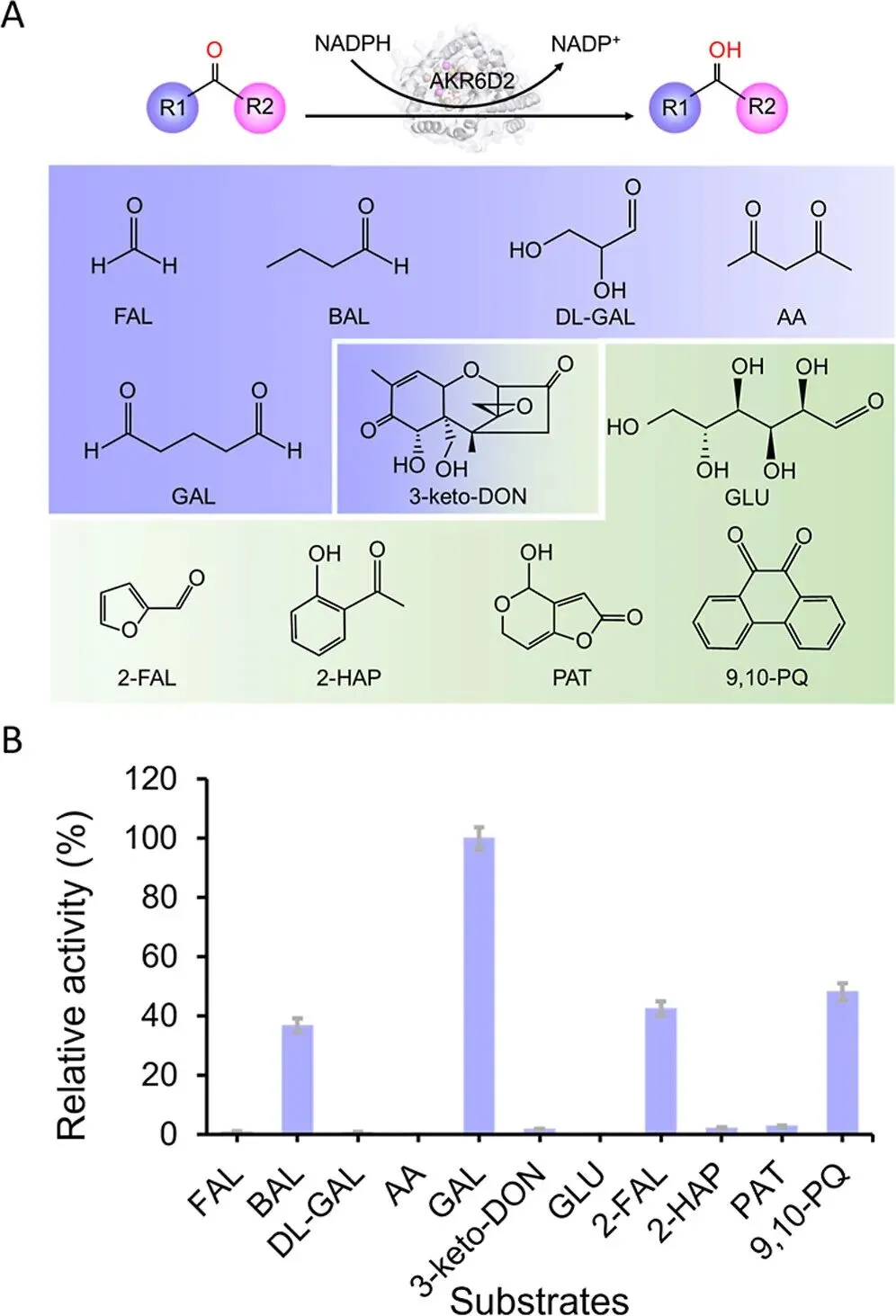
图2|AKR6D2的酶活性及底物特异性分析。
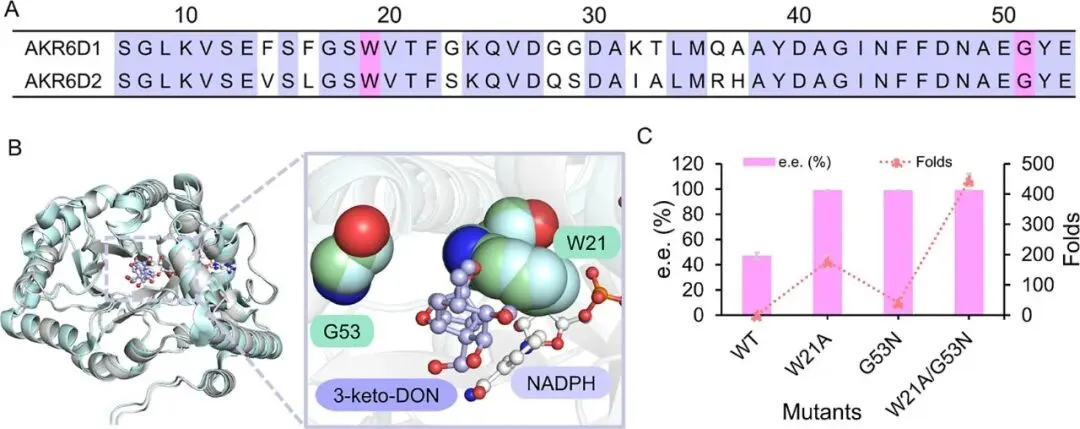
针对AKR6D2在催化3-keto-DON过程中的低活性与低立体选择性问题,研究采用结构导向的半理性设计策略对酶进行改造。首先基于底物结合位点周围4 Å范围内的关键残基进行丙氨酸扫描突变,筛选出对催化性能具有重要影响的位点,其中W21和G53被鉴定为调控酶活性与立体选择性的关键残基。进一步对这两个位点进行饱和突变,发现多个突变体(如W21G、G53Y、G53N)均显著提高了R-选择性,同时在不同程度上增强了催化活性。在此基础上,通过组合突变构建双突变体W21A/G53N,该突变体表现出显著提升的催化性能,其催化效率较野生型提高约330倍,同时立体选择性达到>99% ee。动力学参数分析表明,该突变体不仅kcat显著提高,Km也明显降低,从而使kcat/Km大幅提升,表明底物结合能力与催化转化效率均得到优化。该结果说明通过精确调控关键位点,可以有效实现酶活性与立体选择性的协同提升,避免传统酶工程中常见的“权衡效应”。
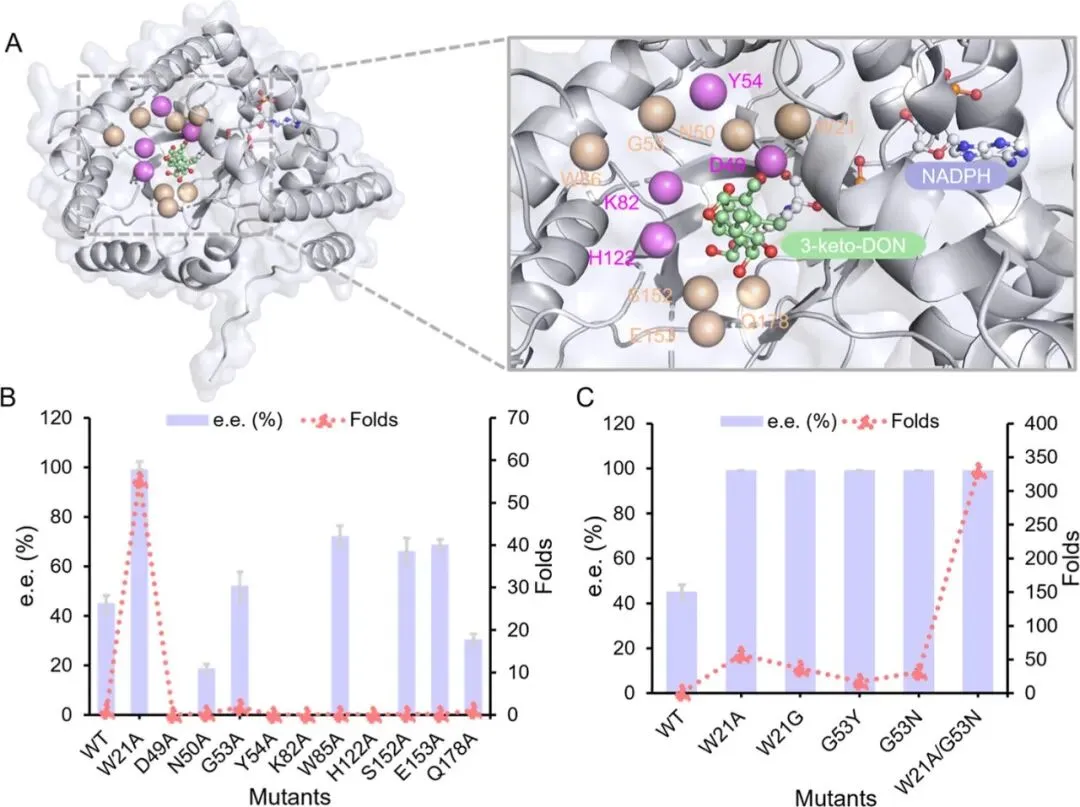
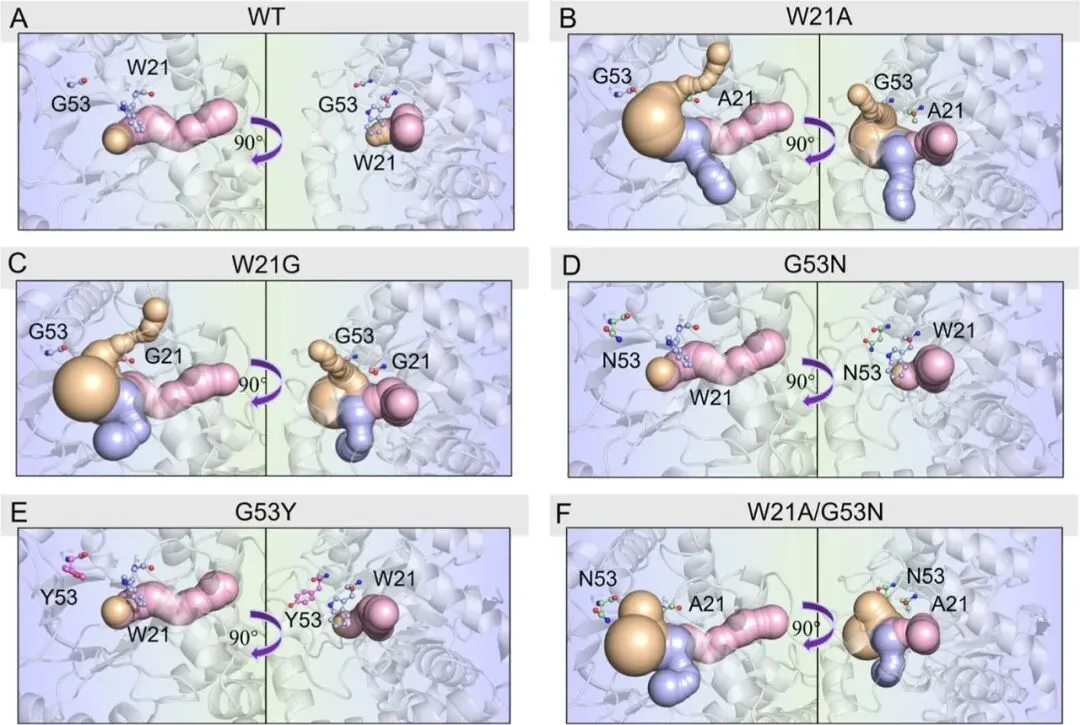

为了深入理解突变对催化性能提升的分子机制,研究结合分子对接、底物通道分析(CAVER)以及结合口袋构型分析对酶结构进行了系统解析。结果表明,野生型AKR6D2存在较狭窄的底物进入通道,限制了大体积底物3-keto-DON的进入与合理构象定位。而在W21A、W21G及W21A/G53N等突变体中,底物通道显著拓宽,甚至形成新的迁移通道,从而提高底物进入与产物释放效率。同时,突变还导致底物结合口袋体积增大并发生形状重构,为底物提供更高的构象自由度,有利于催化反应的发生。另一方面,G53突变通过引入新的氢键或π–π相互作用(如与W85的相互作用),有效限制底物在活性中心中的构象波动,从而提高底物取向的精准性并增强立体选择性。分子动力学模拟进一步表明,突变体更容易形成满足关键距离约束的“预反应态”,尤其有利于生成R构型产物(3-epi-DON),从动态角度揭示了催化效率与选择性提升的本质原因。
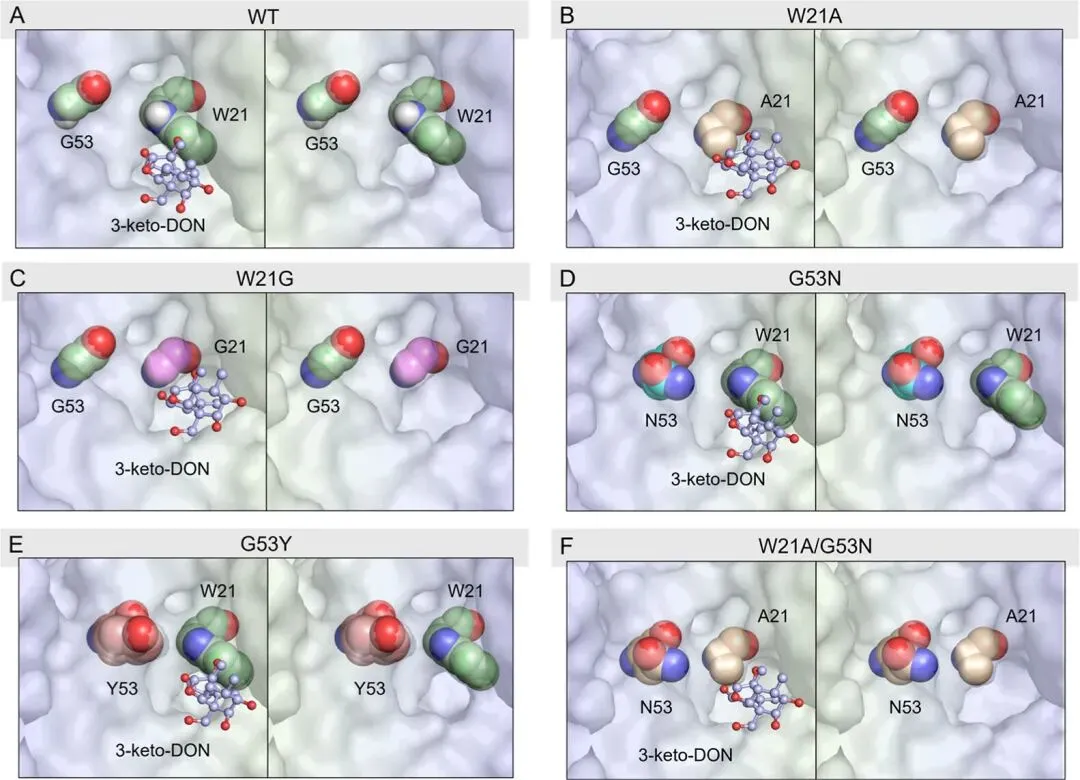
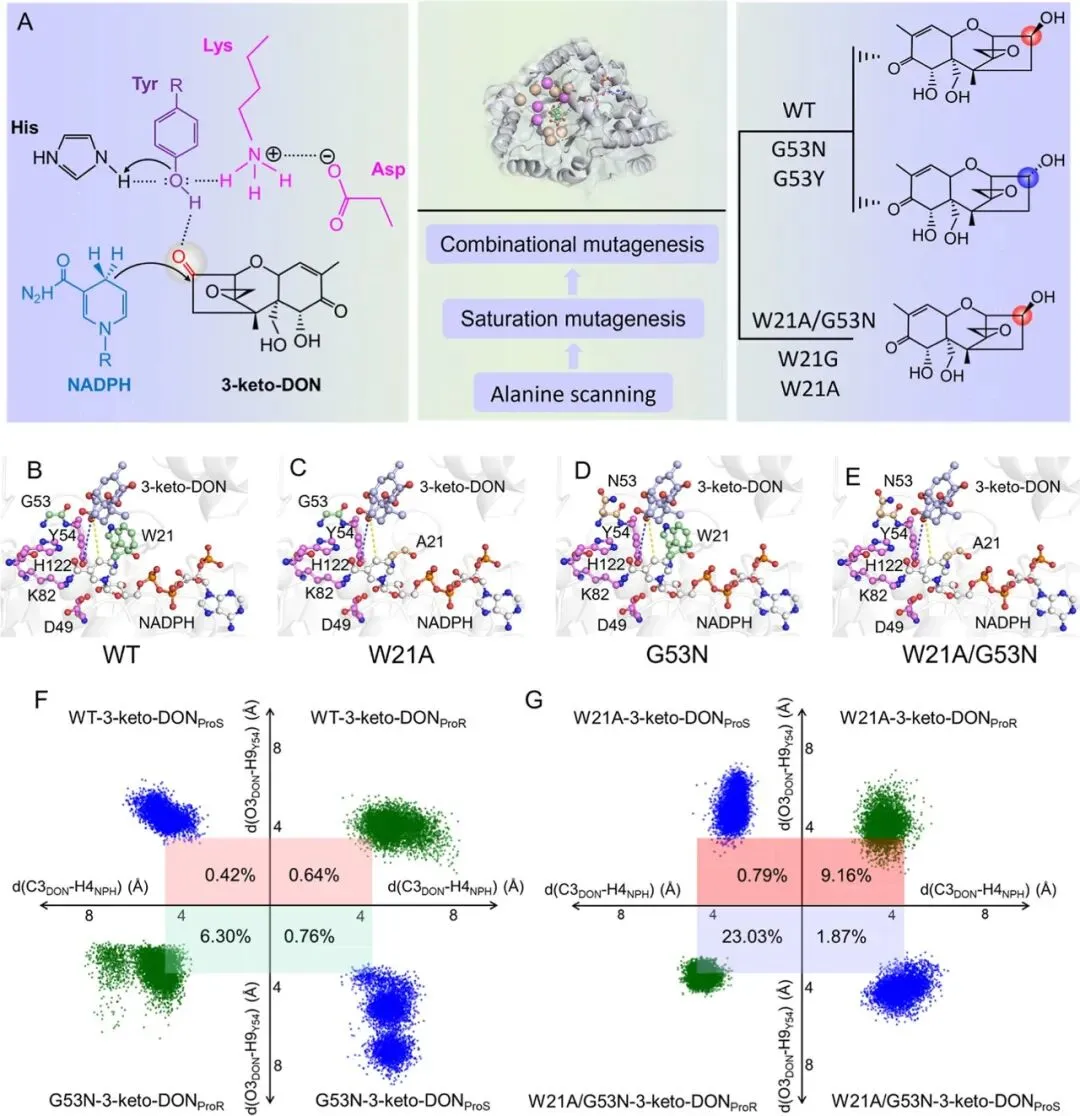

在机制研究中,作者进一步提出并验证了“色氨酸门控(tryptophan gating)”这一关键调控机制。野生型酶中,W21的体积较大的疏水侧链在底物通道入口处形成显著空间位阻,类似“闸门”控制底物与产物的进出。在分子动力学模拟过程中,该“门控”呈现出动态开闭行为,在一定程度上限制了底物传输效率。而当W21突变为Ala或Gly后,该门控结构被破坏,通道显著扩展,从而有效降低空间阻碍,促进底物进入和产物释放,提高整体催化效率。进一步在同源酶AKR6D1中进行对应位点突变验证,发现W21A/G53N同样显著提升催化效率(最高达446倍)并实现高立体选择性,证明该门控机制及关键位点调控策略具有良好的普适性。该研究不仅为DON生物脱毒提供了高效酶工具,也为通过调控通道入口残基实现酶性能优化提供了通用设计思路。
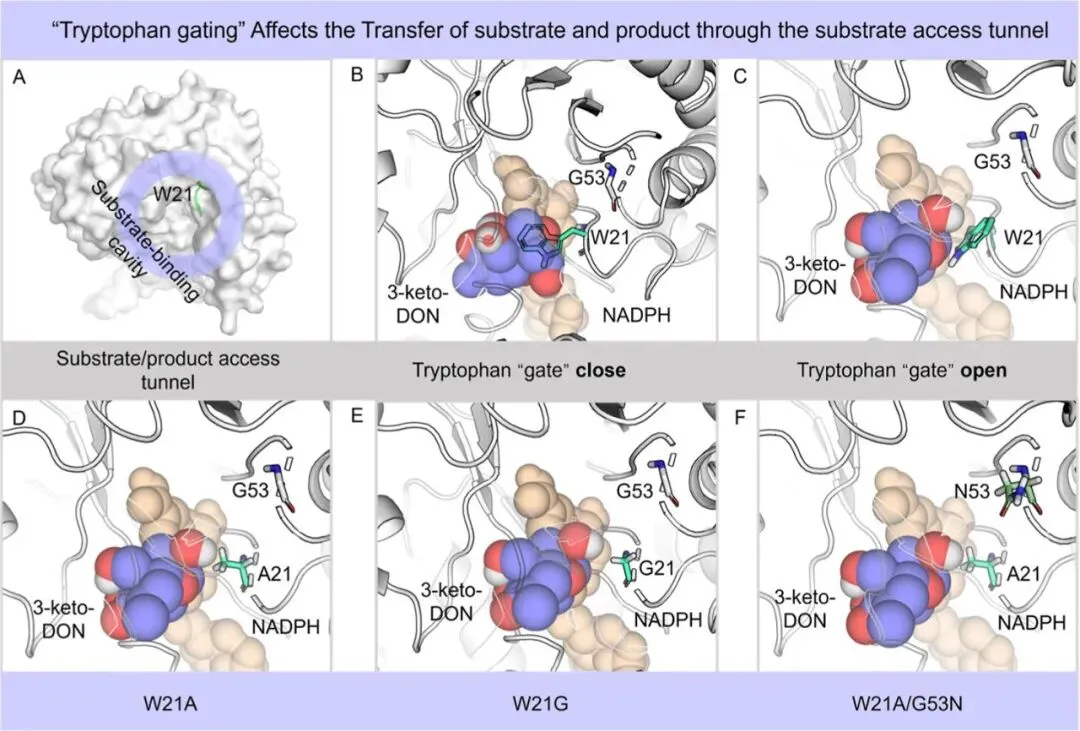
1. 提出“通道门控调控”新机制:首次在AKR6D2中系统揭示色氨酸门控(W21)对底物传输与催化性能的关键调控作用。
2. 实现活性与选择性的协同提升:通过W21A/G53N双突变,成功突破酶工程中活性与立体选择性难以兼顾的瓶颈。
3. 构建结构-动力学协同解析框架:结合分子对接、通道分析与分子动力学模拟,系统阐明突变提升催化性能的分子机制,为理性酶设计提供新范式。


南京师范大学 张幸|中国药科大学 乔梦|远端突变也能“调控全局”?远端别构网络工程驱动底物通道重塑,实现β-熊果苷高效生物合成
中国科学院上海有机化学研究所 洪然|华东理工大学 郁惠蕾 | 两种酶“接力氧化”:精准C–H功能化驱动红花木碱生物碱合成
【直通作者】广西科学院潘丽霞团队挖掘高稳定持续性内切葡聚糖酶DbCel5A,生物质高效转化潜力显著
溦时光
感谢关注,欢迎交流
欢迎添加微信“Helion-682”进微信学术交流群
谢谢支持,感谢转发和点赞

