Nature Plants | 南京农大张正光/张海峰团队揭示稻曲病菌操控水稻发育与免疫
- 2026-05-22 17:15:48
Nature Plants | 南京农大张正光/张海峰团队揭示稻曲病菌操控水稻发育与免疫
稻曲病菌(Ustilaginoidea virens)病是全球水稻产区日益严重的真菌病害,不仅造成严重的产量损失,其产生的真菌毒素还威胁粮食安全。稻曲病菌采取一种独特的花器官特异性侵染策略:它定殖于颖花内部,通过干扰受精过程导致不育,最终形成俗称“稻曲”的菌球。尽管已知稻曲病菌在侵染早期就能诱导水稻灌浆基因表达以获取营养,但其如何从机制上同时破坏水稻受精并抑制寄主免疫,这一直是该领域悬而未决的“认知缺口”。2026年3月23日,南京农业大学植物保护学院张正光教授与张海峰教授团队在国际顶尖植物学期刊 《Nature Plants》 上在线发表了题为“Rice false smut fungus hijacks rice lipid signalling to manipulate floret development and immunity”的研究论文,首次鉴定到稻曲病菌(Ustilaginoidea virens)分泌的一种关键效应蛋白 Sxp1,揭示了其通过靶向水稻质外体脂质转运蛋白 LTPL113,干扰磷脂酸(PA)和磷脂酰丝氨酸(PS)介导的脂质信号通路,从而精准调控水稻颖花发育并抑制植物免疫的分子机制。这一发现不仅阐明了花部病原真菌如何利用生殖组织获取营养,还为解决水稻抗病性与产量平衡的“生长-防御权衡”难题提供了重要的理论指导。 
研究团队首先通过室内表型分析验证稻曲病菌侵染对水稻育性的影响,对比健康稻穗与染病稻穗发现,染病稻穗空秕率高达80.1%,远高于健康稻穗的30.4%;通过时间梯度观察病菌侵染过程,发现侵染初期菌丝缠绕花丝,后期逐步包裹花药与整个花器官,且随着侵染进程推进,花粉活力持续下降,侵染后期花粉几乎完全皱缩失活。基于该结果提出假说:稻曲病菌在侵染早期通过降低花粉活力阻止水稻受精,从而获取持续营养完成定殖。 为筛选稻曲病菌关键效应子,研究团队对营养限制、营养丰富及体内侵染三种条件下的病菌分泌组进行质谱分析,结合主成分分析、火山图与韦恩图筛选候选效应子,最终锁定9个侵染早期高表达的效应子;通过本氏烟瞬时表达与辣椒疫霉(P. capsici)侵染实验,鉴定出Uv_4853(命名为Sxp1)可显著增强病原菌侵染,且其分泌型信号肽是发挥免疫抑制功能的关键;酵母转化酶分泌实验、亚细胞定位检测证实Sxp1为胞外分泌蛋白,侵染水稻花器官后定殖于质外体。 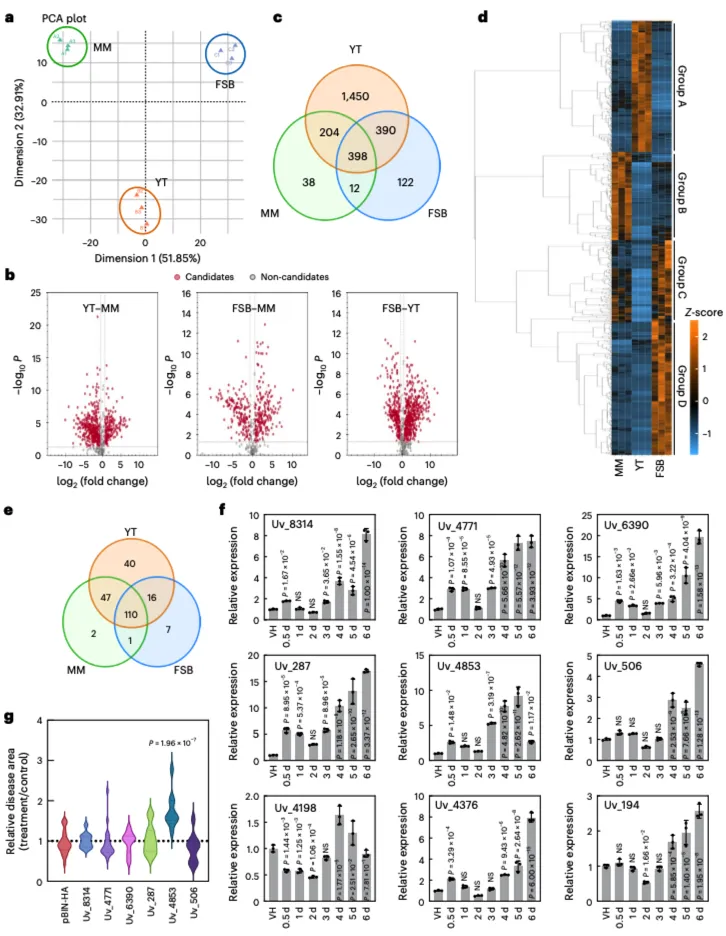
分泌组筛选鉴定Sxp1为稻曲病菌关键胞外免疫抑制效应子 构建Sxp1过表达水稻株系(OE-SXP1),表型鉴定显示过表达株系株高无显著变化,但空秕率超97%,花丝粘连、花粉活力大幅降低;构建Sxp1敲除突变体Δsxp1与回补株系,发现Δsxp1菌株致病力显著减弱,稻穗上病菌生物量与稻曲球数量减少,且对水稻花粉活力的损伤大幅缓解;分子水平检测表明,Sxp1可抑制几丁质诱导的MAPK激活与ROS活性氧爆发,过表达Sxp1的水稻对稻瘟菌、纹枯菌敏感性提升,抗病相关基因表达量下调。 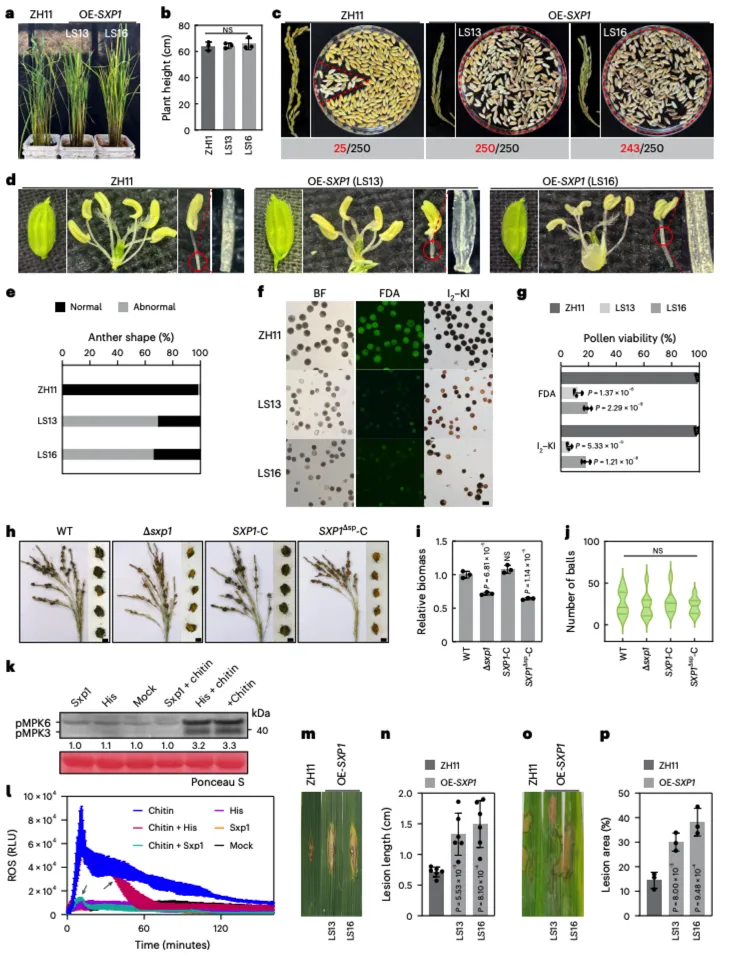
稻曲病菌Sxp1调控水稻花器官发育与免疫应答 利用酵母双杂交文库筛选,鉴定出水稻脂质转运蛋白LTPL113为Sxp1互作蛋白,进一步通过酵母双杂交、免疫共沉淀、微量热泳动(MST)与荧光素酶互补实验,证实Sxp1与LTPL113存在特异性相互作用;亚细胞定位与蛋白免疫印迹检测显示,LTPL113同样定殖于胞外区域,与Sxp1共定位,明确二者在水稻质外体发生互作。 
LTPL113与Sxp1发生物理互作 通过CRISPR-Cas9构建LTPL113敲除株系(ltpl113)与过表达株系(OE-LTPL113),表型分析显示两类株系株高、千粒重无明显差异,但敲除株系空秕率达48%,花药畸形、花粉活力显著降低,过表达株系育性缺陷相对轻微;免疫检测发现,过表达株系几丁质诱导的活性氧积累与MAPK激活水平升高,对稻曲病菌、稻瘟菌、纹枯菌抗性增强,敲除株系则表现为免疫缺陷、抗病性大幅下降。 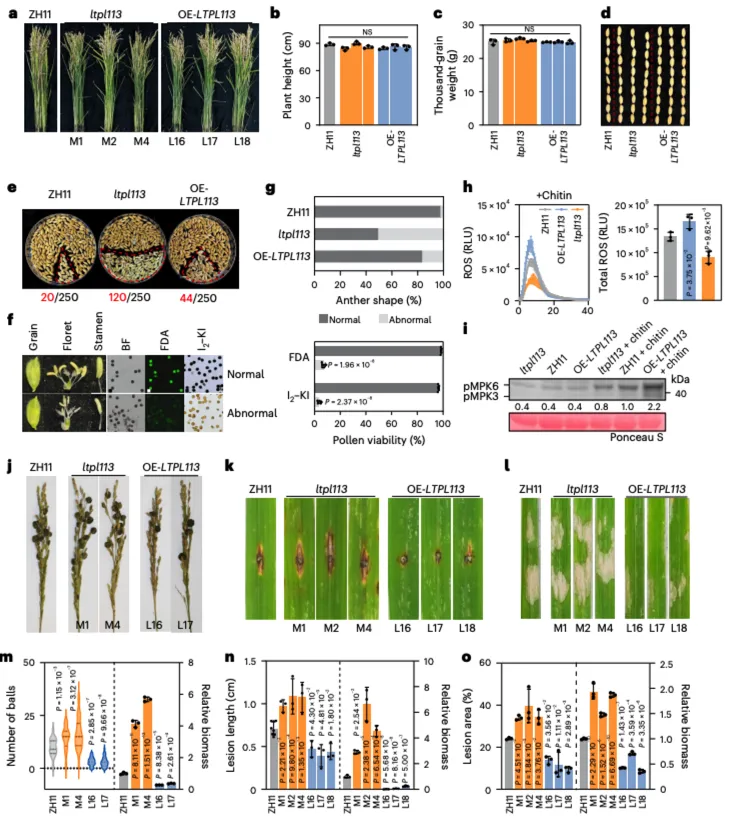
LTPL113对水稻花器官发育与免疫应答至关重要 脂质结合实验表明,LTPL113可特异性高亲和力结合磷脂酸(PA)与磷脂酰丝氨酸(PS),对其他磷脂结合力较弱;功能验证发现,PA、PS单独无法诱导活性氧爆发,但可增强葡聚糖诱导的免疫应答,该增强效应依赖LTPL113;外源施加PA、PS可提升水稻对稻曲病菌的抗性,脂质组学检测显示,ltpl113花器官中PA含量显著降低,Δsxp1侵染的水稻花器官中PA、PS含量高于野生型菌株侵染组。这些数据表明LTPL113通过与脂质结合来促进PAMP触发的免疫反应,从而增强水稻的免疫力;而Sxp1可能拮抗这种脂质介导的防御途径。 
LTPL113通过脂质结合活性增强水稻免疫 利用扫描电镜观察花粉结构,发现ltpl113突变体62%的花粉外壁发育缺陷,表面光滑、颗粒状突起稀疏,而野生型与LTPL113过表达株系花粉外壁结构正常;Sxp1过表达株系花粉表型与ltpl113突变体高度一致,93%花粉外壁畸形,证实LTPL113是花粉外壁形成的关键因子,Sxp1通过拮抗LTPL113功能破坏花粉外壁发育。 
LTPL113调控生殖发育阶段花粉外壁形成 竞争性结合实验显示,Sxp1可显著降低LTPL113与PA、PS的结合亲和力;通过蛋白同源建模与分子对接,定位二者互作关键位点,构建位点突变体后验证发现,突变后的LTPL113无法与Sxp1和脂质结合,突变型Sxp1也丧失与LTPL113的互作能力;生物层干涉实验表明,Sxp1通过竞争性结合LTPL113阻断PA介导的免疫,同时直接结合PS干扰其免疫信号传导,实现双重免疫抑制。 
Sxp1干扰LTPL113脂质结合抑制免疫 将互作位点突变的LTPL113转入ltpl113突变体构建回补株系,表型检测发现,回补株系株高、千粒重与野生型一致,但花器官发育、花粉活力及免疫抗性缺陷未得到恢复,进一步证实LTPL113与Sxp1的互作位点是其发挥发育调控与免疫功能的关键区域。 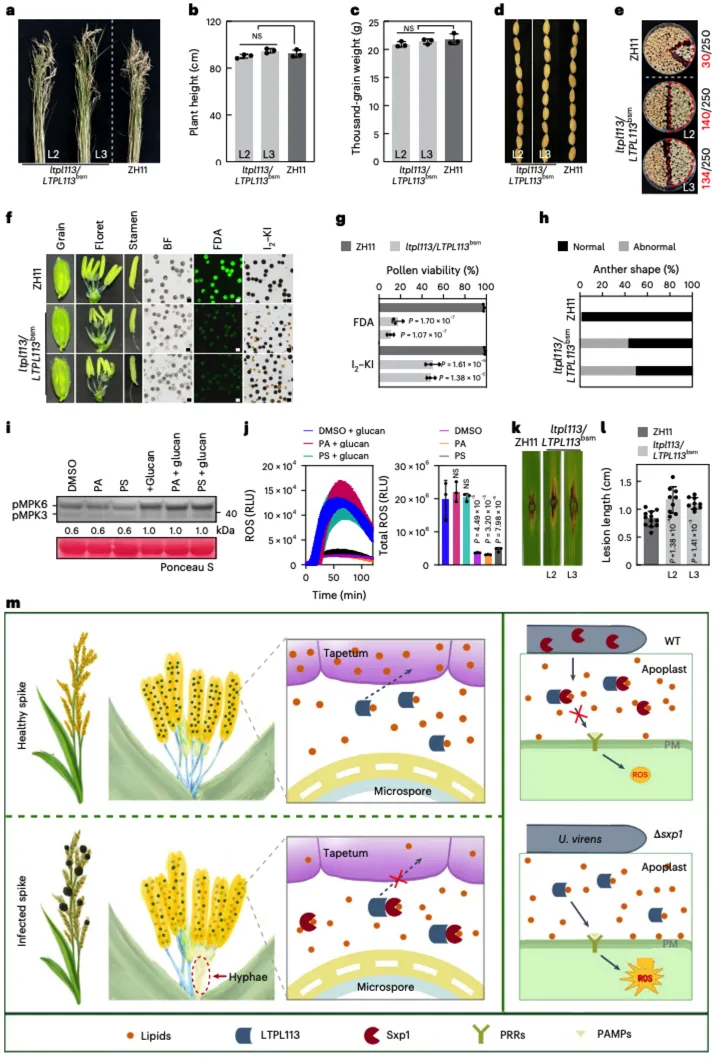
脂质结合缺陷的 LTPL113 bsm无法挽救ltpl113突变体的发育和免疫缺陷 研究构建了一个精巧的病原菌致病模型:稻曲病菌分泌 Sxp1,停靠在 LTPL113 上, 阻断 LTPL113 对 PA/PS 脂质分子的转运,导致花粉发育停滞(产生空瘪粒)并关闭寄主免疫响应(利于真菌扩张)。首次证明了稻曲病菌通过操纵寄主脂质信号这一非传统路径,同时实现“发育控制”与“免疫抑制”的双重目标。未来通过精准修饰 LTPL113 的结合位点,有望创制出既不减产又能高效抵御稻曲病的水稻新品种,为水稻抗稻曲病分子育种提供了关键靶标与理论依据,对保障水稻粮食安全具有重要的应用价值。 文献简报 Nature Plants | 中国农大团队揭示小麦耐热负调控基因TaHST2 Mol Plant | 崖州湾国家实验室钱前/郑晓明/王克剑团队揭示无融合生殖杂交稻产量稳定新策略 中法团队联合突破!CRISPR编辑AtRING1揭秘RAWUL结构域调控PRC1转录抑制的核心机制 PBJ | 西南大学吕典秋/荐红举团队揭示 m6A 甲基化调控马铃薯耐盐性的新机制 《Science》封面 | 我国科学家破解水稻驯化谜题,培育出“长寿水稻” Nature Plants | 中国科大张志勇团队揭示ZmMYB127调控玉米胚乳灌浆提升产量与品质 JIPB | 中国农大吴健团队建立百合高效遗传转化与基因编辑体系:转化周期缩短3-4倍 福建师范大学登 Nature!揭示植被在气候变暖下的生态系统特异性驱动 PBJ | 北京农学院刘子妍/段留生团队揭示SlMYB17拮抗SlCBF通路负调控番茄耐寒性 【Plant Commun.】 西北工业大学蔡晶解析洋葱近完整基因组,揭秘起源进化与育种密码 Advanced Science | 突破传统模型!中科院团队揭秘植物代谢组调控真菌生活史策略的全新机制










论文链接:https://doi.org/10.1038/s41477-026-02260-5
本文来自网友投稿或网络内容,如有侵犯您的权益请联系我们删除,联系邮箱:wyl860211@qq.com 。

