【IF=11.4】南京大学医学院顾宁/朱玉敏团队:多组学揭秘邻苯二甲酸酯通过ARF6-铁死亡-EMT轴促子宫内膜异位症新机制
- 2026-04-16 03:49:11

如果你也在愁没明确环境暴露与疾病的微观机制、缺多组学数据整合思路、难解析关键分子通路与细胞表型关联,不如换个思路,用多维生信挖掘(多组学分析、机器学习、分子对接、单细胞/空间转录组)+机制创新(关键基因识别、通路轴构建、特异性细胞转化模型)杀出重围!
就像这篇聚焦“邻苯二甲酸酯-铁死亡-EMT-子宫内膜异位症”的研究——通过整合bulk RNA-seq、scRNA-seq、空间转录组数据,用12种机器学习算法锁定关键铁死亡相关基因ARF6,构建“Lumenal+Ciliated→Fibros”上皮-间质转化模型,最终提出“PAEs-铁死亡-EMT-EM”致病轴,从“宏观关联”深挖到“微观机制”。你的课题若涉及环境污染物-疾病关联、分子通路-细胞表型交互或缺乏体内外实验条件,不妨借鉴这种“生信全景扫描+机制精准定位”的思路。
你的课题是否适合类似“环境暴露-多组学挖掘-关键分子-通路轴-细胞模型”的全链条解析路径?欢迎咨询评估~

中文标题:邻苯二甲酸盐暴露促进子宫内膜异位症的机制研究:基于铁磷灭症的视角
发表期刊:Journal of Hazardous Materials
发表时间:2026年4月
影响因子:11.3/Q1
核心问题:邻苯二甲酸酯(PAEs)作为典型环境内分泌干扰物,流行病学已证实其与子宫内膜异位症(EM)风险相关,但PAEs如何通过铁死亡(ferroptosis)和上皮-间质转化(EMT)驱动EM进展的微观机制尚未明确。
1.1 PAEs的暴露与危害
来源与迁移:PAEs是工业塑化剂,因与聚合物无稳定共价键,易从塑料制品中释放至空气、水、土壤(大气浓度0.004-33,851 ng·m⁻³,水体0.01-71,980 ng·L⁻¹,土壤0.001-820 mg·kg⁻¹)。
人体暴露:通过吸入、食入、皮肤接触累积,具有生殖毒性,尤其损害女性生殖健康(如干扰卵巢激素合成、损伤卵母细胞)。
1.2 EM的病理特征与负担
定义:子宫内膜样组织在宫腔外异常植入,症状包括慢性盆腔痛、进行性痛经、不孕等。
负担:全球患者年均医疗成本近£10,000,亟需深入病理机制研究。
1.3 铁死亡与EM的关联
铁死亡的作用:EM异位内膜组织中脂质过氧化产物和铁死亡相关基因(FRGs)显著升高,铁死亡通过促进异位细胞异常存活增殖参与EM发病。
研究空白:PAEs暴露、铁死亡与EM三者的交互机制不明,尤其是PAEs是否通过调控铁死亡通路介导“PAEs-EM”轴。
本研究整合多组学分析、机器学习、分子模拟与临床验证,系统探究PAEs促EM的机制,具体方法如下:
2.1 数据与靶点收集
PAEs成分:从PubMed等数据库获取7种常见PAEs(DMP、DEP、DiBP、DBP、DEHP、DiNP、DOP)。
靶点来源:
PAEs相关靶点:ChEMBL、CTD、PharmMapper、Swiss Target Prediction(5325个);
EM相关靶点:GeneCards、TTD、DrugBank、OMIM(2440个);
FRGs:FerrDb数据库(471个)。
2.2 多组学数据处理
Bulk RNA-seq:GEO数据库获取GSE51981(训练集,71正常+77 EM样本)、GSE7305/GSE7846(验证集),limma包分析差异表达基因(DEGs),WGCNA识别EM相关共表达模块(turquoise模块,2215个基因)。
scRNA-seq:Tan等研究的6个EM样本,Seurat包过滤低质量细胞(线粒体基因<20%、nFeature RNA 200-6000),UMAP降维,注释7种细胞类型(上皮细胞Epi、间质细胞MSCs等)。
空间转录组:GSM6690476数据集,Seurat+SCTransform归一化,RCTD反卷积解析细胞类型空间分布。
2.3 生物信息学分析
功能富集:clusterProfiler包GO/KEGG分析(P<0.05),ggplot2可视化。
机器学习:12种算法(82个框架)筛选关键FRG,XGBoost+Lasso+RF组合最优(平均C-index最高),识别共同候选基因ARF6。
免疫细胞浸润:ssGSEA评估28种免疫细胞(TISIDB数据库),Wilcoxon检验比较组间差异。
2.4 机制验证实验
单细胞分析:CytoTRACE评估Epi干性,GSVA分析MSCs的EMT特征,Monocle2伪时间轨迹分析细胞转化。
ARF6功能模拟:scTenifoldKnk算法构建基因调控网络(GRN),虚拟敲除ARF6分析下游FRGs扰动。
分子对接:AutoDock Vina模拟PAEs与ARF6(PDB ID:2A5D)结合,PyMOL可视化互作。
临床样本验证:10例EM患者/非EM对照的子宫内膜组织,IHC(ARF6抗体)、IF(ARF6与EMT标志物共定位)检测表达。
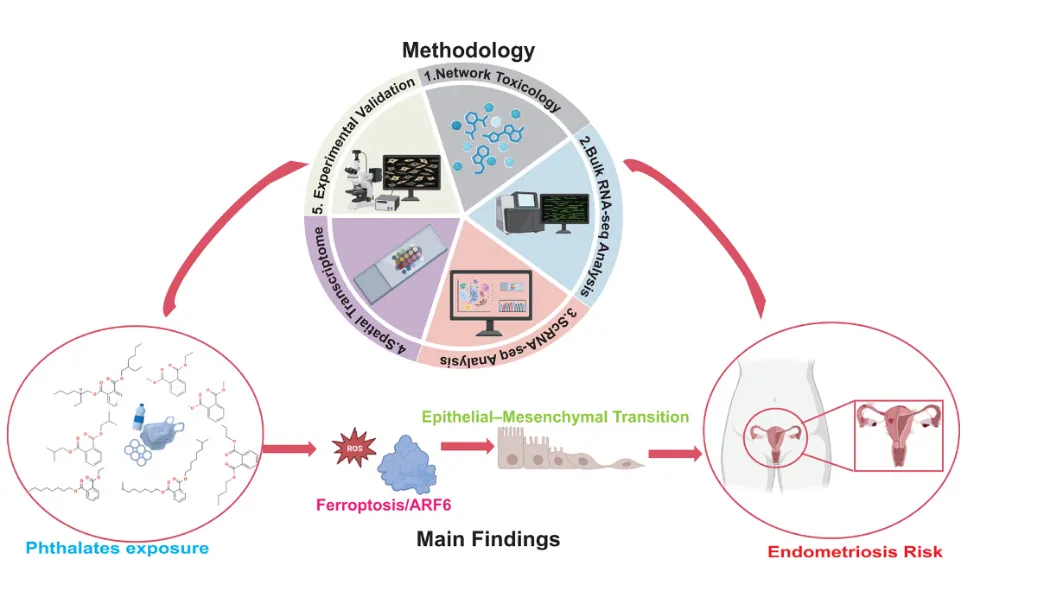
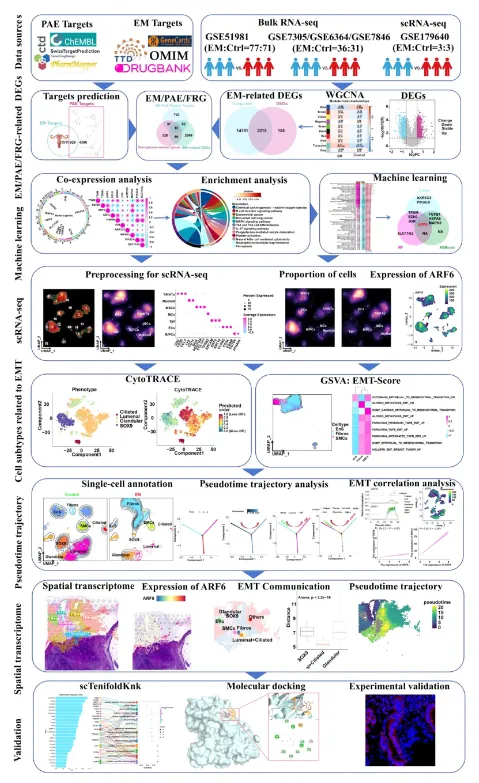
图1 本研究分析流程图
3.1 识别PAEs暴露下EM中差异表达的FRGs
流程与交集:PAE-EM预测靶点929个(Fig.2A),GSE51981的DEGs 2370个(Fig.2B-C),WGCNA识别turquoise模块(Fig.2D),交集得2215个EM相关DEGs(Fig.2E),与FRGs重叠得10个PAEs/EM-FRGs(TFAM、TGFB1、ARF6、EZH2等,Fig.2F-G)。
3.2 PAEs/EM-FRGs富集于氧化应激和EMT通路
功能富集:GO分析显示其参与“响应活性氧”“EMT正调控”等(Fig.2I);KEGG分析关联“铁死亡”“子宫内膜癌”等通路(Fig.2J)。
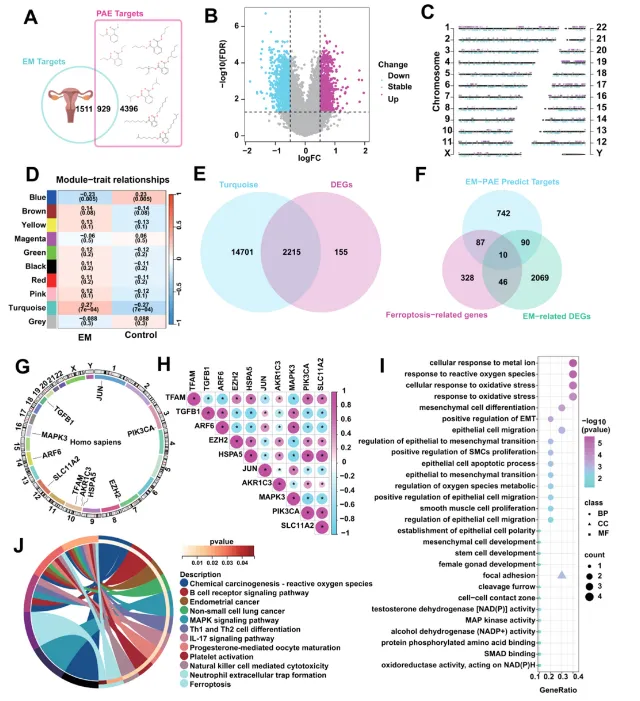
图2 PAES/EM-FRGs的鉴定
3.3 ARF6是PAEs暴露下的关键FRG
机器学习筛选:XGBoost+Lasso+RF组合从10个FRGs中识别ARF6(所有算法共同指向,Fig.3A-E)。
实验验证:IHC/IF显示EM组织中ARF6表达显著高于对照(Fig.3F-I)。
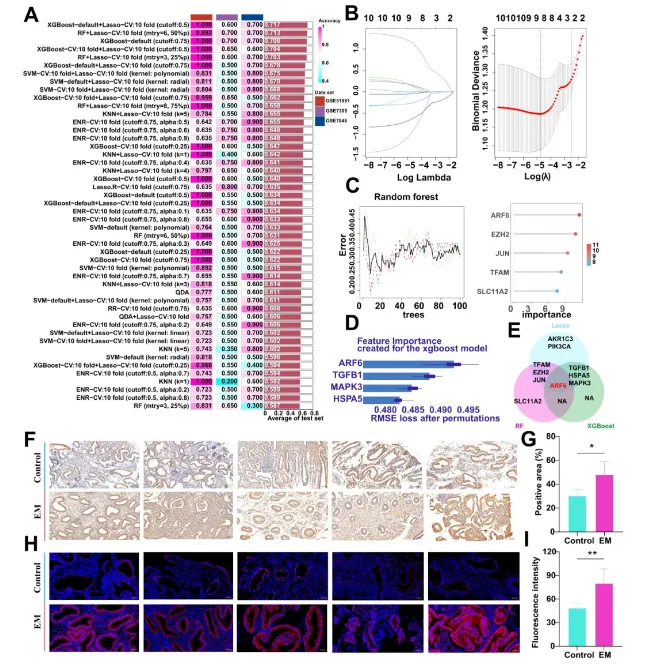
图3 使用多种机器学习算法识别暴露于PAEs的集线器FRG
3.4 ARF6影响EM免疫微环境
免疫细胞浸润:ssGSEA分析发现15种免疫细胞(T/B细胞、巨噬细胞等)在EM中浸润紊乱,ARF6表达与这些细胞丰度显著相关(Figure S2)。
3.5 ARF6与EM中EMT相关细胞共定位
单细胞表达:scRNA-seq聚类19个细胞簇(Fig.4A),注释Epi(对照组富集)、MSCs(EM组富集)(Fig.4D-E),ARF6在Epi和MSCs中均有表达(Fig.4F)。
共定位验证:IF显示对照组ARF6与EPCAM(Epi标记)低表达共定位,EM组与COL1A1(MSCs标记)高表达共定位(Fig.4G)。
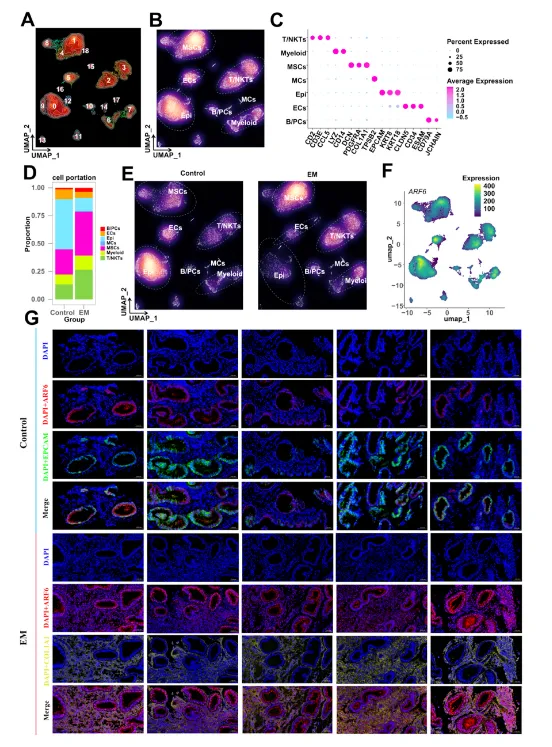
图4 单细胞转录组图谱
3.6 ARF6表达与Epi干性正相关
Epi亚型分析:Epi分SOX9、Lumenal、Glandular、Ciliated亚型(Fig.5A-B),Lumenal/Ciliated在对照组为主(Fig.5C-D),ARF6在Lumenal/Glandular高表达(Fig.5E-G)。
干性关联:CytoTRACE分析显示Lumenal/Ciliated干性最高(Fig.5H-I),ARF6表达与两者干性显著正相关(Fig.5J-K)。
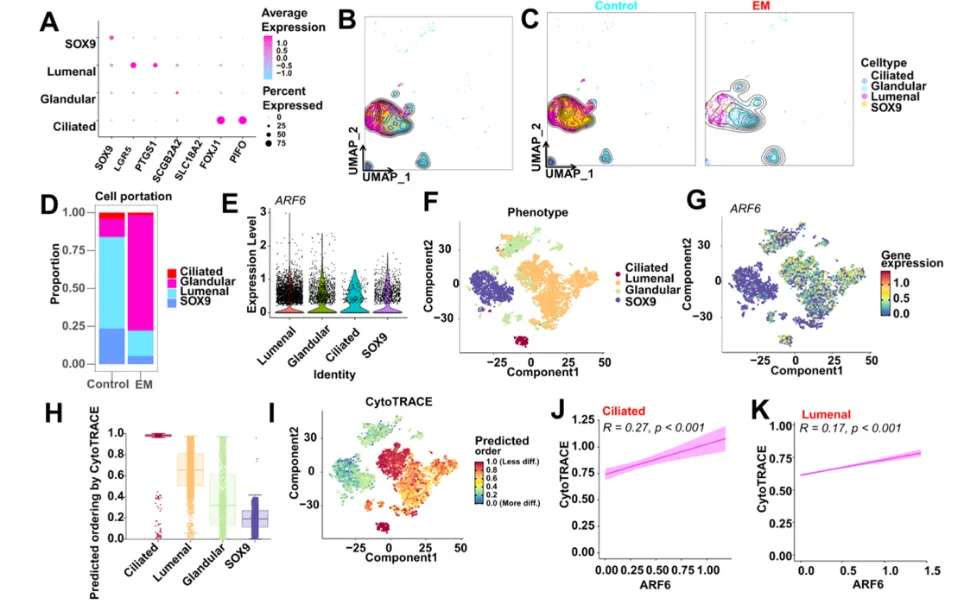
图5 EPI亚型的注释和细胞追踪分析
3.7 MSCs中Fibros亚型的EMT能力强
MSCs亚型:分EnS、Fibros、SMCs(Fig.6A-B),Fibros在EM组富集(Fig.6C-D),ARF6在Fibros高表达(Fig.6E-F)。
EMT能力:GSVA分析显示Fibros的EMT特征最显著(Fig.6G)。
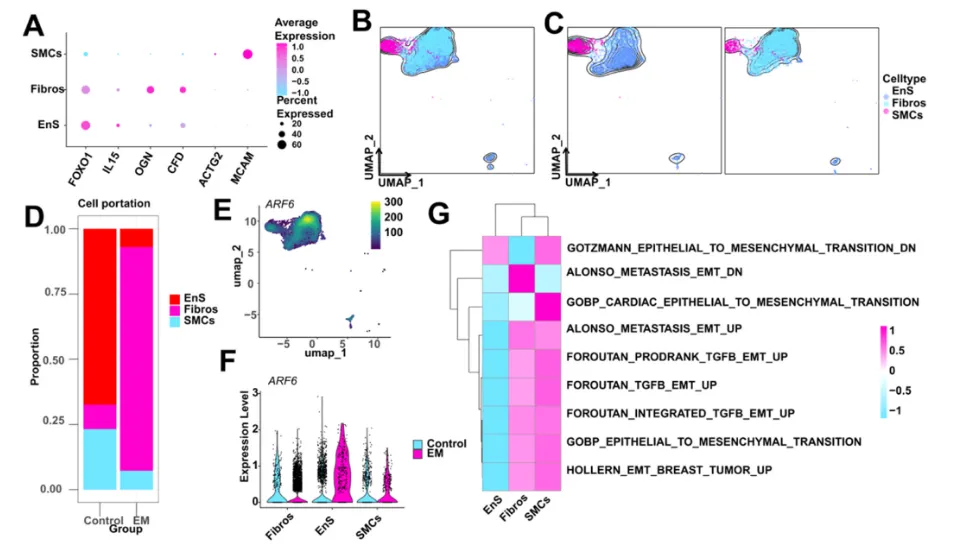
图6 MSC亚型的注释和GSVA分析
3.8 ARF6介导EMT促进Fibros分化
伪时间轨迹:对照组Lumenal/Ciliated向EM组Fibros转化(Fig.7A-G),ARF6表达与Fibros的EMT分化水平(CDH2/SNAI1)正相关(Fig.7H-K)。
蛋白共定位:IF显示ARF6与CDH2(间质标记)在EM中共定位(Fig.7L)。
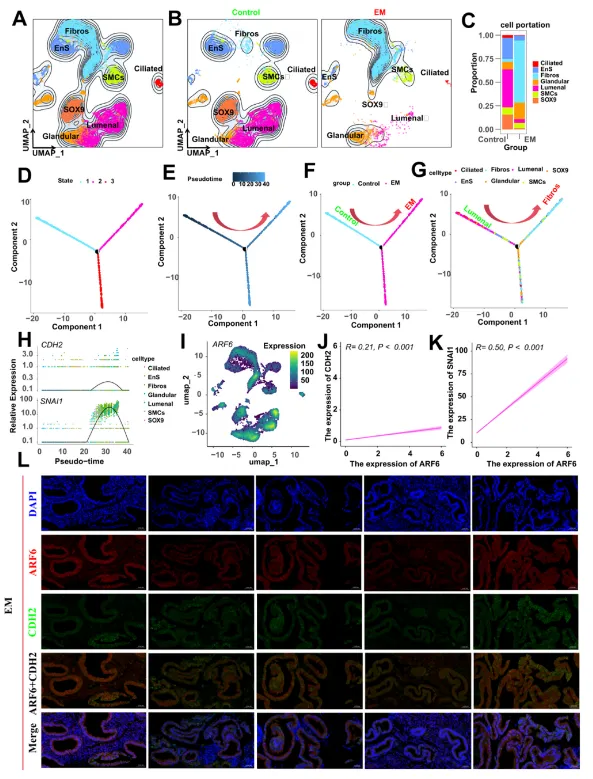
图7 EPI/MSC亚型的伪时间分析
3.9 空间转录组结合IF验证EM中EMT
空间特征:空间转录组显示EM组织异质性(Fig.8A-B),RCTD反卷积注释EMT细胞(Fig.8C-D),ARF6在EMT细胞中高表达(Fig.8E)。
分子机制:对照组ARF6与CDH1(上皮标记)共定位(Fig.8F),IL6信号在Lumenal+Ciliated与Fibros间显著(Fig.8J),空间距离两者最近(Fig.8K),伪时间分析支持转化(Fig.8L)。
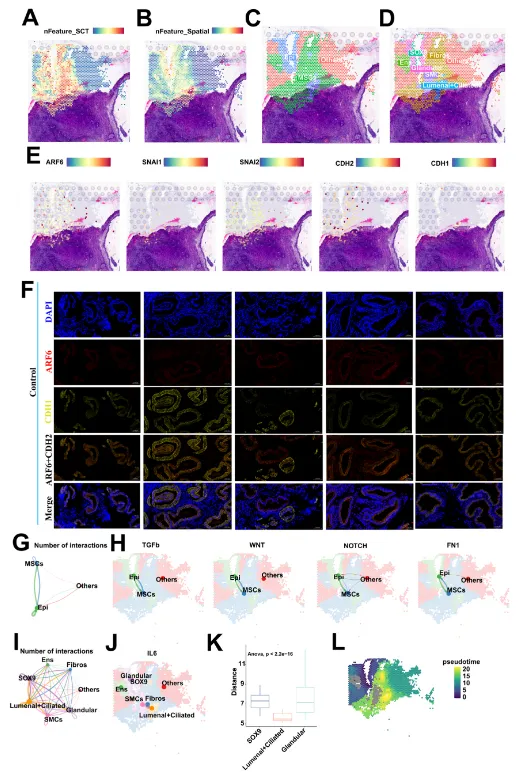
图8 空间转录组学和免疫荧光共定位揭示了ARF6介导的EM中上皮-间质转化的空间分子机制
3.10 ARF6虚拟敲除揭示铁死亡调控网络
扰动效应:scTenifoldKnk模拟ARF6敲除,23个FRGs扰动(Figure S5),富集于“氧化应激响应”“蛋白磷酸化调控”等(Fig.9A)。
3.11 PAEs与ARF6的分子对接
结合能力:PAEs与ARF6结合能<-5 kcal/mol(优秀亲和力),存在氢键和范德华力(Fig.9B-I)。
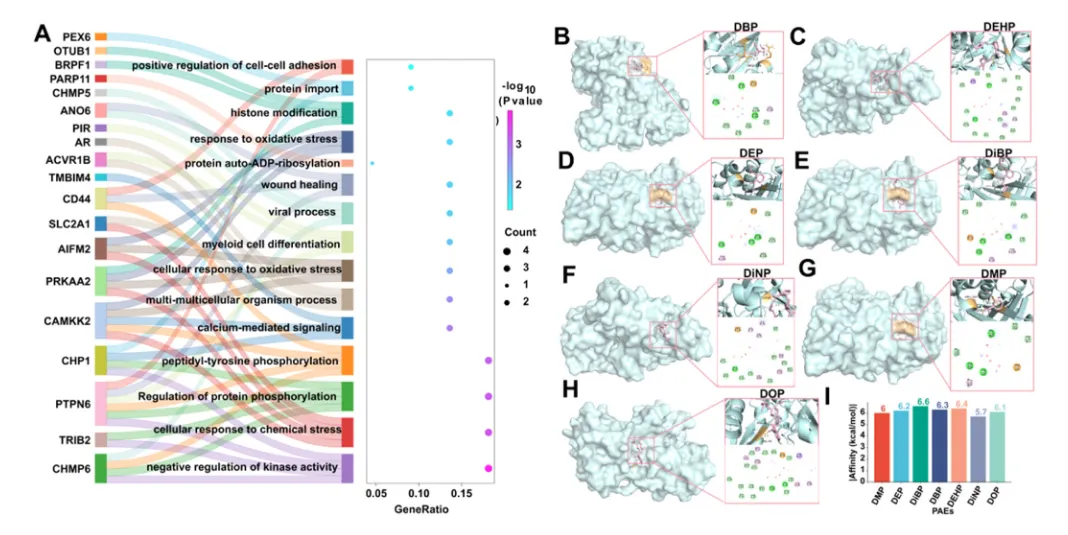
图9 利用模拟敲除和分子对接揭示ARF6促进EM的潜在机制
4.1 核心结论
关键分子:ARF6是PAEs暴露下促EM的关键FRG,通过调控铁死亡和EMT驱动EM进展。
EMT模型:构建“Lumenal+Ciliated(Epi)→Fibros(MSCs)”的特异性EMT转化模型,突破传统“混合细胞群体”研究的局限。
致病轴:提出“PAEs-铁死亡-EMT-EM”轴,阐明PAEs通过上调ARF6表达,增强Epi干性、促进EMT转化、扰动铁死亡通路,最终破坏免疫微环境促EM。
4.2 意义与展望
临床价值:ARF6可作为EM的新型治疗靶点(如靶向抑制ARF6表达)。
公共卫生:强调控制PAEs暴露(如减少塑料用品使用)对EM预防的重要性。
局限与未来:需扩展多组学维度(ATAC-seq、ChIP-seq)、开展体内外实验验证ARF6的具体调控机制。
后续协助方向:是否需要我帮你进一步解析该研究中某部分实验设计的细节(如scTenifoldKnk算法的虚拟敲除原理),或整理关键基因(如ARF6、FRGs)的功能列表?

扫描上方二维码关注我~
