在自然界中,活组织能够通过反复的力学载荷不断增强自身强度——肌肉越用越强壮,骨骼在应力刺激下愈加密实。然而,在合成材料中复现这种适应性生长能力,长期以来一直是材料科学领域的巨大挑战。传统合成材料往往在受力后产生不可逆的损伤或疲劳,而非获得性的强化。如何将力学信号转化为可控的化学键形成,从而实现材料的自主进化,是科学家们孜孜以求的目标。
近日,南京大学王炜教授、薛斌研究员、曹毅教授、李一然副教授合作,开发出一种基于蛋白质的力学响应水凝胶,能够在循环力学载荷下实现自主、可编程的机械性能增强。这项研究的核心创新在于利用了一种名为Csp1的铜储存蛋白作为力学门控催化模块。在拉伸变形时,Csp1蛋白发生去折叠并释放出储存的铜离子(Cu(I)),这些铜离子催化原位叠氮-炔环加成反应(CuAAC),在凝胶网络内形成新的共价交联。当外力卸载后,Csp1重新折叠并重新螯合铜离子,从而迅速终止催化反应。这一可逆的闭环力化学反馈机制,使得水凝胶能够在无需外部单体供给的情况下,实现应力和时间依赖的自我强化,并具备可编程的力学“记忆”功能。相关论文以“Mechanically Induced Adaptive Self-Growing Protein Hydrogel”为题,发表在Advanced Materials上。
图1 | 力诱导自适应自生长蛋白水凝胶的设计。 (a) 传统力响应自生长水凝胶的示意图。一旦聚合反应被引发,新聚合物网络就会持续形成,独立于力学输入(插图:应变输入)。由于初级网络的断裂和自由基的释放,杨氏模量和最大应力等力学性能最初会下降,随后随着新共价网络的形成而增加。(b) 自适应力响应自生长水凝胶的示意图及相应的输入应变信号(插图)。交联仅在力学加载期间发生,并在松弛时立即停止,从而实现应变依赖和可编程的网络发展。(c) 铜储存蛋白水凝胶中力诱导自适应自生长的机制。力学变形使Csp1去折叠并释放Cu(I)离子,这些离子催化网络中预载的叠氮/炔单体的共价交联。在松弛时,Csp1重新折叠并重新螯合Cu(I)离子,停止进一步生长并防止不可逆的离子损失。(d) 水凝胶内力触发蛋白去折叠和重新折叠的示意图,以及在力诱导自适应自生长过程中与Cu(I)催化的叠氮-炔环加成反应(CuAAC)的耦合。
为了验证这一设计的可行性,研究团队首先在单分子层面利用原子力显微镜力谱技术探究了Csp1的力学去折叠行为(图2a)。实验结果显示,Csp1蛋白在约120皮牛的拉力下发生去折叠,其轮廓长度增加约42纳米(图2b-d)。无论是否结合铜离子,Csp1的去折叠行为均未受到显著影响。更重要的是,研究团队通过超声模拟力学拉伸,诱导溶液中的Csp1蛋白去折叠并释放铜离子(图2e-g),利用BCA显色试剂可以清晰观察到紫色复合物的生成(图2h-i)。当超声停止后,蛋白重新折叠并重新吸收铜离子,在5分钟和10分钟内恢复效率分别达到66%和78%(图2j-k)。这一系列单分子和溶液实验,确凿地证明了Csp1能够作为力学响应的可逆离子开关。
图2 | 蛋白去折叠介导的Cu(I)释放和重新折叠介导的Cu(I)恢复的分子表征。 (a) 基于AFM的单分子力谱示意图。融合蛋白共价锚定在玻璃基底上,并用功能化的AFM探针拾取。(b) 融合蛋白的代表性单分子力-拉伸曲线。每个去折叠事件均使用蠕虫链模型进行拟合。轮廓长度增量约为42 nm的峰对应Csp1去折叠(红色箭头),随后是五个GB1去折叠峰(蓝色箭头),最后一个峰代表Fgβ/SdrG复合物的断裂(黑色箭头)。(c) Csp1去折叠力的直方图(平均值:120 ± 43 pN)。(d) Csp1轮廓长度增量的直方图(ΔLc = 42 ± 2.4 nm)。(e) 超声触发SC-Csp1-SC的力诱导去折叠并通过疏水染料ANS检测的示意图。(f, g) 超声或加热处理后ANS染色的SC-Csp1-SC溶液(1.25 mM)的荧光图像(f)和荧光光谱(g)。未处理的蛋白作为对照。(h) SC-Csp1-SC去折叠时Cu(I)释放的示意图(上)和图像(下),通过与BCA络合形成紫色复合物进行可视化。(i) 对应(h)的紫外-可见吸收光谱。插图:Cu(I)释放的定量(以储存在Csp1中的总Cu(I)为100%归一化)。(j) SC-Csp1-SC重新折叠后Cu(I)离子恢复的示意图(上)和图像(下)。超声处理后,将SC-Csp1-SC溶液静置恢复0、5和10分钟,紫色逐渐褪去表明Csp1重新摄取Cu(I)。(k) 超声后不同静置时间下Cu(I)恢复效率的定量,以从Csp1释放的总Cu(I)为100%。图(i)和(k)插图数据为平均值±标准差,n = 3。
在建立分子层面的机制后,研究团队将Csp1作为共价交联剂整合到聚丙烯酰胺水凝胶网络中,构建了单网络水凝胶(PAAm/Csp1)(图3a)。在循环拉伸-松弛过程中,水凝胶的应力-时间曲线表现出明显的应力衰减,暗示着蛋白质在持续载荷下的去折叠过程(图3c)。通过BCA显色原位监测,发现紫色络合物在拉伸时出现,在松弛时消失,直接证明了水凝胶内部的铜离子释放与再捕获过程(图3b)。系统分析表明,铜离子的释放量随应变幅度、Csp1浓度和拉伸时间的增加而提高(图3f-h),而恢复效率则随着应变增大而降低,但延长松弛时间可显著改善恢复能力(图3i-k)。值得注意的是,在生理条件下孵育18天后,水凝胶的铜离子释放与再结合性能以及力学表现均几乎保持不变,显示出优异的长期功能稳定性。
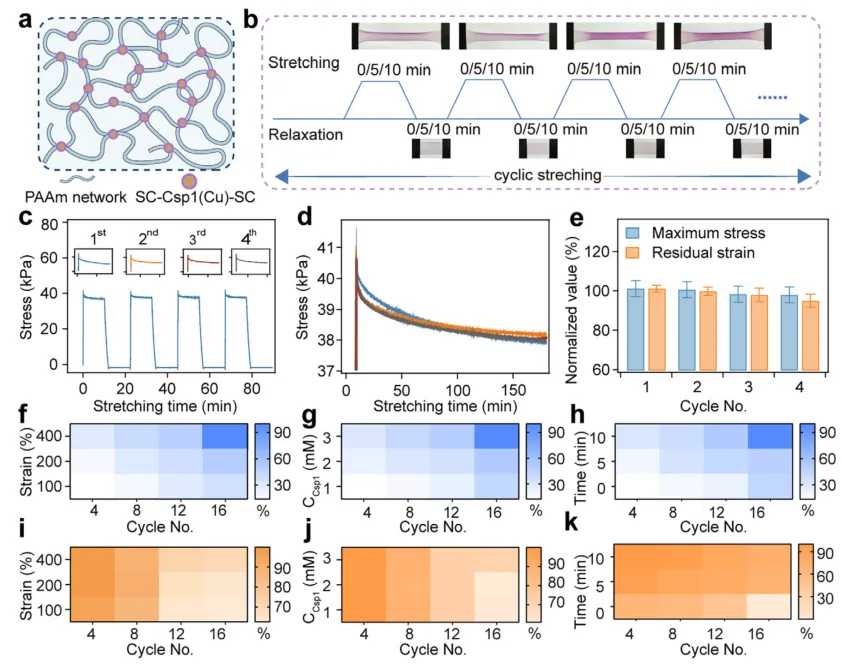
图3 | Csp1交联水凝胶中力诱导的Cu(I)离子释放与恢复。 (a) 单网络铜储存蛋白水凝胶(PAAm/Csp1水凝胶)的示意图。Csp1通过SpyCatcher-SpyTag连接然后共聚作为共价交联剂。(b) 力学拉伸诱导的Cu(I)离子释放与恢复循环的示意图和图像,通过BCA显色测定可视化。松弛使蛋白重新折叠并恢复Cu(I)。(c) 四个拉伸-松弛循环过程中的代表性应力-时间曲线。插图显示了放大的松弛阶段。(d) PAAm/Csp1水凝胶从第一个到第四个拉伸-松弛循环的重叠应力-应变曲线。(e) 从第一个到第四个循环的归一化最大应力和残余应变的总结。数据为平均值±标准差,n = 3。(f) 在不同拉伸应变(100%、200%、400%)下,不同循环次数时Cu(I)释放的热图。拉伸时间=10 min;Csp1浓度=3 mM。(g) 在不同Csp1浓度(1、2、3 mM)下,不同循环次数时Cu(I)释放的热图。拉伸时间=10 min;应变=400%。(h) 在不同拉伸持续时间(0、5、10 min)下,不同循环次数时Cu(I)释放的热图。应变=400%;Csp1浓度=3 mM。(i) 在不同拉伸应变(100%、200%、400%)下,不同循环次数时Cu(I)恢复的热图。拉伸时间=10 min;松弛时间=0 min;Csp1浓度=3 mM。(j) 在不同Csp1浓度(1、2、3 mM)下,不同循环次数时Cu(I)恢复的热图。拉伸时间=10 min;松弛时间=0 min;应变=400%。(k) 在不同松弛持续时间(0、5、10 min)下Cu(I)恢复效率的热图。应变=400%;拉伸时间=10 min;Csp1浓度=3 mM。
为了实现力学自适应生长,研究团队进一步在水凝胶网络中预载了叠氮和炔基官能团(PAAm/Csp1/AA)(图4a)。在循环拉伸-松弛训练下,水凝胶的杨氏模量和最大应力在16个循环内分别提高了超过400%和250%(图4b)。相比之下,不含铜离子的apo-Csp1对照水凝胶在相同条件下不仅没有增强,反而出现了轻微的力学性能下降(图4b)。这种渐进式的强化源于CuAAC反应在原位不断生成新的共价交联,而强化最终趋于饱和则归因于反应官能团的逐渐消耗。研究团队系统考察了不同Csp1浓度、拉伸应变、拉伸持续时间和松弛时间对自生长行为的影响(图4c-f),发现更高的拉伸应变和更长的拉伸时间会加速自生长,而更长的松弛时间则会减弱这一过程。更重要的是,研究团队通过逐步增重实验展示了水凝胶的阶梯式自生长能力:初始无法提起50克砝码的环形水凝胶,经过8个拉伸循环后便能成功提起;随着训练次数增加,它甚至能依次提起70克和100克的砝码,实现了力学性能的“按需”进化(图4g-h)。
除了宏观的力学强化,研究团队还实现了空间可控的力学生长图案化。他们采用“NJU”字形的模具对水凝胶进行局部压缩,在压缩区域内,力诱导的铜离子释放催化了CuAAC反应,形成了额外的交联(图4i)。随后用荧光探针3AH染色,只在压缩区域观察到了明亮的荧光信号,而未压缩区域则保持暗淡(图4j)。原子力显微镜纳米压痕测试进一步证实,压缩区域的杨氏模量显著高于非压缩区域(图4k)。这一“力刻蚀”技术为水凝胶的表面功能化和图案化提供了全新的力学调控手段。
图4 | 水凝胶的力触发时空自生长。 (a) 负载叠氮和炔基的Csp1交联水凝胶网络(PAAm/Csp1/AA水凝胶)的示意图。(b) PAAm/Csp1/AA(蓝色)和PAAm/apo-Csp1/AA(黄色)水凝胶在重复拉伸-松弛循环期间的应变-时间和力-时间曲线。顶部轨迹显示了循环期间施加的输入应变信号。(c) 含有不同叠氮/炔基浓度(3、6和9 mM)的PAAm/Csp1/AA水凝胶在16次拉伸-松弛循环之前(虚线)和之后(实线)的应力-应变曲线。拉伸和松弛时间分别固定为10 min和0 min;应变=400%。(d) PAAm/Csp1/AA水凝胶在16次拉伸-松弛循环之前(对照)和之后(使用不同拉伸持续时间(0、5和10 min)进行循环)的应力-应变曲线。C叠氮 = C炔基 = 9 mM;使用不同的松弛时间(0、5和10 min)。C叠氮 = C炔基 = 9 mM;拉伸时间=0 min;应变=400%。(f) PAAm/Csp1/AA水凝胶在16次拉伸-松弛循环之前(对照)和之后(使用不同应变(100%、200%和400%)进行循环)的应力-应变曲线。C叠氮 = C炔基 = 9 mM;拉伸时间=0 min;松弛时间=0 min。(g) 通过循环拉伸后依次提起质量递增(50、70和100 g)的砝码来可视化逐步力诱导的自生长。(h) 对应于(g)中逐步提重行为的力-时间曲线。(i) 力刻蚀的示意图。模具对水凝胶的局部压缩在压缩区域选择性地引发CuAAC反应。(j) 使用3-叠氮-7-羟基香豆素(3AH)可视化未反应的叠氮基团后,图案化PAAm/Csp1/AA水凝胶的明场(上)和荧光(下)图像。比例尺:(左、右)2 mm和120 μm。(k) 从(j)所示压缩和未压缩区域的AFM纳米压痕获得的杨氏模量直方图。
为了深入理解自生长的化学机制,研究团队对力诱导的铜催化点击化学反应进行了系统验证。收集经过不同循环次数后的水凝胶浸出液,并与荧光探针3AH反应,发现荧光强度随循环次数增加而显著上升,证明释放的铜离子具备催化活性(图5a-c)。对水凝胶本体直接染色则显示,经过16个循环后,水凝胶的荧光信号几乎消失,意味着高达96.47%的炔基已被消耗(图5d-f)。傅里叶变换红外光谱证实了叠氮和炔基特征峰的逐渐消失以及三唑环新峰的出现(图5g),扫描电镜图像则显示水凝胶的孔径从约5.20微米逐渐减小至约0.83微米(图5h)。此外,双折射成像揭示了在循环拉伸过程中,PAAm/Csp1/AA水凝胶内部形成了持续性的分子链取向和各向异性结构,而对照水凝胶则几乎没有变化,这为力学强化提供了直接的结构证据(图5i-j)。
图5 | 力触发Cu(I)催化的叠氮-炔环加成反应(CuAAC)和二次交联形成的机理验证。 (a) 从去折叠的Csp1释放Cu(I)引发CuAAC的示意图。(b, c) 从单网络PAAm/Csp1水凝胶在拉伸-松弛循环后收集的浸出液的光学图像(b)和荧光光谱(c),使用CuAAC开启探针3AH检测。比例尺:3 mm。(d-f) 使用3AH在不同拉伸-松弛循环后测定PAAm/Csp1/AA水凝胶中CuAAC反应的示意图(d)、图像(e)和效率(f)。比例尺:10 mm。图f中的数据为平均值±标准差,n = 3。(g) PAAm/Csp1/AA水凝胶在0、8和16次拉伸-松弛循环后的FT-IR光谱。(h) PAAm/Csp1/AA水凝胶在增加拉伸-松弛循环次数后的SEM图像(上)和相应的孔径分布(下)。比例尺:7 μm。(i) PAAm/apo-Csp1/AA(左)和PAAm/Csp1/AA(右)水凝胶在300%应变下的双折射图像。比例尺:20 mm。(j) 随着拉伸-松弛循环次数的增加,(i)中水凝胶的定量双折射强度演变。
这项研究不仅成功模拟了生物组织的适应性生长行为,更开辟了一条连接生物力传导与合成力化学的全新路径。通过将可逆的蛋白质力学响应与催化网络演化相耦合,研究团队在无需结构损伤或外部单体供给的条件下,实现了可重复、可控制的材料强化。Csp1蛋白约120皮牛的去折叠力阈值远低于传统合成力敏团所需的500皮牛以上,使其能够在普通单网络水凝胶中直接激活。这一通用性设计原则可望拓展至其他金属蛋白体系,为设计能够在力学刺激下自主优化结构和功能的下一代自适应生物材料、软体机器人和植入式系统提供了崭新的平台。