【ACS Catal.】南京大学潘惠杰课题组:一种基于链霉亲和素的模块化铜(II)人工金属酶用于不对称路易斯酸催化
- 2026-06-06 06:38:40

背景介绍:在可持续化学合成和生物经济发展的推动下,酶催化技术受到广泛关注。然而,天然酶的应用常受限于其狭窄的底物范围和有限的反应类型。人工金属酶(ArMs)通过将合成金属配合物嵌入蛋白质支架,有望结合过渡金属的反应活性和生物催化剂的立体选择性,从而突破天然酶的局限。在多种ArMs构建策略中,生物素-链霉亲和素(Biotin-Streptavidin, Sav)体系因其超强的结合亲和力(Kd≈ 10-14 M)成为构建活性位点的理想锚点,已被成功应用于多种反应。然而,目前主流的Sav-ArMs通常依赖于铱、铑、钌等贵金属和复杂配体,其多步合成路线限制了可持续性和可扩展性。相比之下,丰产、低成本的碱金属(如铜、铁、镍)更具优势。同时,碱金属是高效路易斯酸催化剂的核心,但天然酶体系中类似的催化功能有限,这为设计基于碱金属的新型路易斯酸人工金属酶带来了机遇。
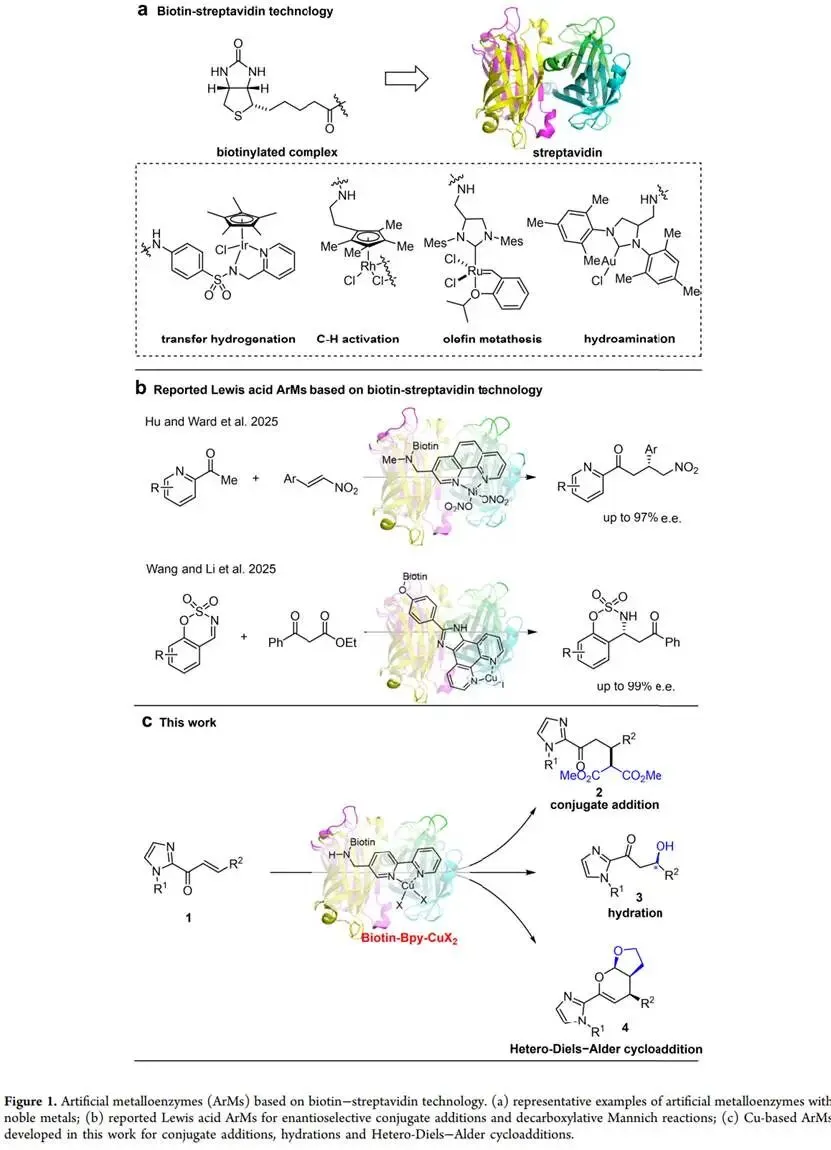
研究思路:为了开发更具可持续性和普适性的碱金属人工金属酶平台,本研究聚焦于廉价、易得的铜(II)离子。研究者设计并合成了一个结构简单、仅需两步即可制备的Biotin-Bipyridine-Cu(II)金属辅因子,并将其模块化地嵌入链霉亲和素(Sav)蛋白支架中。该设计的核心思路是利用Sav蛋白提供一个可编程、可优化的手性空腔,来调控铜(II)中心周围微环境的立体化学性质,从而实现对三种不同类型路易斯酸催化反应(共轭加成、烯烃水合、杂狄尔斯-阿尔德环加成)的立体选择性控制,并评估其通用性。
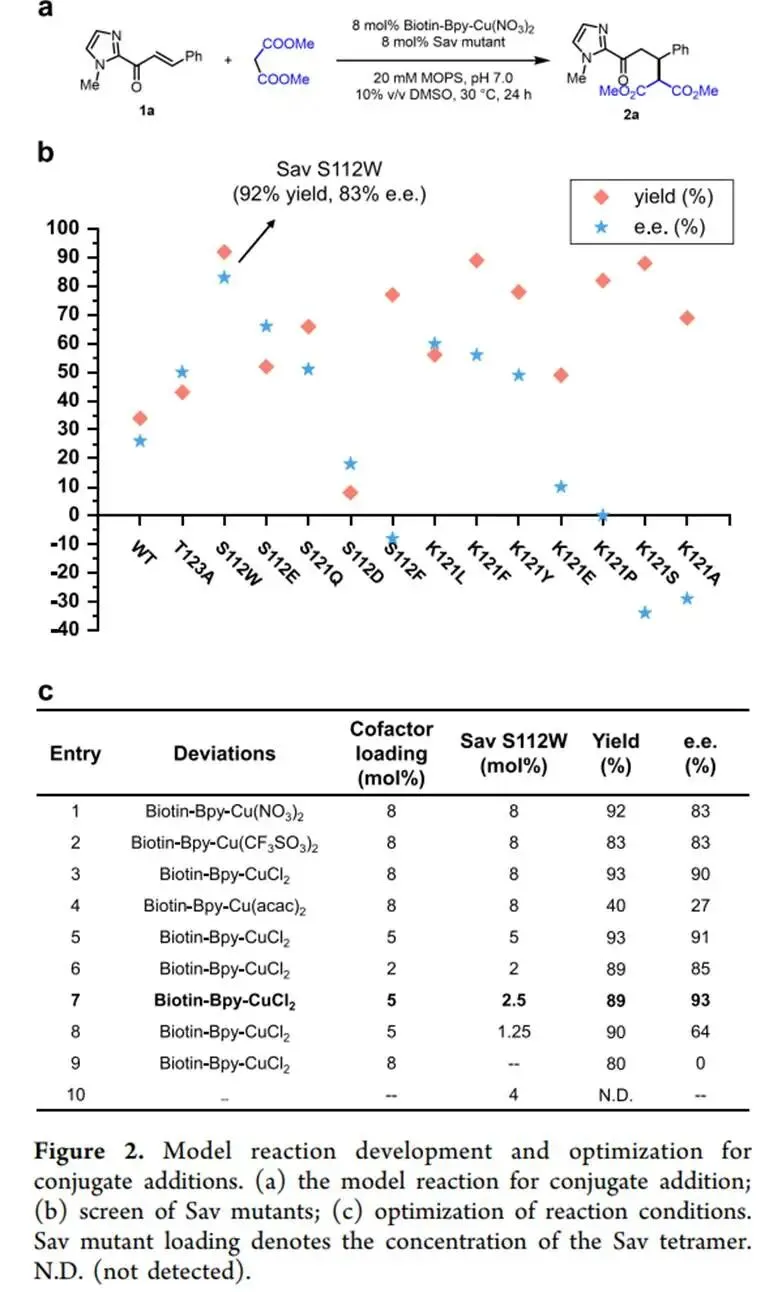
研究内容:研究首先成功组装了该人工金属酶体系,并以一个通用模型底物对上述三类反应进行了系统性优化。对于迈克尔共轭加成反应,通过对Sav蛋白关键氨基酸残基(S112和K121)进行定点突变,筛选出最优突变体S112W,将反应的对映选择性(e.e.值)从26%大幅提升至90%。研究还发现,反应性能高度依赖于金属盐和辅因子占据数,例如,使用CuCl2盐、且只有单个辅因子占据Sav蛋白二聚体结合口袋时,获得了最优的选择性。对于烯烃水合反应,突变体K121L表现出最佳效果。有趣的是,该反应与共轭加成不同,需要两个辅因子占据空腔才能获得最佳立体控制。对于杂狄尔斯-阿尔德环加成反应,通过条件优化,使用K121L突变体与Biotin-Bpy-Cu(NO3)2辅因子组合,实现了高达90%的对映选择性。
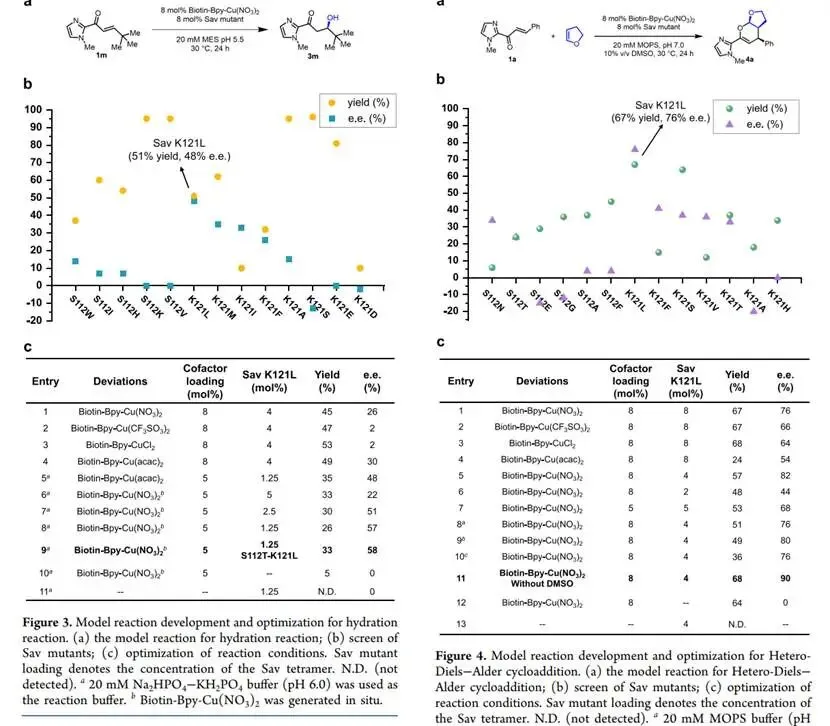
优化后,该Cu(II)-ArM平台对三类反应的多种底物均表现出良好的普适性,共轭加成可获得高达94%的e.e.值,杂狄尔斯-阿尔德环加成最高可达96%的e.e.值,而烯烃水合反应的选择性因底物空间位阻不同在31%至60%之间。
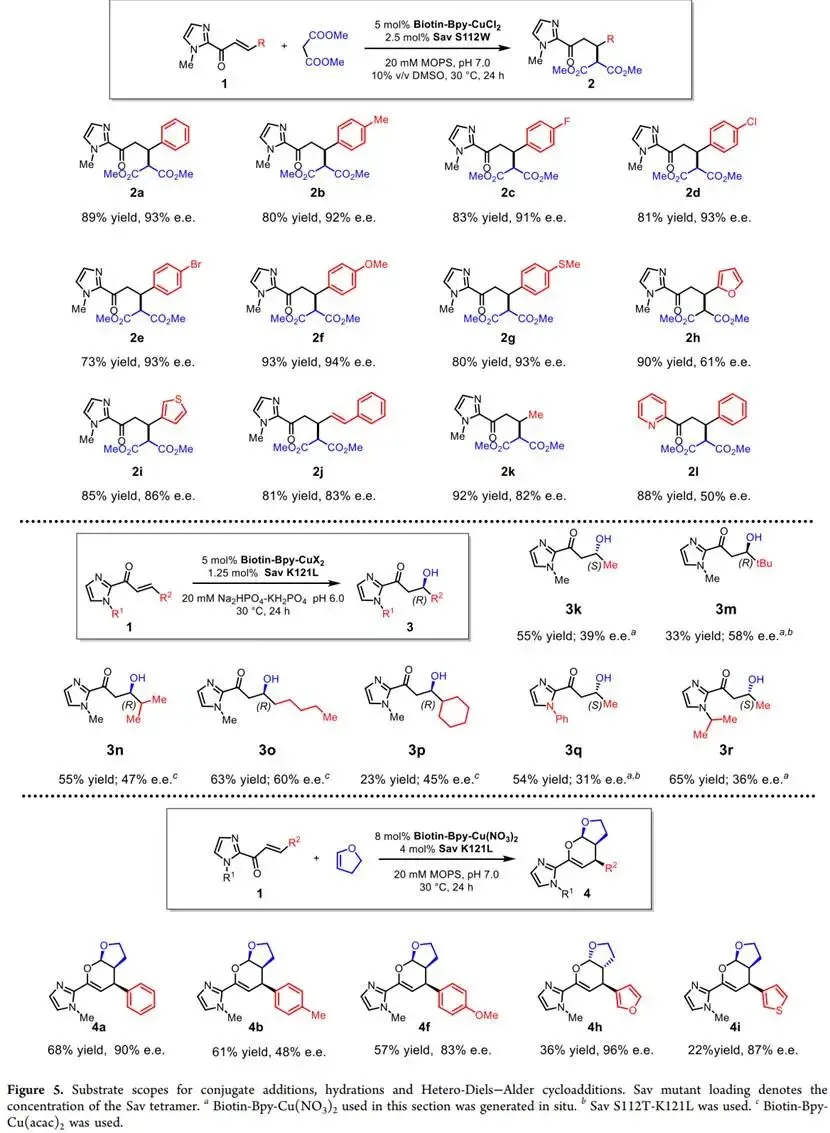
总结:本研究成功构建了一个基于链霉亲和素和合成Biotin-Bipyridine-Cu(II)辅因子的、可持续且通用的模块化人工金属酶系统。该系统能够在单一平台上催化三种截然不同的非天然路易斯酸反应,并通过对活性位点的工程化改造,实现了高达96%的对映选择性。该工作证明了利用廉价铜离子结合简单配体构建高性能人工金属酶的可行性,强调了活性位点微环境的精细调控对催化性能的关键影响,为开发新一代基于碱金属的、可适应多种反应类型的可持续催化平台开辟了道路。
文献详情:
- 作者:Qingqing Chen, Jinmeng Yu, Chang Wang, Jing Zhao, Hui-Jie Pan
- 题目:A Modular Cu(II)-Based Artificial Metalloenzyme for Enantioselective Lewis Acid Catalysis
- 期刊:ACS Catalysis
- DOI:10.1021/acscatal.5c07673
(所有图片来自网络,如有侵权联系删除)
看往期精彩文章 ↓
【Nat. Chem.】天津大学福州国际联合学院赵宇/杨彬淼团队联合蓝宇实现中环合成新突破
如果我们的文章对你有帮助, 点击左下角“+关注 ”!这样就不会错过每次的推送啦!
右下点赞、点分享、点推荐,就是最好的支持
