康复大学陈刚、南京中医药大学曹鹏、扬州大学郇长超Biomaterials!!工程化噬菌体纳米组装体:通过稳定免疫突触提升流感疫苗效能
- 2026-04-11 04:02:50
医学研究前沿——聚焦医学前沿研究进展。100多万医学领域硕博医生们订阅的微信公众号。点击标题下蓝字“医学研究前沿”关注,我们将为您提供最有价值、最前沿的医学前沿资讯。

树突状细胞(DCs)作为关键的抗原呈递细胞,在激活T细胞免疫应答中扮演核心角色,其与T细胞之间形成的免疫突触(IS)稳定性直接决定疫苗效果。然而,现有疫苗策略往往侧重于抗原递送或DC成熟调控,而对体内DC-T细胞相互作用的有序增强研究不足。核酸疫苗虽展现出潜力,但递送效率、靶向性和安全性问题制约其发展。康复大学陈刚团队联合多家机构在《Biomaterials》发表研究,提出一种创新性疫苗设计:通过工程化噬菌体纳米组装体靶向增强DC-T细胞免疫突触稳定性,从而提升流感疫苗的免疫保护效果。该策略突破传统思路,将重点从单一抗原递送转向细胞间相互作用调控,为疫苗开发提供新方向。
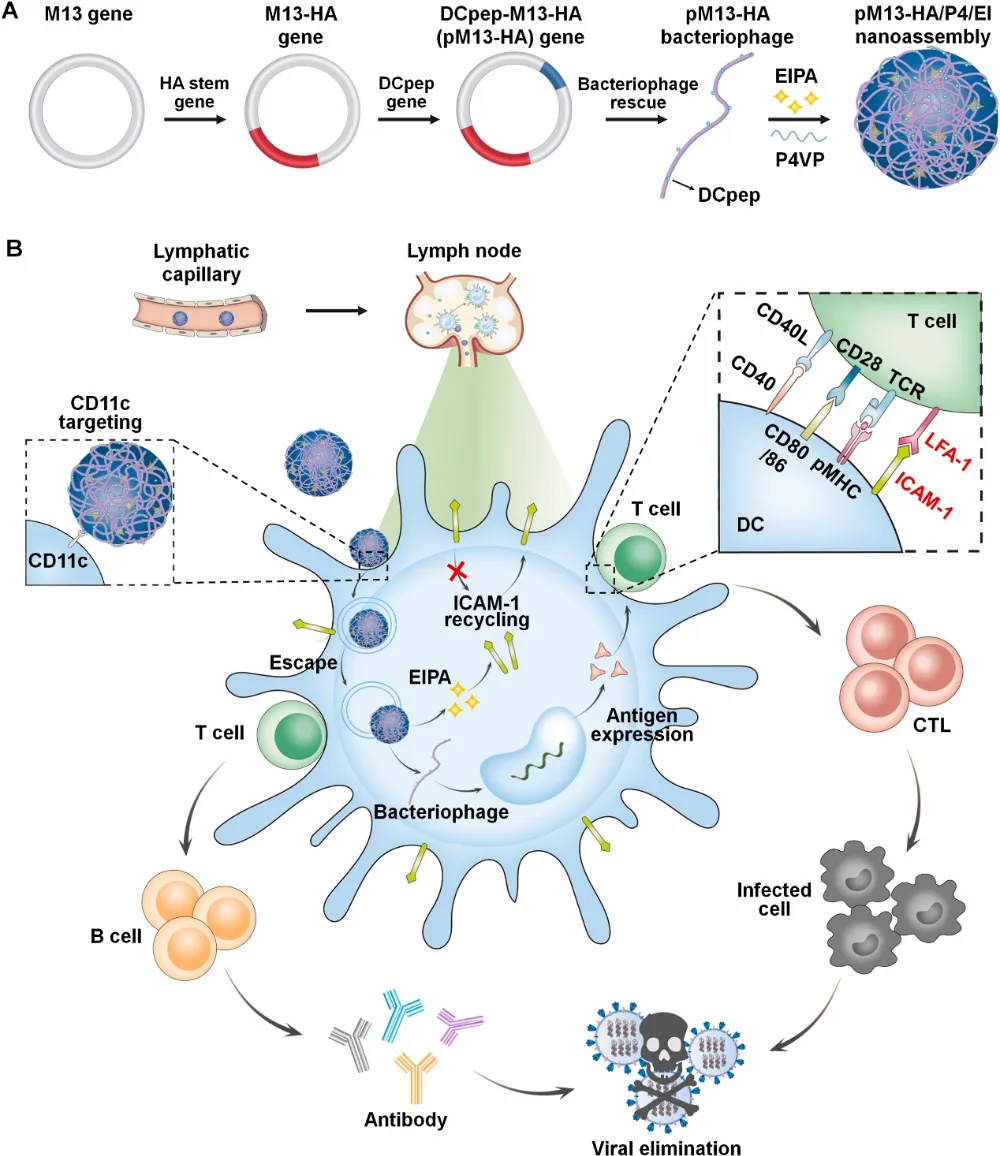
研究团队以M13噬菌体为基础构建纳米组装体,首先通过基因工程将流感病毒血凝素(HA)干基因插入噬菌体基因组,并在病毒侧壁融合DC靶向肽,实现抗原编码序列的特异性递送。随后,噬菌体作为表面活性剂包裹疏水性聚(4-乙烯基吡啶)颗粒,颗粒内部包载钠/质子泵抑制剂,用于调控细胞间黏附分子1(ICAM-1)的膜定位。尺寸可控的纳米组装体通过激活NF-κB、PI3K-AKT和RhoA-ROCK信号通路,有效抑制ICAM-1的内化过程,从而增强DC与T细胞界面黏附,稳定免疫突触结构。实验表明,该设计能促进抗原呈递效率,并显著提高T细胞活化水平。与常规递送系统相比,噬菌体平台兼具佐剂效应和安全性优势,且生产成本低、易于规模化。
在流感病毒感染小鼠模型中,纳米组装体免疫可触发强烈的T细胞和抗体应答,提供完全保护并诱导长期免疫记忆。研究证实,通过体内靶向稳定免疫突触,能有效提升疫苗效能,且该噬菌体纳米组装体平台具有灵活性和通用性,可适配不同病原体抗原进行改造。这一策略不仅为流感疫苗开发提供新途径,也为针对其他传染病的疫苗设计奠定基础,未来有望推动高效、安全疫苗制剂的临床应用



说明:
🔹本文仅作科研人员学术交流。
🔹本文内容若存在版权问题,请联系我们及时处理。
🔹欢迎广大读者对本文进行转发宣传。
🔹《医学研究前沿》会不断提升自身水平,为读者分享更加优质的材料研究成果解读,欢迎关注我们。
欢迎广大科研工作者投稿最新研究成果。
