中药复方如何护心?天津中医药大学& 南京中医药大学:藿丹清化方通过 TGR5-DHHC4 通路抑制 CD36 膜定位,以改善糖尿病心肌病的脂毒性损伤
- 2026-05-06 02:19:56

各位热爱科研的小伙伴们,今天为大家推介2026年4月发表在 《Phytomedicine》杂志的研究性文章。该文章由天津中医药大学 张军平教授 南京中医药大学 胡玥教授等团队共同完成,主要研究方向为中医药防治心脑血管病、中西医结合防治神经系统疾病及医学大数据应用研究等。文章题目“Huodan Qinghua formula inhibits CD36 membrane localisation via the TGR5-DHHC4 pathway to ameliorate lipotoxic damage in diabetic cardiomyopathy”。本研究旨在探讨HDQH是否通过减少脂肪酸摄取(Fatty Acid Uptake, FAU)来缓解心脏脂毒性,从而阐明其治疗DCM的潜在机制,并且围绕藿丹清化方(Huodan Qinghua formula)、糖尿病心肌病(Diabetic cardiomyopathy)、TGR5-DHHC4通路(TGR5-DHHC4 pathway)、CD36、脂肪酸摄取(Fatty acid uptake)、脂毒性(Lipotoxicity)等关键词展开研究。

背景:糖尿病心肌病(DCM)是糖尿病相关的心脏并发症,发病率持续上升,其发病机制复杂且易反复,临床治疗面临挑战。藿丹清化方(HDQH)是一种中药复方,在临床用于治疗糖尿病心血管疾病已逾十年,能改善心功能和预后,但其具体作用机制尚不完全清楚。
糖尿病心肌病本质上是一种“心肌底物代谢失稳态”疾病 。在胰岛素抵抗背景下,心肌对脂肪酸的过度摄取(Over-uptake)远超其线粒体氧化能力,导致有害脂质堆积,引发从“能量过剩”到“结构塌陷”的病理级联反应 。
健康心肌可在葡萄糖和脂肪酸间切换;DCM 早期即出现代谢倾向偏移,心肌能耗的 90% 以上被迫依赖脂肪酸氧化。心肌细胞膜上的转运蛋白(如 CD36)在高血糖/高脂环境下发生异常转位,持续开启脂肪酸进入细胞的通道 。未被氧化的脂肪酸转化为神经酰胺(Ceramide)和二酰基甘油(DAG)等毒性脂质 。
TGR5-DHHC4-CD36轴是心肌代谢从“脂毒性过载”向“代谢稳态”回归的关键闸门。通过激活 TGR5 诱导的信号级联,调控棕榈酰转移酶 DHHC4,从空间定位上阻断 CD36 向细胞膜的迁移,从而从源头上切断了诱发心肌损伤的有害脂肪酸流。
目的:探讨HDQH是否通过减少脂肪酸摄取(FAU)来减轻心脏脂毒性,从而阐明其治疗DCM的潜在机制。
方法:
1. 成分鉴定:采用超高效液相色谱-串联质谱(UPLC-MS/MS)技术鉴定HDQH及其体内生物活性成分。
2. 靶点预测:利用网络药理学和分子对接技术预测HDQH治疗DCM的关键靶点和信号通路。
3. 体内实验:通过高脂饮食联合链脲佐菌素(STZ)诱导建立C57BL/6J小鼠糖尿病模型,灌胃给予HDQH 12周。通过超声心动图、Masson三色染色和HE染色评估心脏功能和形态;通过油红O染色和荧光标记脂肪酸检测心肌脂质沉积和FAU;通过ELISA和生化检测测定总胆汁酸、胰岛素、NT-proBNP和血脂水平;检测游离脂肪酸(FFAs)和活性氧(ROS)水平;通过Western blot和实时定量PCR(RT-qPCR)探索潜在分子机制。
4. 体外实验:采用棕榈酸(PA)诱导H9C2心肌细胞损伤模型,通过药理学激活和抑制靶蛋白表达进一步验证HDQH的作用机制。
结果:
1. 成分分析:在血浆中鉴定出16种化合物及代谢物,主要成分包括巴马汀(palmatine)、补骨脂色烯醇(bavachromanol)、马钱苷元(loganetin)、氧化小檗碱(oxyberberine)和新隐丹参酮(neocryptotanshinone)。
2. 靶点预测:网络药理学和分子对接分析提示HDQH可能通过调节TGR5受体相关信号通路发挥治疗DCM的潜在作用。
3. 体内药效:HDQH显著改善DCM小鼠心脏功能,有效减轻心肌肥厚、纤维化和脂质沉积;同时升高总胆汁酸水平,降低FFA和ROS水平。
4. 分子机制:Western blot和RT-qPCR分析表明,HDQH抑制心脏脂毒性与调节心肌细胞膜上TGR5、DHHC4和CD36的表达密切相关。
5. 体外验证:HDQH激活TGR5表达,导致下游靶点DHHC4受到抑制,进而通过抑制CD36膜定位减少过度的FAU。值得注意的是,TGR5抑制剂SBI-115可减弱HDQH的有益作用。
结论:HDQH通过调控TGR5-DHHC4通路,抑制CD36膜定位,从而减少心脏脂肪酸摄取和脂质积聚,发挥对DCM的心肌保护作用。该研究为HDQH治疗糖尿病心肌病提供了有力的机制证据。
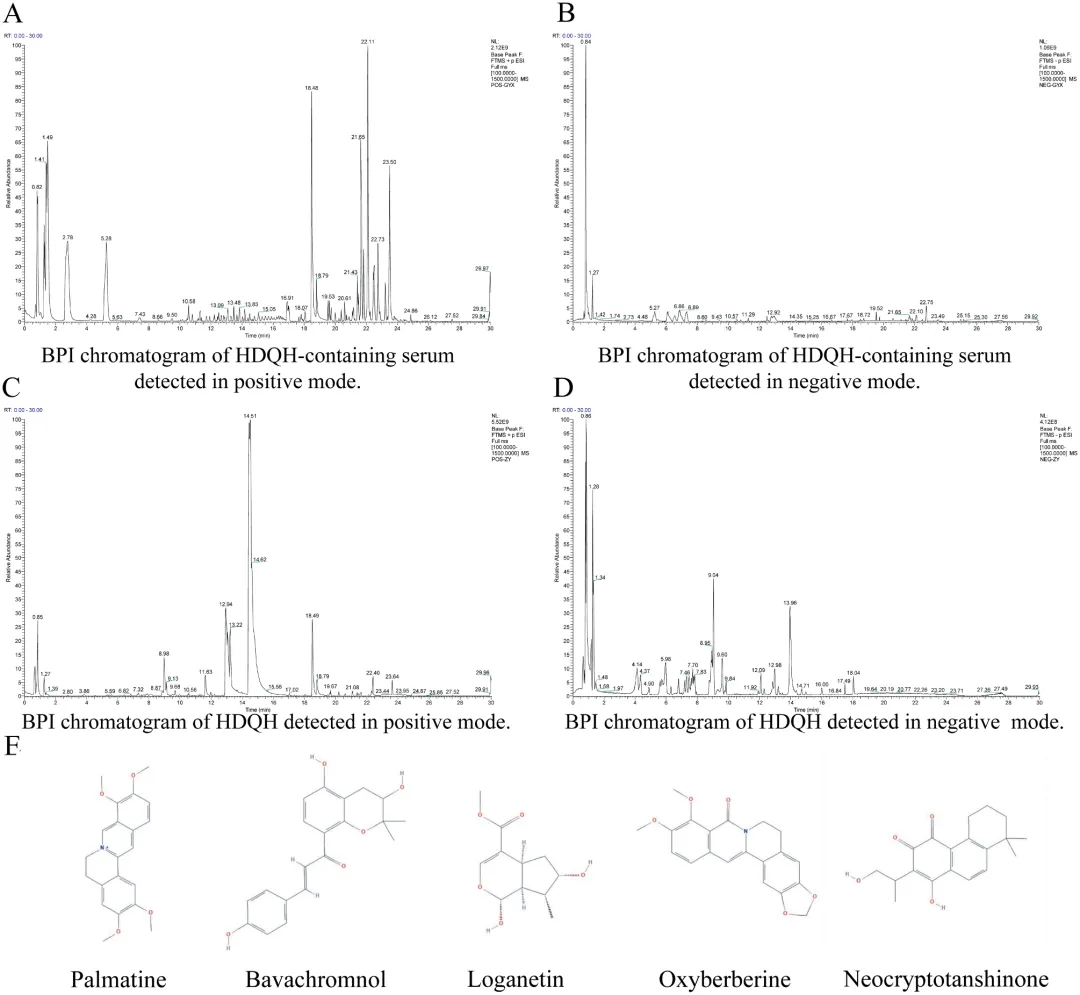
图1 HDQH生物活性化合物的特征。
(A) HDQH含药血清在正离子模式下检测的基峰离子(BPI)色谱图。(B) HDQH含药血清在负离子模式下检测的BPI色谱图。(C) HDQH在正离子模式下检测的BPI色谱图。(D) HDQH在负离子模式下检测的BPI色谱图。(E) HDQH中排名前5位成分的化学结构式。
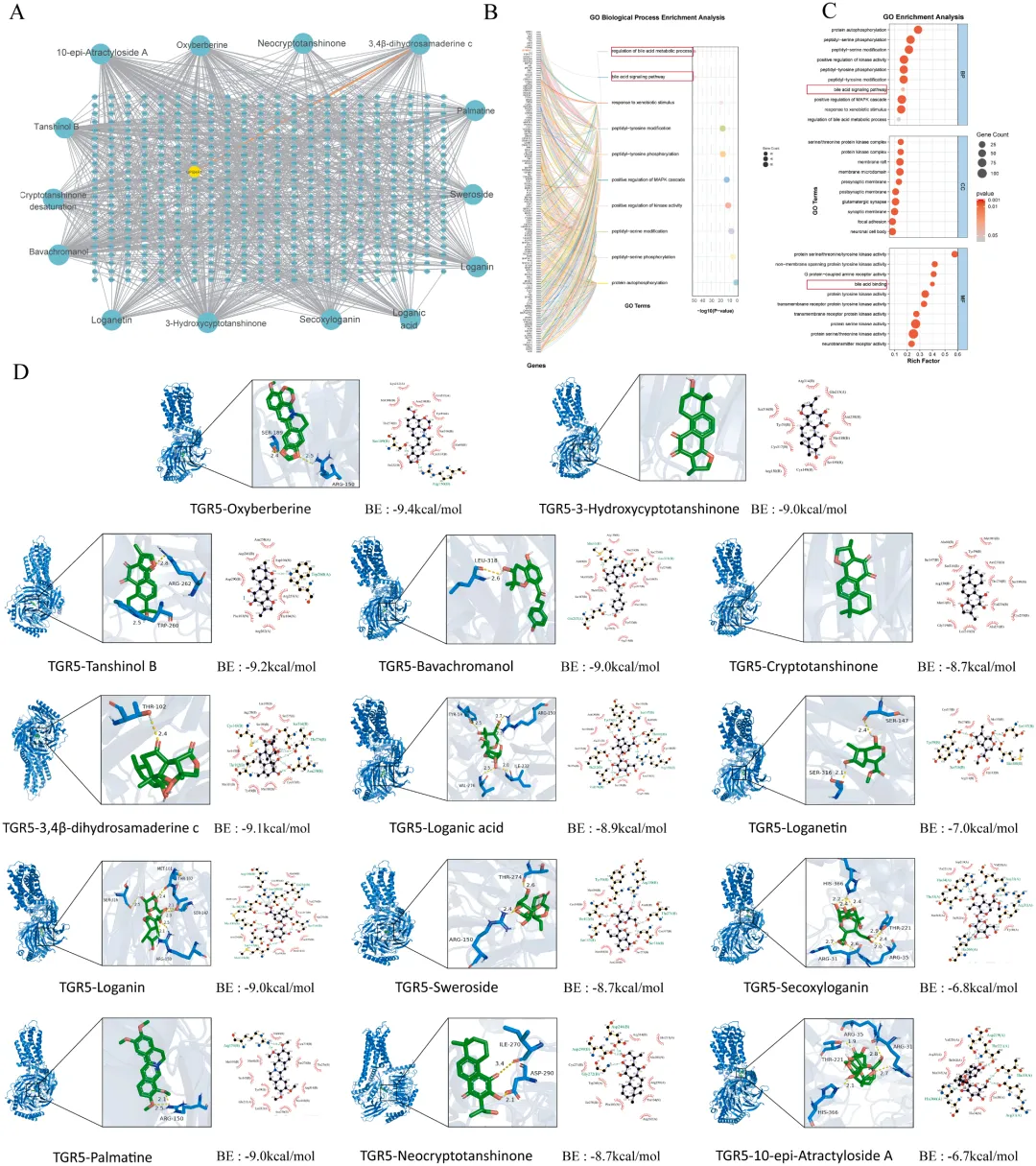
图2 HDQH活性成分靶点预测及TGR5结合验证。
(A) 药物-成分-靶点网络图。(B) GO生物学过程富集分析。(C) GO富集分析(包括生物过程BP、细胞组分CC、分子功能MF)。(D) HDQH活性成分与TGR5的分子对接图。BE:结合能。
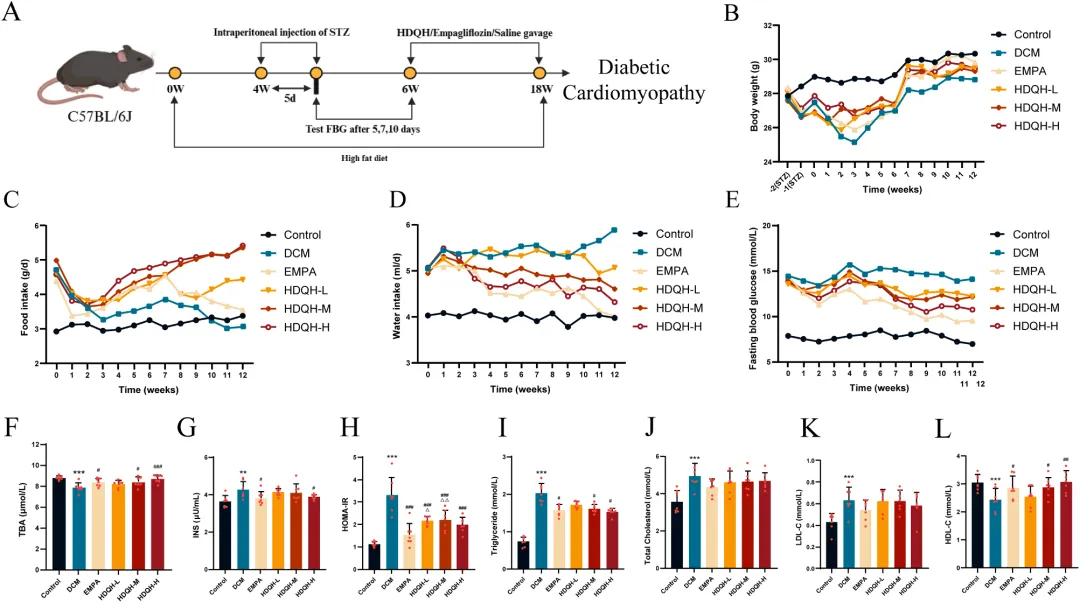
图3 HDQH有效改善DCM小鼠异常的糖脂及胆汁酸代谢。
(A) DCM小鼠模型建立流程图。(B-E) 小鼠12周内体重、摄食量、饮水量及空腹血糖水平的变化。(F-H) 总胆汁酸、胰岛素及稳态模型评估胰岛素抵抗指数。(I-L) 甘油三酯、总胆固醇、低密度脂蛋白胆固醇和高密度脂蛋白胆固醇水平。
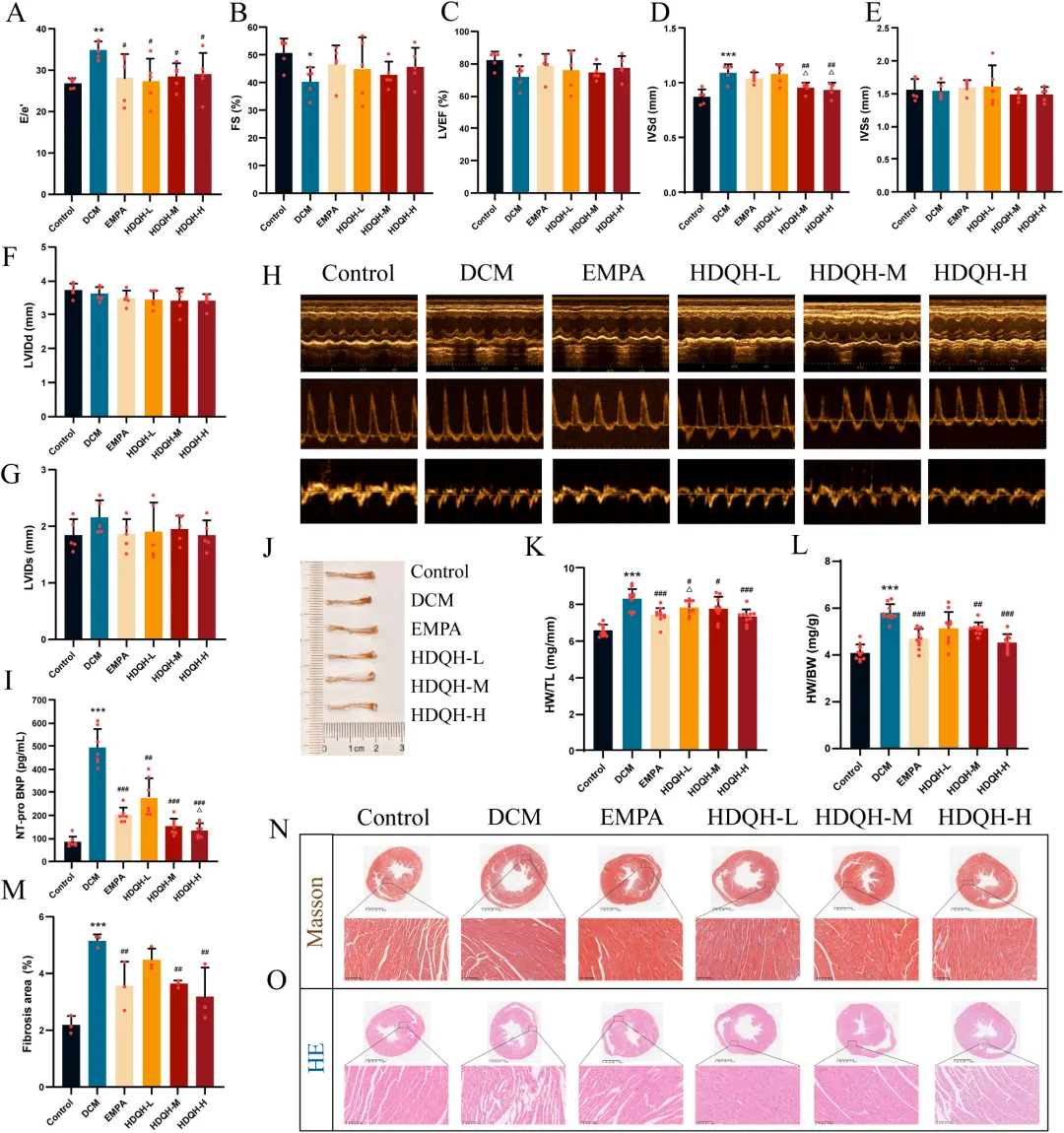
图4 HDQH改善DCM小鼠心脏功能与结构重塑。
(A-G) 峰值E/e'比值、缩短分数、左心室射血分数、舒张期室间隔厚度、收缩期室间隔厚度、舒张期左心室内径、收缩期左心室内径。(H) 超声心动图典型图像。(I) N末端B型利钠肽原(NT-proBNP)水平。(J) 小鼠胫骨照片。(K-L) 心脏重量/胫骨长度(HW/TL)比值和心脏重量/体重(HW/BW)比值。(M) Masson染色测定的纤维化面积。(N-O) Masson染色和HE染色代表性图像。
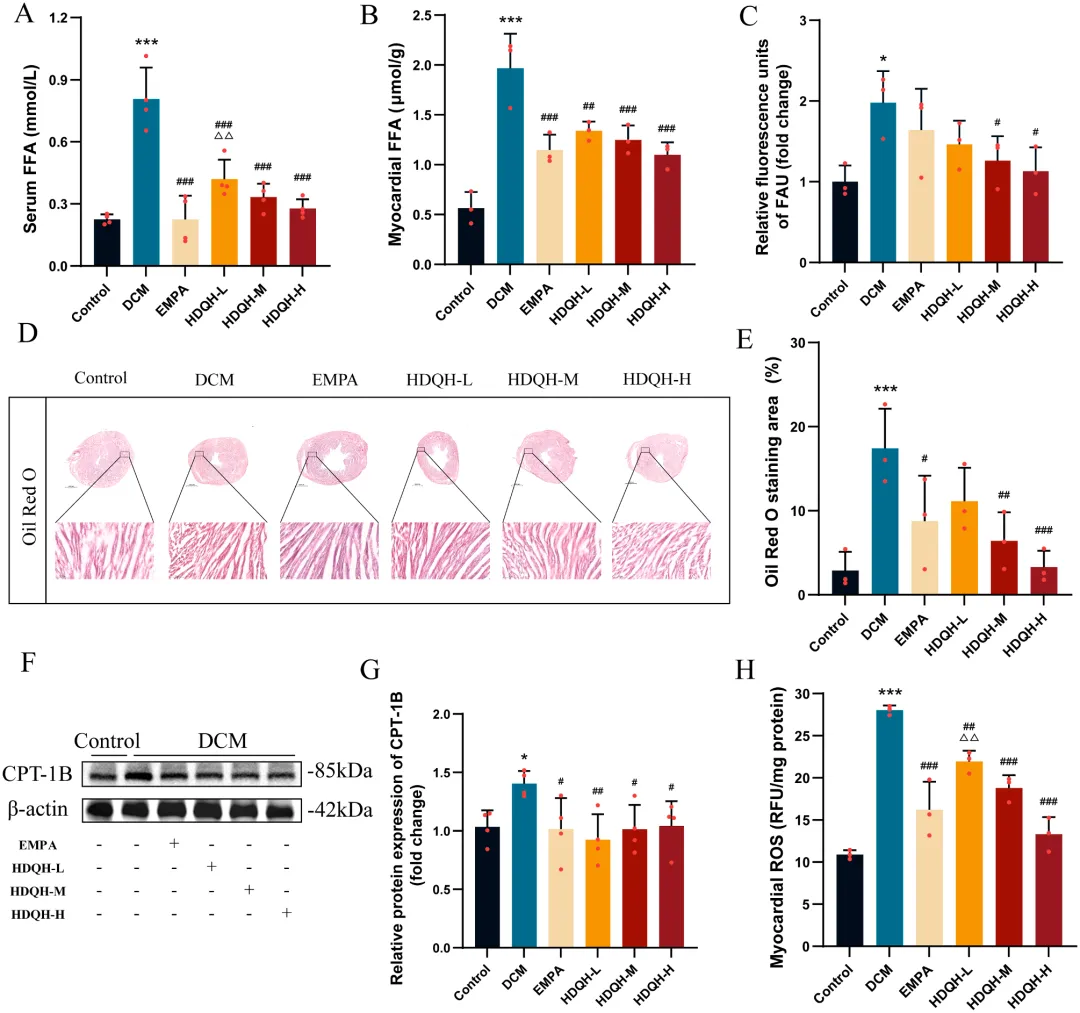
图5 HDQH抑制DCM小鼠心肌脂肪酸摄取(FAU)和脂质蓄积。
(A) 血清中游离脂肪酸(FFA)水平。(B) 心肌组织中FFA水平。(C) 心脏组织中脂肪酸的相对荧光单位(FAU)。(D-E) 油红O染色代表性图像及染色面积百分比。(F) Western blot检测心脏组织中CPT1B蛋白表达水平。(G) 心脏组织中CPT1B相对蛋白表达水平。(H) 心脏组织中ROS水平。
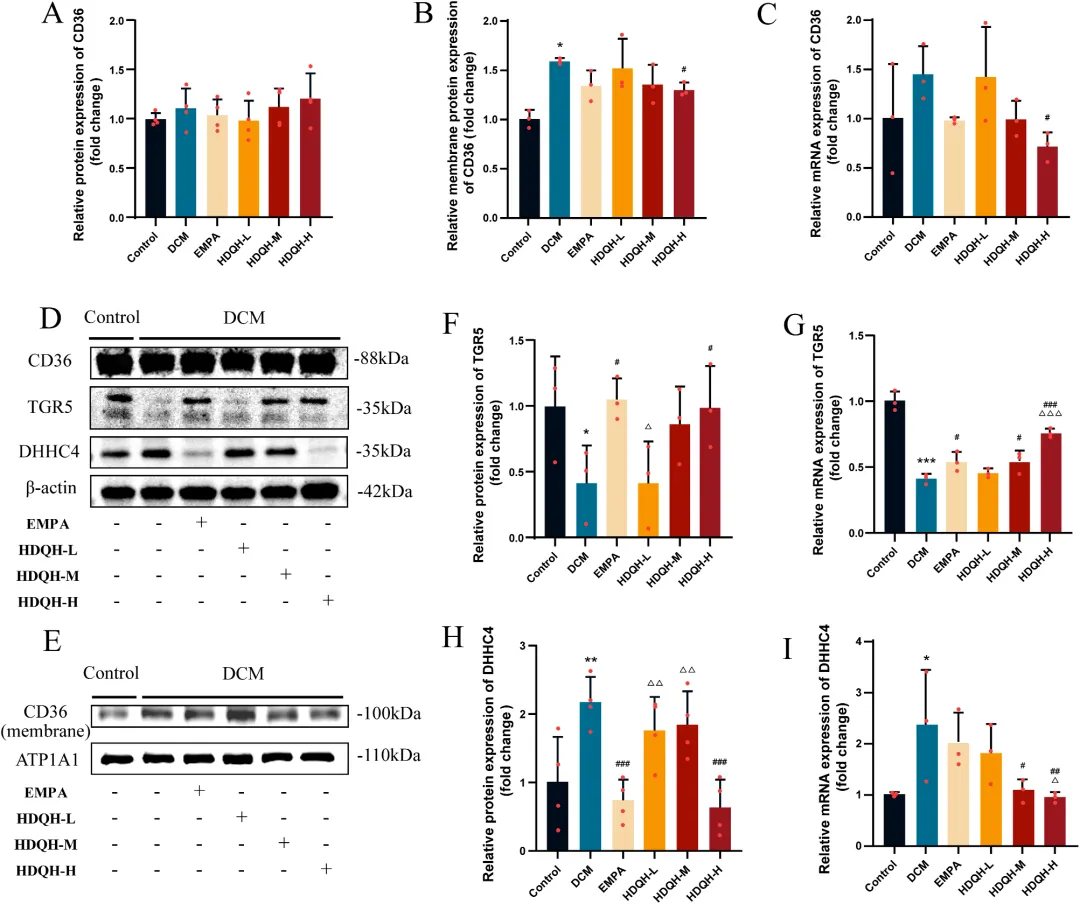
图6 HDQH调控TGR5-DHHC4通路并抑制CD36膜定位。
(A-C) 心脏组织中CD36的总蛋白、mRNA和膜蛋白相对表达水平。(D) Western blot检测心脏组织中TGR5、DHHC4和CD36的蛋白表达水平。(E) Western blot检测心脏组织中CD36膜蛋白表达水平。(F-G) 心脏组织中TGR5的相对蛋白和mRNA表达水平。(H-I) 心脏组织中DHHC4的相对蛋白和mRNA表达水平。
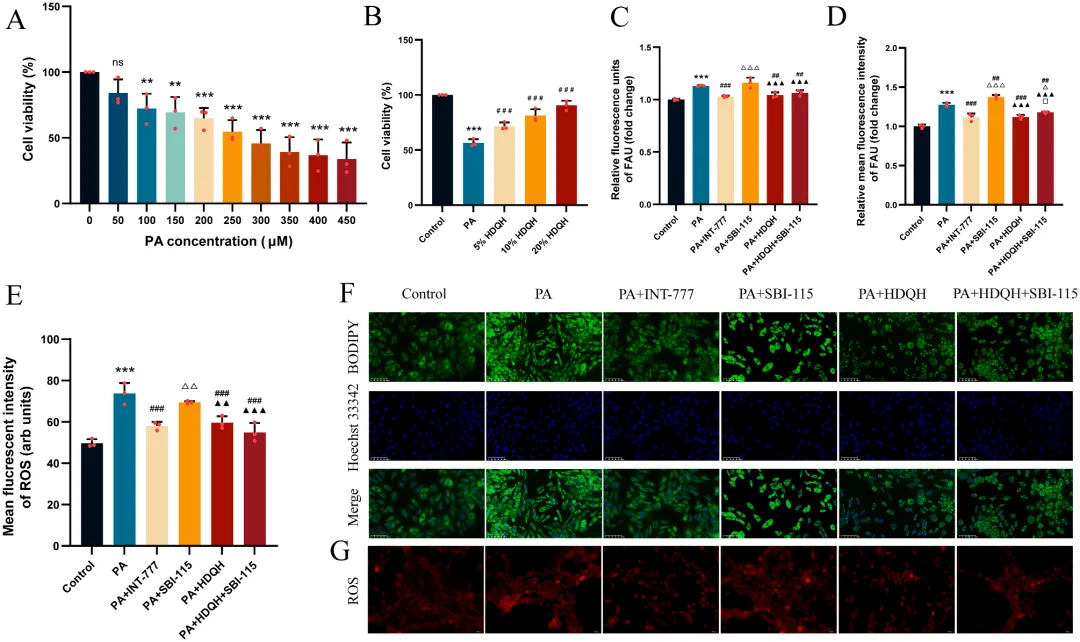
图7 HDQH抑制棕榈酸(PA)诱导的心肌细胞脂肪酸摄取(FAU)。
(A-B) CCK-8法检测不同浓度PA及含药血清对细胞活力的影响。(C) 基于多功能酶标仪检测的心肌细胞FAU相对荧光单位。(D) 荧光显微镜下观察的心肌细胞FAU相对平均荧光强度。(E) 心肌细胞活性氧(ROS)的平均荧光强度。(F-G) 心肌细胞FAU和ROS的典型荧光图像。
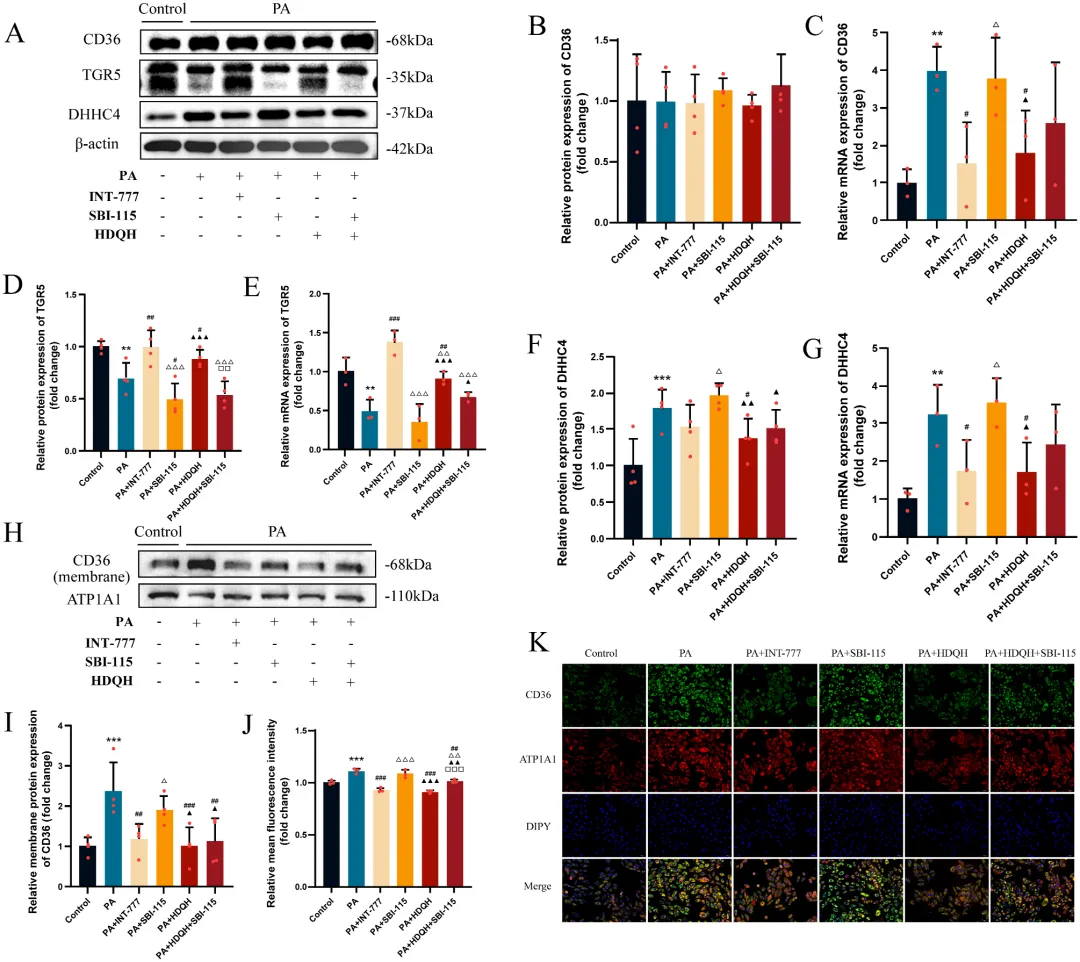
图8 HDQH通过调控TGR5-DHHC4通路抑制CD36膜定位。
(A) Western blot检测心肌细胞中TGR5、DHHC4和CD36的蛋白表达水平。(B-G) 心肌细胞中CD36、TGR5和DHHC4的相对蛋白和mRNA表达水平。(H-I) Western blot检测心肌细胞中CD36膜蛋白及其相对蛋白表达水平。(J) CD36和ATP1A1双重荧光染色的相对荧光强度及代表性图像,显示CD36在膜上的表达。(K) CD36和ATP1A1双重荧光染色的代表性图像。
综上所述,我们的研究证实,藿丹清化方(HDQH)通过调节TGR5-DHHC4信号通路,抑制CD36在心肌细胞膜上的定位,从而减少心肌对游离脂肪酸的过度摄取,降低脂质蓄积和氧化应激,减轻脂毒性诱导的心肌损伤,最终改善糖尿病心肌病小鼠的心脏功能与结构重塑。
HDQH还能上调总胆汁酸水平,改善全身糖脂代谢紊乱,其作用可被TGR5拮抗剂SBI-115部分逆转。尽管尚未明确HDQH中直接激活TGR5的具体活性成分,但本研究充分展示了中药复方通过多成分、多靶点协同作用治疗DCM的潜力,并为靶向TGR5-DHHC4-CD36轴防治糖尿病心肌病提供了新的科学依据。


需要领取文献的同学,后台私信“89”,即可领取!
《医研三人行》公众号推送文章仅为学术交流使用,仅供读者参考。公众号中“原创”标识仅代表原创编译之作,不代表本公众号对文本主张版权。版权归文章作者所有。
1、伊朗德黑兰大学联合新加坡国立大学团队Autophagy发文:营养过剩时代,我们是否需要强制重启细胞的"自清洁"程序?
2、Phytomedicine!广州中医药大学史亚飞、张荣、赵金兰等团队:四逆散如何通过5-HT4R"重启"抑郁大脑的奖赏环路?
3、脑出血治疗新星!郑州大学 薛孟周教授(IF 13):MyD88 抑制肽-2 (MIP2) 可改善脑出血介导的继发性脑损伤后的神经功能预后并减轻神经炎症



