IF38.7!南京医科大学用“国自然”拿下TOP!锁定METTL4动脉粥样硬化治疗新靶点!
- 2026-05-08 14:45:59


🧬线粒体功能障碍是动脉粥样硬化发生发展的关键因素。METTL4是哺乳动物中线粒体DNA N6-甲基脱氧腺苷(6mA)的甲基转移酶,但其在动脉粥样硬化中的作用尚不清楚。
🔎本研究首次发现巨噬细胞中METTL4介导的mtDNA 6mA修饰通过抑制MT-ATP6转录导致线粒体复合物V缺陷、质子积累、ROS爆发、mtDNA泄漏和炎症小体激活,从而促进动脉粥样硬化。研究还筛选出首个METTL4拮抗剂培美曲塞,并开发了靶向斑块巨噬细胞的PROTAC药物,为动脉粥样硬化治疗提供了新策略。
📚如果你也想用“国自然”发文的话,关注兔子生信,联系我们带你进一步了解~

文章标题:METTL4介导线粒体DNA N6-甲基脱氧腺苷修饰促进巨噬细胞炎症和动脉粥样硬化
发表期刊:Circulation
发表时间:2025年4月1日
影响因子:IF38.7/Q1


线粒体功能障碍通过加剧氧化应激、炎症反应、凋亡和胆固醇积累,在动脉粥样硬化发生发展中起重要作用。mtDNA 6mA修饰是近年发现的新型表观遗传修饰,但其在动脉粥样硬化中的作用尚不清楚。METTL4是目前已知唯一能催化哺乳动物mtDNA 6mA修饰的甲基转移酶。


本研究综合运用ox-LDL刺激的巨噬细胞模型、髓系特异性METTL4敲除小鼠、甲基转移酶活性位点突变小鼠、骨髓移植、RNA测序、线粒体移植、化合物库筛选、分子对接和PROTAC技术,系统阐明METTL4在动脉粥样硬化中的作用机制并开发靶向治疗策略。
🌎降脂治疗不能解决的“残余风险”还有什么❓
🌟线粒体功能障碍!它在动脉粥样硬化发生发展中扮演关键角色,但具体机制不清。
🌎METTL4是什么❓
⌛️METTL4是目前已知唯一能催化哺乳动物线粒体DNA发生6mA甲基化修饰的酶。但它在动脉粥样硬化中的作用完全未知。
🌎这篇研究发现了什么❓
🧠首次揭示METTL4在斑块巨噬细胞中显著高表达!它通过催化mtDNA 6mA修饰,抑制MT-ATP6基因表达,导致线粒体复合物V功能障碍、质子堆积、mtDNA泄漏到胞浆,激活炎症小体,驱动动脉粥样硬化!更重磅的是,筛选出首个METTL4抑制剂培美曲塞,并开发了靶向巨噬细胞的PROTAC降解剂,显著减轻动脉粥样硬化!

ox-LDL刺激的人单核细胞来源巨噬细胞中,mtDNA 6mA水平显著升高,而内皮细胞和平滑肌细胞中无变化。METTL4主要定位于巨噬细胞线粒体,敲低METTL4可显著降低ox-LDL诱导的mtDNA 6mA升高(图1)。
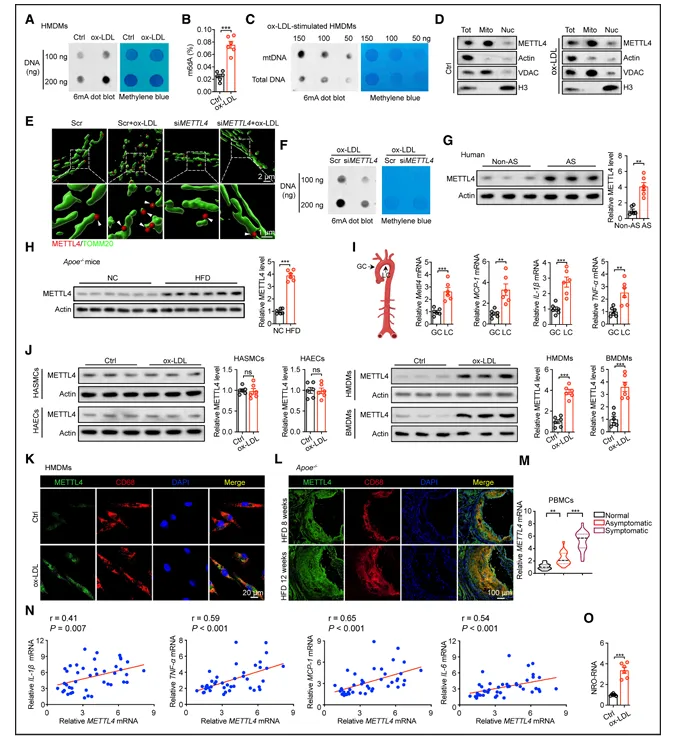
图1.METTL4参与动脉粥样硬化进展
人及小鼠动脉粥样硬化斑块组织中METTL4蛋白和mRNA水平均升高,且主要表达于CD68+巨噬细胞,外周血单个核细胞中METTL4水平与炎症因子IL-1β、TNF-α等呈正相关。ox-LDL刺激可促进METTL4的新生转录。

成功构建髓系特异性METTL4敲除小鼠。高脂饮食喂养12周后,敲除小鼠主动脉斑块面积显著减少,脂质沉积减少,坏死核心减小(图2)。
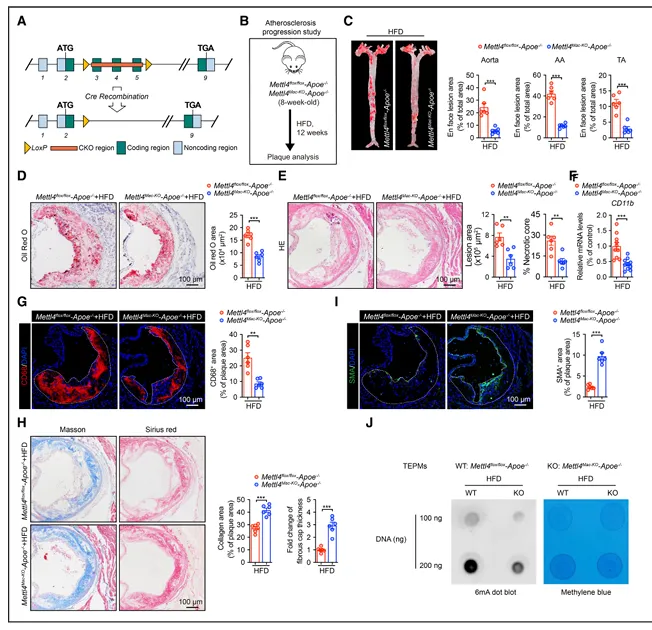
图2.髓系特异性敲除METTL4减轻动脉粥样硬化
斑块内巨噬细胞含量减少,胶原含量、纤维帽厚度和平滑肌细胞含量增加,提示斑块稳定性增强。敲除小鼠腹腔巨噬细胞中mtDNA 6mA水平降低。骨髓移植实验证实上述表型由髓系细胞METTL4缺失所致。

RNA测序显示METTL4敲低影响炎症反应相关基因。METTL4敲低可逆转ox-LDL诱导的线粒体膜电位下降、氧耗率降低、胞外酸化率升高、ROS增加。透射电镜显示METTL4敲低可抑制ox-LDL诱导的线粒体肿胀、嵴断裂和溶解。ox-LDL刺激的HMDM中mPTP开放增加,胞质DNA主要来源于mtDNA,这些现象可被METTL4敲低逆转(图3)。
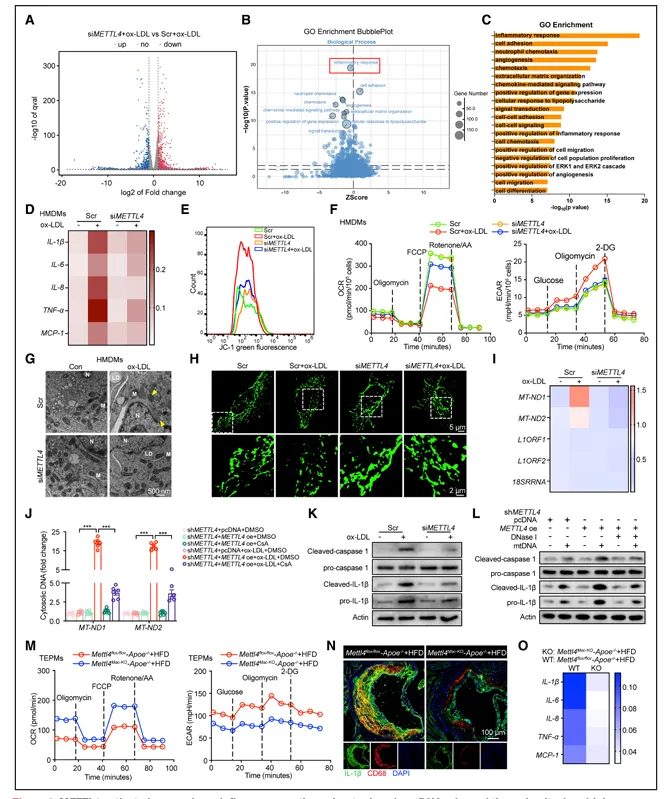
图3.METTL4通过胞质mtDNA激活巨噬细胞炎症小体
线粒体ROS清除剂TEMPO可抑制mPTP开放和mtDNA释放。METTL4敲低可抑制caspase-1和IL-1β活化。从METTL4过表达的巨噬细胞中提取mtDNA转染至naive巨噬细胞可激活炎症小体。在敲除小鼠腹腔巨噬细胞中也观察到线粒体功能改善、mtDNA释放减少、炎症因子降低。

过表达野生型METTL4而非酶活突变体可增加mtDNA 6mA水平。在METTL4敲低细胞中,回补野生型METTL4而非突变体可恢复线粒体ROS产生、mtDNA释放、线粒体膜电位下降和能量代谢障碍(图4)。
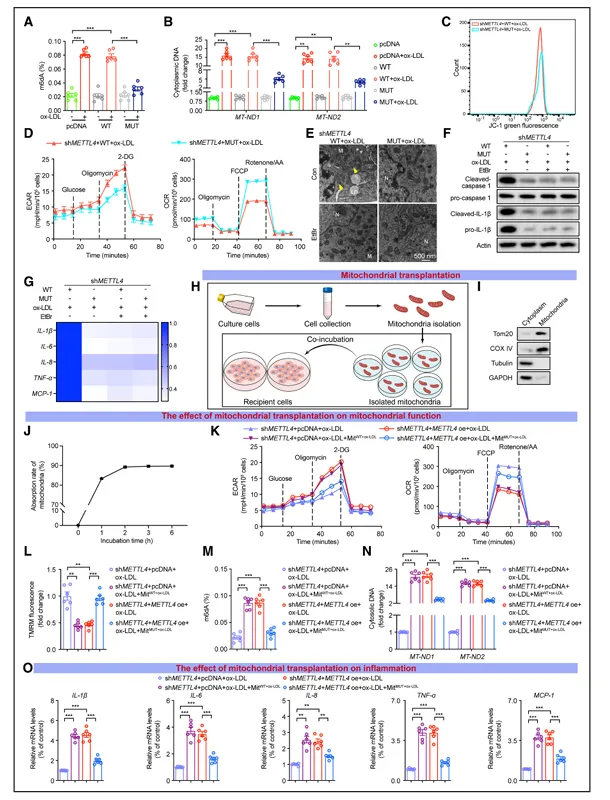
图4.mtDNA 6mA是METTL4调控线粒体功能障碍的关键
使用溴化乙锭耗竭mtDNA的ρ0细胞中,METTL4过表达不再诱导上述表型。线粒体移植实验显示,从野生型METTL4过表达细胞提取的线粒体移植至敲低细胞可诱导线粒体功能障碍和炎症,而突变体来源线粒体则无此效应。

METTL4敲低可增加ox-LDL刺激巨噬细胞中线粒体呼吸链复合物V的活性和表达,并上调MT-ATP6表达。在敲低细胞中回补野生型METTL4而非突变体可降低MT-ATP6表达。MT-ATP6基因存在6mA修饰基序,免疫沉淀显示野生型METTL4过表达可增加MT-ATP6的6mA修饰,减少TFAM与MT-ATP6的结合(图5)。
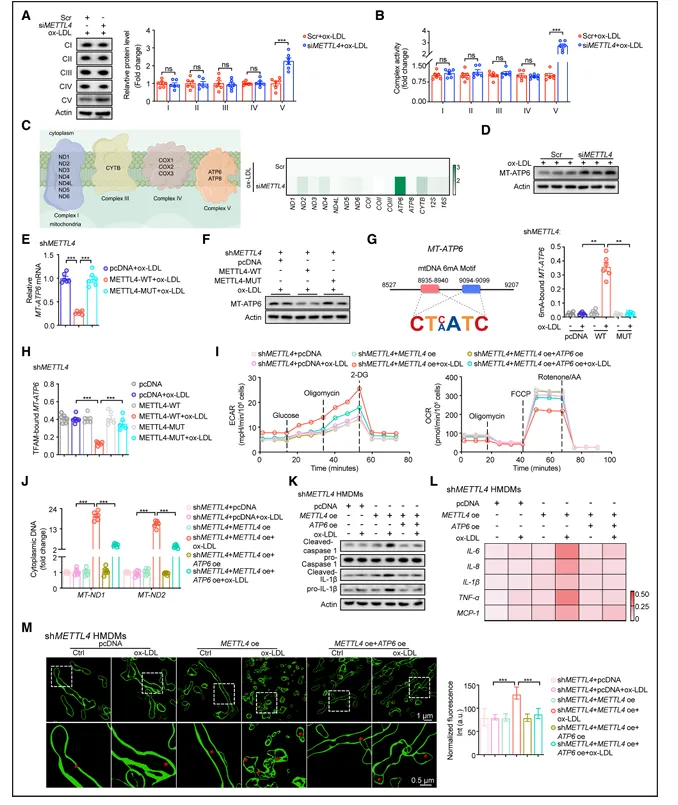
图5.METTL4介导的MT-ATP6 6mA导致质子积累
回补ATP6可逆转METTL4过表达诱导的线粒体功能障碍、mtDNA释放和炎症。METTL4过表达导致线粒体膜间隙质子积累,回补ATP6可逆转此现象。

成功构建METTL4酶活位点突变小鼠。高脂饮食后,突变小鼠主动脉斑块面积减少,mtDNA 6mA水平降低,脂质沉积减少,坏死核心减小,巨噬细胞含量减少,胶原和平滑肌细胞增加,斑块内炎症因子降低(图6)。
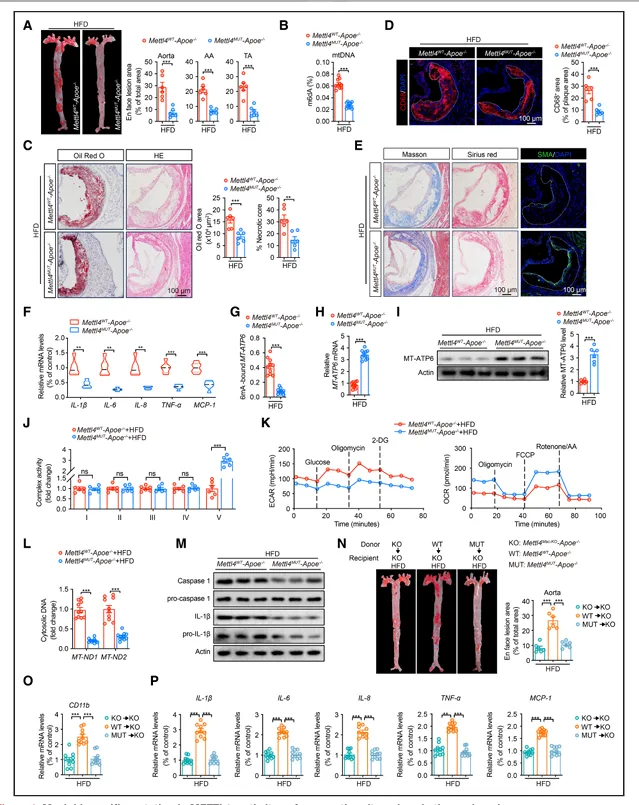
图6.髓系特异性METTL4酶活突变减轻动脉粥样硬化
突变小鼠腹腔巨噬细胞中MT-ATP6 6mA修饰减少、MT-ATP6表达增加,复合物V活性升高,线粒体能量代谢改善,mtDNA释放减少,炎症小体活化受抑。骨髓移植实验证实上述表型依赖于髓系细胞METTL4酶活。

通过基于结构的虚拟筛选,从TargetMol化合物库中筛选出18个候选化合物,其中培美曲塞、烟酸占替诺和利格列汀可抑制METTL4甲基转移酶活性。培美曲塞可有效逆转ox-LDL诱导的MT-ATP6降低和炎症因子升高,最佳作用浓度为75 nM。培美曲塞可减少MT-ATP6 6mA修饰,降低线粒体ROS、胞质mtDNA积累和炎症因子表(图7)。
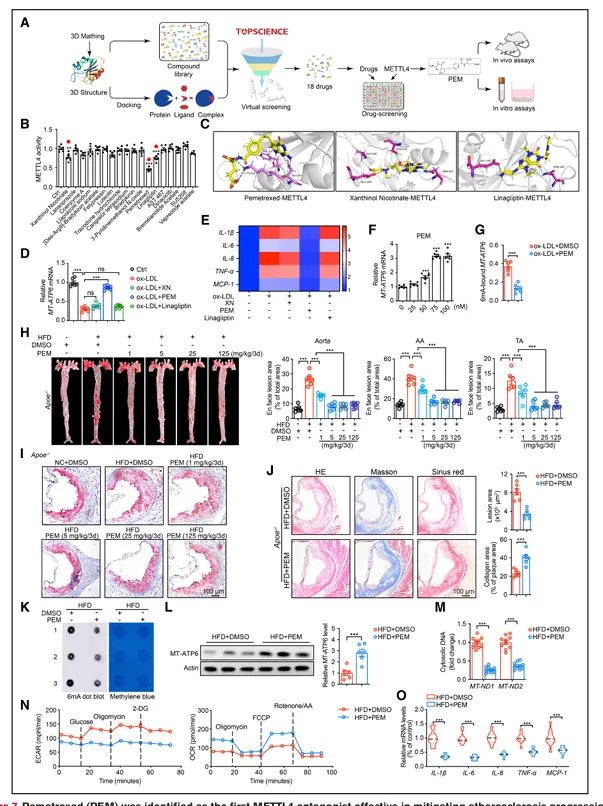
图7.培美曲塞是首个METTL4拮抗剂
在Apoe^-/-小鼠中,培美曲塞可显著减少主动脉斑块面积和脂质沉积,增加胶原含量和纤维帽厚度。培美曲塞处理小鼠腹腔巨噬细胞中mtDNA 6mA降低、MT-ATP6增加、mtDNA释放减少,线粒体功能改善,炎症因子降低。
本研究首次揭示METTL4介导的mtDNA 6mA修饰在动脉粥样硬化中的关键作用。动脉粥样硬化斑块巨噬细胞中METTL4和mtDNA 6mA水平升高;METTL4通过催化MT-ATP6基因6mA修饰,抑制其转录,导致线粒体复合物V缺陷、质子积累、ROS爆发、mPTP开放和mtDNA泄漏,激活炎症小体;
髓系特异性敲除或酶活突变METTL4可显著减轻动脉粥样硬化;筛选出首个METTL4拮抗剂培美曲塞,可有效抑制METTL4活性并减轻动脉粥样硬化;开发靶向斑块巨噬细胞的PROTAC-PEM,通过降解METTL4发挥更强更特异的治疗作用。该研究为动脉粥样硬化提供了新的治疗靶点和策略。
如果你也想用“国自然”进行发文,思路复现,那就快来联系我们吧~







