IF13.3!多组学+分子对接!南京医科大学“国自然”研究拿下双一区TOP!
- 2026-03-24 10:04:51


结肠腺癌(COAD)是第三常见的诊断癌症,也是癌症相关死亡的第二大原因,估计每年造成903,859人死亡。尽管多种治疗策略不断进步,但仍有相当比例的患者出现治疗抗性,尤其是转移性疾病患者,其5年生存率骤降至15%以下。这一临床危机主要源于COAD的分子异质性,这导致了不同的治疗反应,并促进了先天和获得性抗性机制。COAD的治疗效果尚未达到理想水平,这强调了迫切需要发现创新的分类策略,以优化风险分层并指导临床干预。
↓关注云端生信,获取更多科研洞察↓
用分子对接发文真的并不难,需要用分子对接进行发文的话快关注我们后台咨询吧!创新选题,精准辅导!

标题:程序性细胞死亡相关亚型的鉴定揭示了结肠癌中的免疫异质性和治疗分歧
发表期刊:Theranostics
发表时间:2026年2月18日
影响因子:13.3/Q1
在结肠腺癌(COAD)中,治疗耐药仍然是一个关键挑战。程序性细胞死亡(PCD)途径的失调显著影响治疗反应,但其在塑造肿瘤微环境(TME)和驱动COAD临床异质性中的整体作用尚不明确。
研究方法
1️⃣多组学分析与功能注释
▷通过差异表达分析、功能富集分析、突变谱分析(如TMB、MSI状态)、免疫浸润分析(CIBERSORT)、TIDE评分等,系统比较三种亚型的分子特征、免疫微环境及治疗响应差异。
2️⃣单细胞与空间转录组分析
▷利用单细胞RNA-seq数据解析不同亚型中细胞组成和细胞间通讯,重点分析了肿瘤细胞与成纤维细胞之间的MDK-SDC2相互作用。结合空间转录组数据验证其在组织中的空间共定位。
3️⃣药物敏感性预测与分子对接
▷使用oncoPredict工具和GDSC2数据库预测药物敏感性,识别出与SDC2表达显著相关的药物,进一步通过分子对接(MOE软件)验证sunitinib与SDC2的结合能力。
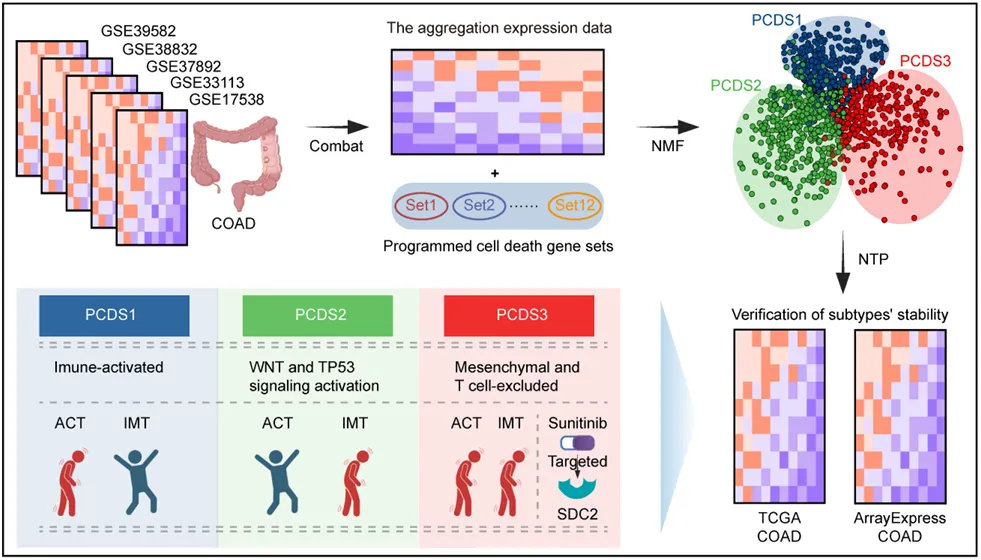
图1 研究设计示意图
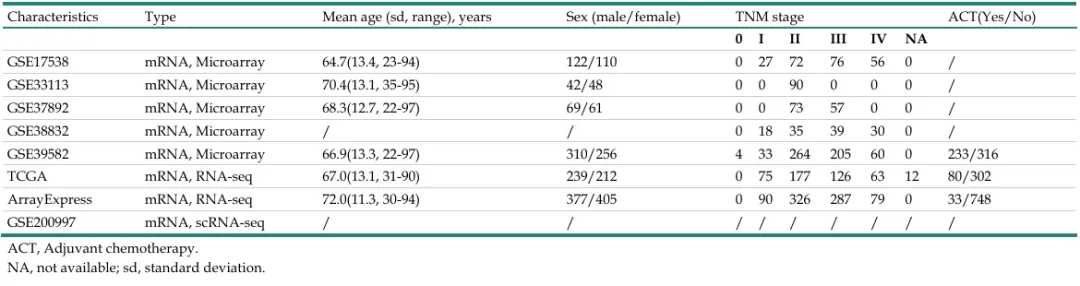
表1 不同数据集的患者和肿瘤特征

你也想尝试这方面的选题?你也想get同款数据库,却不知道该如何下手?不要再犹豫了,快来联系云端生信团队!我们为你提供专业的团队服务,数据分析,思路设计统统不再是问题!
👨🔬首次系统整合12种PCD通路构建结肠癌分子亚型
与传统CMS分型相比,PCDS分型更聚焦于细胞死亡通路与治疗耐药之间的关系,揭示了不同亚型在免疫微环境、治疗响应上的显著差异。
📰发现PCDS3为“双重耐药”亚型
PCDS3患者对化疗和免疫治疗均不敏感(>80%无响应),预后最差。其机制与成纤维细胞富集、T细胞功能障碍/排斥密切相关。
🔬揭示MDK-SDC2信号轴在免疫排斥中的作用
单细胞和空间转录组分析发现,PCDS3中肿瘤细胞通过MDK与成纤维细胞上的SDC2相互作用,与T细胞排斥和功能障碍密切相关,mIF染色进一步验证了这一空间共定位。
🧬提出sunitinib作为PCDS3的潜在靶向治疗药物
通过药物敏感性预测和分子对接,研究首次提出sunitinib可能通过靶向SDC2,打破肿瘤-成纤维细胞间的免疫屏障,为PCDS3患者提供了新的治疗策略。
COAD中稳健PCDS的鉴定
这些亚型特异性的基因特征在转录组水平上划分了三个明确分离的患者群体,支持了每个PCDS的生物学差异性(图2A)。303个特征基因在三个PCDS中的表达模式及患者相应的临床特征显示在热图中(图2B)。
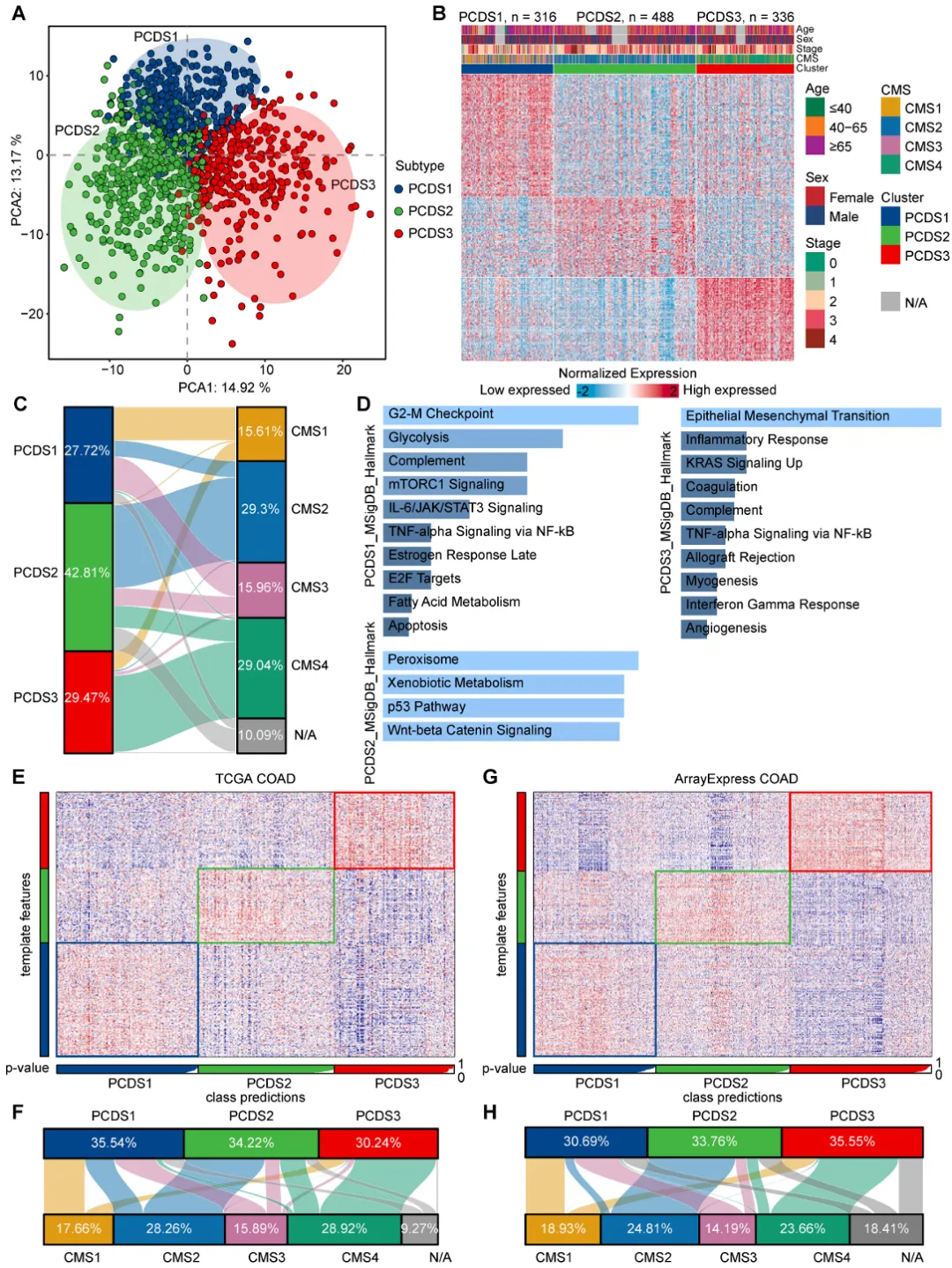
图2 PCDS的定义及稳健性验证
我们还比较了这两个验证数据集中PCDS和CMS分类的患者比例(图2F、H),结果显示的模式与基于微阵列的分类(图2C)中观察到的相似,表明PCDS分类是一个稳健的亚型框架。
描述与PCDS相关的
基因改变和临床预后
我们发现三种PCDS之间的不匹配修复基因表达状态和微卫星不稳定性状态分布显著不同(图3B-C)。具体而言,PCDS2患者表现出较高水平的功能性MMR表达,其MSI状态主要表现为微卫星稳定或低频不稳定。
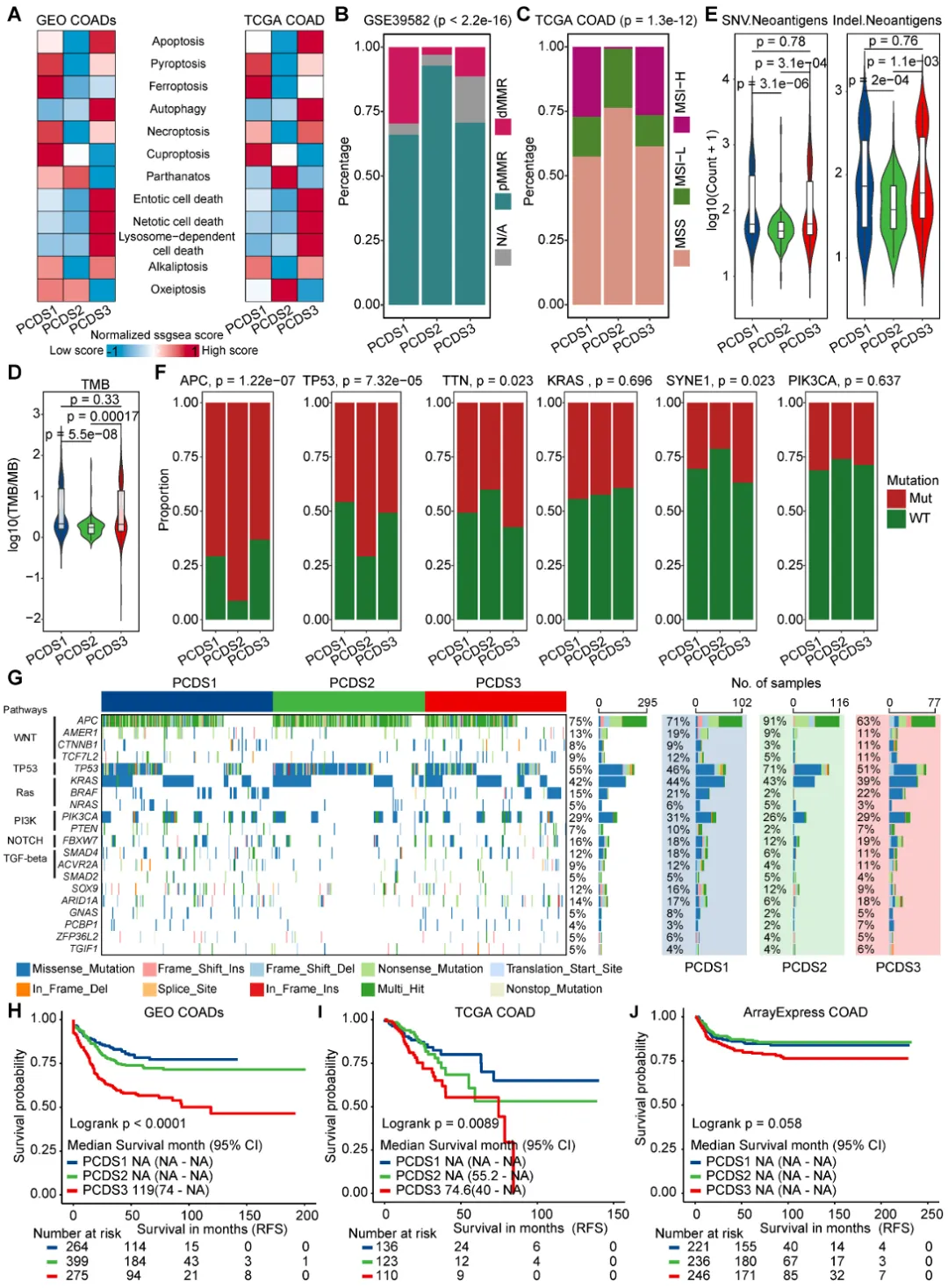
图3 PCDS的遗传特征和临床结局的特征分析
我们使用TCGA COAD突变数据研究了PCDS与驱动基因突变之间的关系,最初对前50个高频突变基因进行了特征化。根据整体突变谱计算的TMB显示PCDS1和PCDS3患者的TMB显著高于PCDS2患者(图3D)。
确定PCDS在化疗和免疫
治疗反应中的特异性变异
免疫去卷积分析显示三种PCDS的免疫细胞组成存在显著差异,特别是在T细胞和巨噬细胞群体中,这暗示了对免疫治疗反应的潜在影响(图4A)。
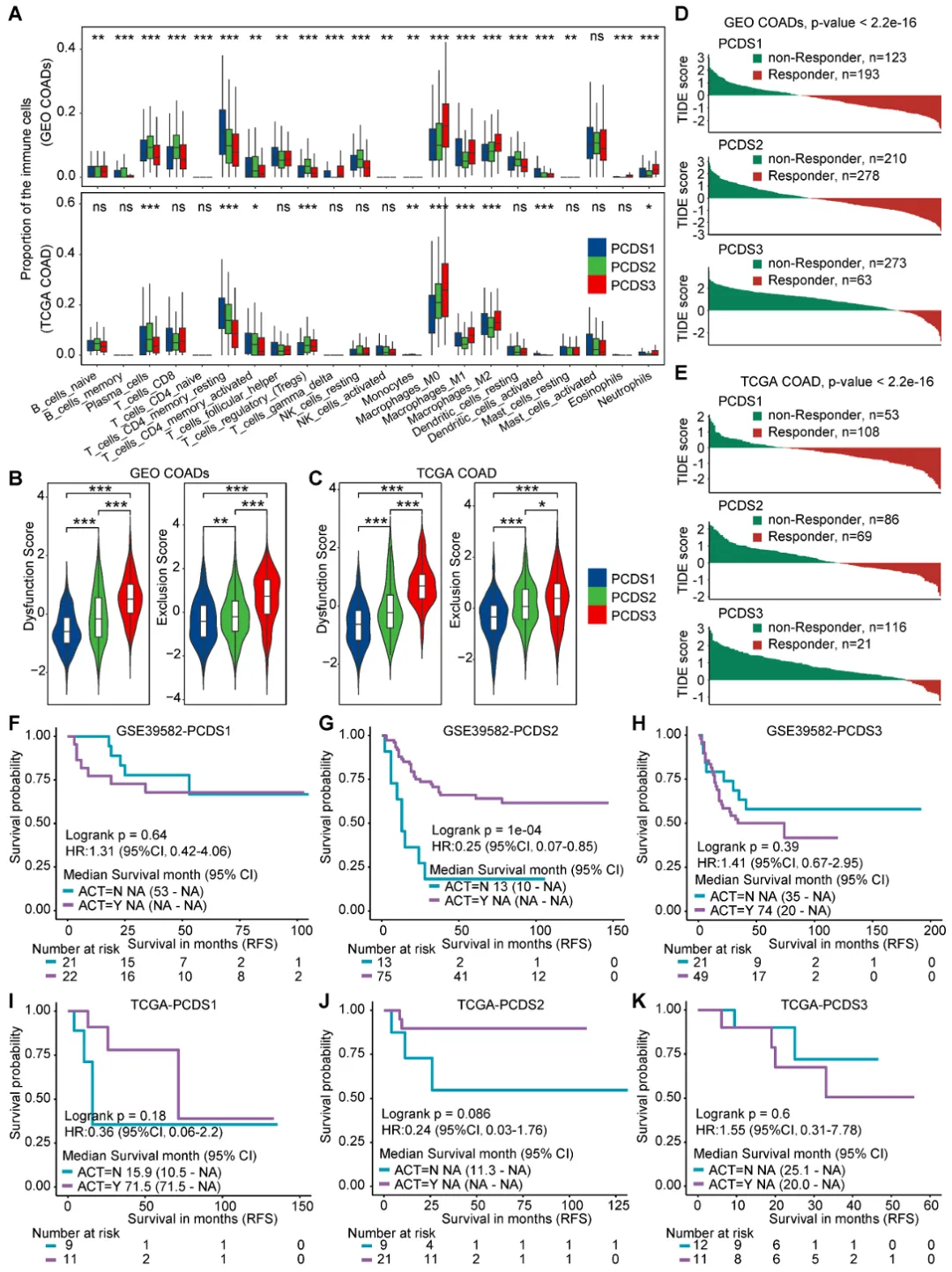
图4 PCDS对化疗/免疫治疗的差异性反应
TIDE评分是预测ICB反应的有效工具,我们在PCDS3患者中观察到明显的T细胞功能障碍和排斥特征(图4B-C)。
单细胞分析描绘了三种
PCDSs中TME的差异
使用来自GSE200997的COAD患者成对的整体RNA-seq表达谱,我们应用NTP算法将他们分类为三种PCDS,每个亚型各有五名患者(图5A)。处理后的scRNA-seq数据集包含7个邻近正常组织和16个肿瘤组织,共获得49,859个高质量的单细胞。
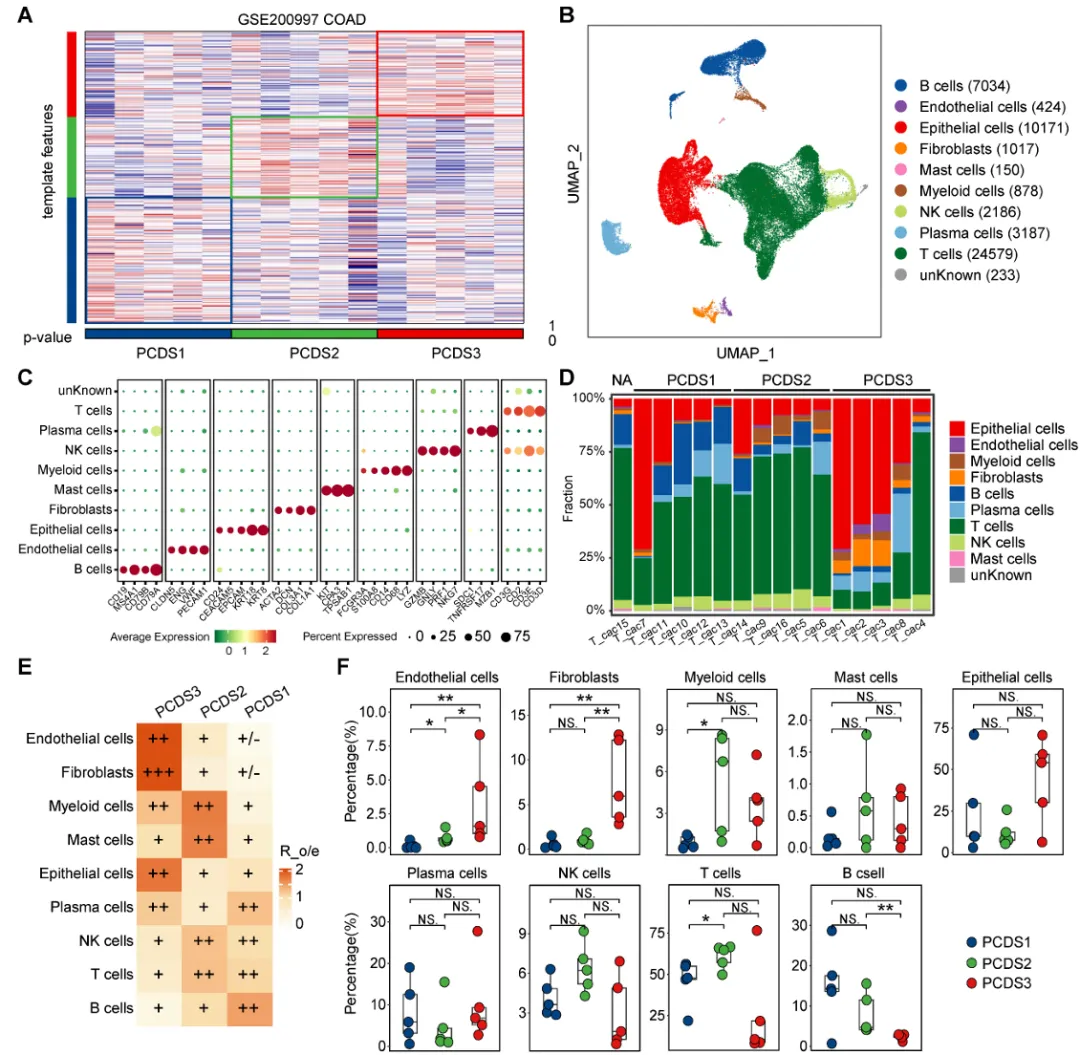
图5 不同PCDS患者的肿瘤微环境描述
我们通过使用带有PCDS标签的患者数据计算观察到的细胞数量与预期细胞数量的比值,定量评估了主要细胞群的相对PCDS富集(图5D-E)。结果显示,PCDS3患者的内皮细胞和成纤维细胞明显富集。
肿瘤细胞与成纤维细胞
的细胞间相互作用揭示了
PCDS3患者的潜在治疗靶点
我们使用CopyKAT从10,171个上皮细胞中识别出2,568个恶性肿瘤细胞,随后将成纤维细胞亚群分为三个子群,并通过已建立的谱系特异性标志物将其标注为肌成纤维细胞、炎症性CAF和抗原呈递CAF(图6A-B)。
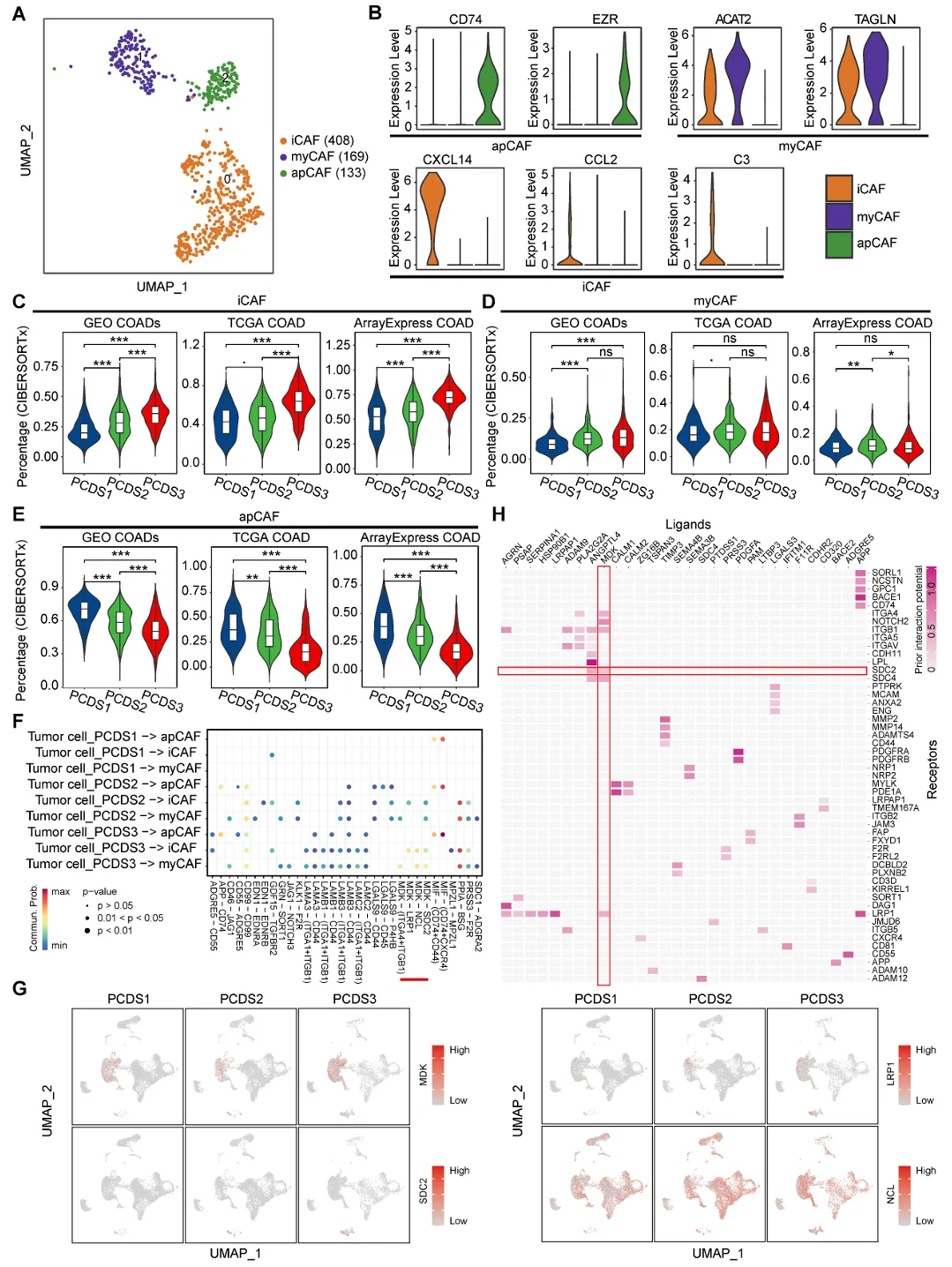
图6 不同PCDS中成纤维细胞的特征描述
MyCAF的浸润在三种PCDSs之间未显示出显著差异(图6C-E)。使用CellChat来识别参与三种PCDSs中肿瘤细胞与成纤维细胞相互作用的配体受体对。
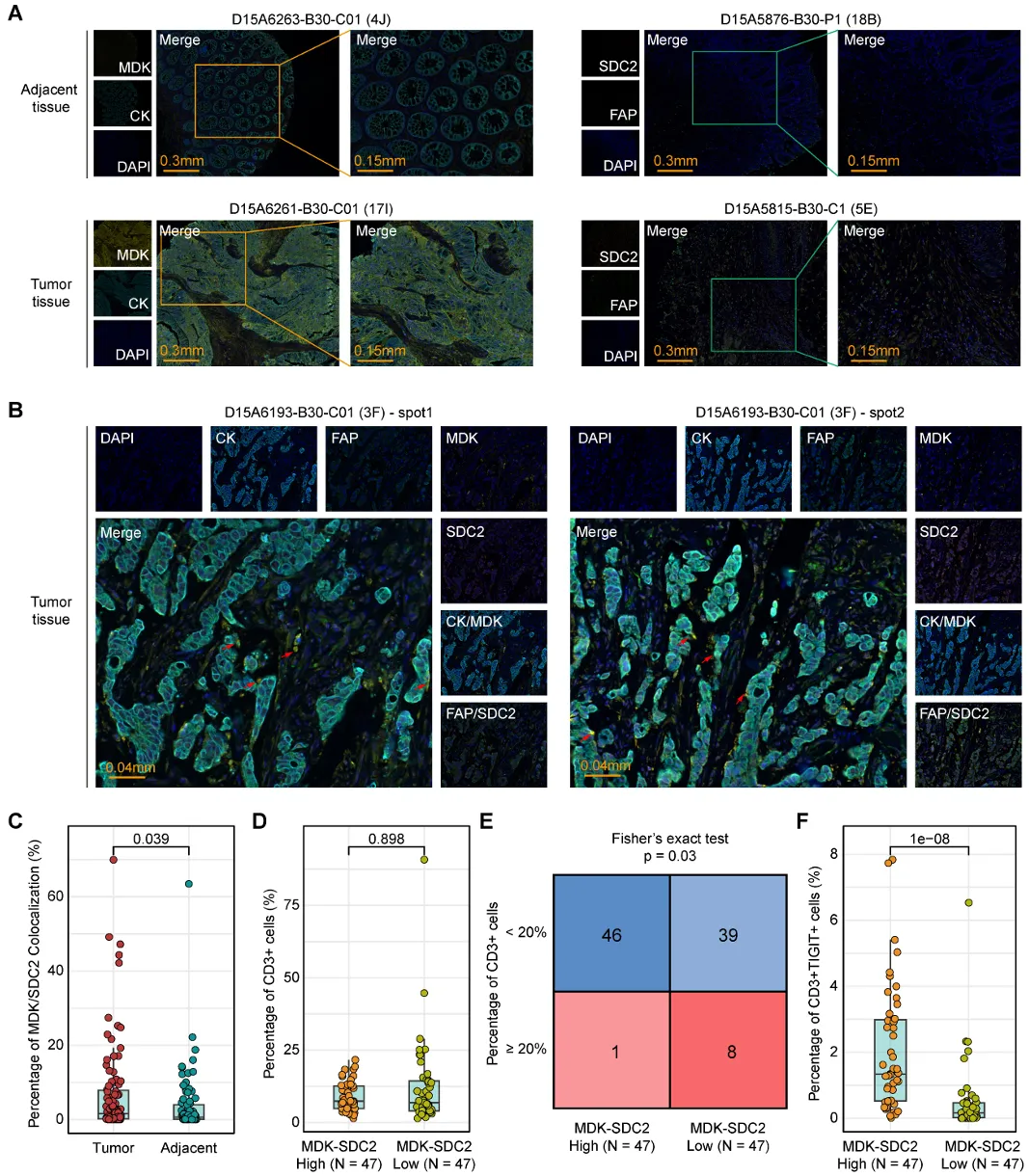
图7 MDK–SDC2介导的肿瘤–成纤维细胞相互作用与T细胞功能障碍及排斥的关联
我们在组织层面寻求正交的实验验证。对94例结直肠癌患者的肿瘤组织和86例配对邻近组织进行的mIF染色证实了肿瘤细胞来源的MDK与成纤维细胞来源的SDC2在肿瘤区域的空间共定位(图7A-B)。
使用舒尼替尼针对SDC2
对PCDS3患者是一
种潜在的治疗策略
我们在三个COAD队列中重新验证了配体MDK和受体SDC2的表达水平,发现与其他两个亚型相比,PCDS3患者的SDC2表达始终显著更高(图8A-C)。
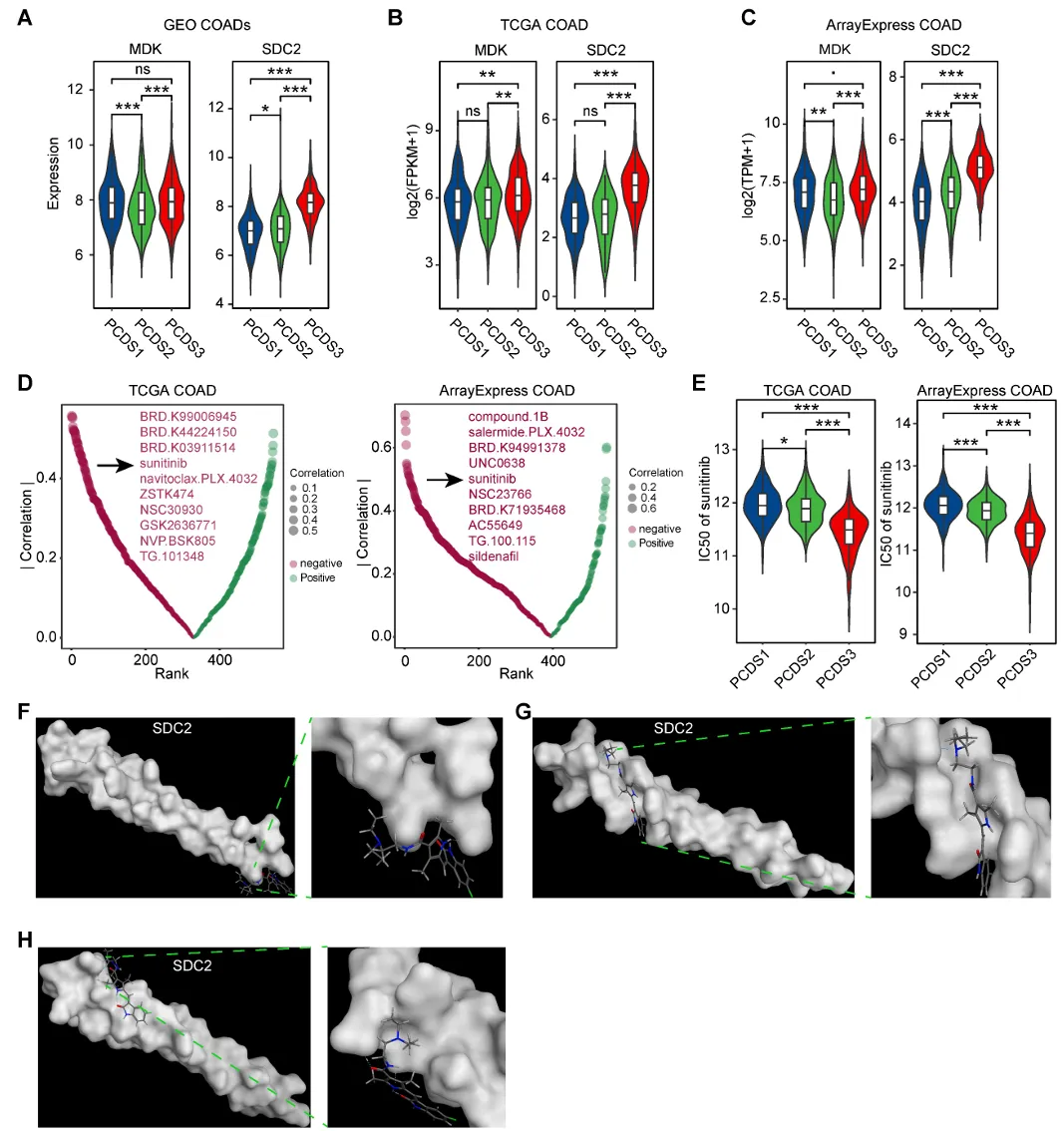
图8 PCDS3患者潜在靶向药物的识别
我们确定了舒尼替尼与SDC2之间的多种结合构象,如图8F-H所示,前三种结合构象的S分数分别为-17.2199(图8F)、-15.4535(图8G)和-13.8831(图8H),这表明舒尼替尼是SDC2一种有前景的潜在靶向药物。
本研究通过整合12种程序性细胞死亡通路,将结肠癌分为三种分子亚型,其中PCDS3亚型预后最差,对化疗和免疫治疗双重耐药。单细胞分析揭示MDK-SDC2信号轴介导的肿瘤-成纤维细胞互作是导致T细胞排斥的关键机制,而舒尼替尼可通过靶向SDC2为该亚型提供潜在治疗策略。
如果你也想分子对接进行数据分析、思路复现,那就快联系云端生信吧!


IF15.7!五图登顶《Nature Communications》!用机器学习拿下一区“豪门水刊”!

