
柔性电子器件开创了新一代可弯曲、可折叠、可拉伸的电子设备,使其能够自由改变形状并附着于各类物体表面。为实现有效功能,这些设备需与目标物体集成以进行原位检测。柔性电子器件与目标表面之间柔软、共形的粘附对于健康监测、运动追踪和人机交互至关重要,因其能提升检测能力并最大限度减少运动伪影。然而,植物、人体及其他自然与人造物体等目标表面具有复杂不规则特性,常呈现不规则、多毛发及动态可变形特征(图1a),这对实现无缝集成构成重大挑战。柔性电子器件与非标准化生物组织的共形集成对下一代可穿戴设备至关重要。然而,柔性器件主要采用传统平面形式制造,与生物体的非平面、多毛或动态表面不相容。
来自南京邮电大学的赵强等团队通过引入一种通用的固-液-固相变策略改进了柔性器件的相容性问题。该方法采用水溶性聚乙烯醇(PVA)作为基底,润湿时暂时液化流动以匹配目标形貌,随后原位固化,实现完美的共形界面。该过程使重构器件能与皮肤建立牢固(界面韧性约29 J m−2,拉伸强度约161 kPa)、可拉伸且无应力的界面。此外,这种强韧界面允许在强粘附与弱粘附间可逆切换,同时可按需溶解实现无痛、无创移除。本文通过形状自适应传感器和电极验证了该方法的有效性:这些器件可无缝包裹脆弱蠕动的蚕体实现运动追踪,也能贴合多毛带刺的叶片进行植物电生理监测,将可穿戴电子设备的应用范围拓展至以往难以触及的生物表面。相关工作以题为“Phase-Transition-Driven Adaptive Reconfiguration of Wearable Devices for Conformal Biointerfaces”的文章发表在2026年04月13日的期刊《Advanced Materials》。

【创新型研究内容】
在实际应用中,柔性器件的使用常涉及与皮肤的直接接触,"共形"这一术语被广泛采用。然而,将大多数仅贴合在皮肤上的柔性器件描述为具有共形接触并不准确。真正的"共形接触"要求器件在目标表面的每个点上都匹配其曲率。因此,即使是基于褶皱、蛇形或波浪形结构的高拉伸性器件,也只能实现宏观接触;其微观结构起伏阻碍了真正的亚微米级共形贴合。超薄柔性电子器件通过最小化弯曲刚度和半径来实现无缝可穿戴传感器,但需要外部压力才能有效接触。相比之下,亚微米厚度的器件可以仅依靠范德华力建立接触,但仍受限于其固有的平面几何形状,缺乏主动重塑和适应任意表面形貌的能力。为匹配曲面目标,大多数柔性器件通过机械弯曲、拉伸或扭曲来近似局部形貌。这些基于变形的方法受限于有限的弯曲刚度、累积的应变能以及可能损坏器件和目标的内应力。因此,它们仅能适应简单的可展曲面(如圆柱体、圆锥体),而无法在不可展曲面(如半球体、鞍形曲面;图1b)上实现无应力、无褶皱的共形贴合。柔性器件与不可展曲面之间的这种界面会产生气隙,影响原位检测。
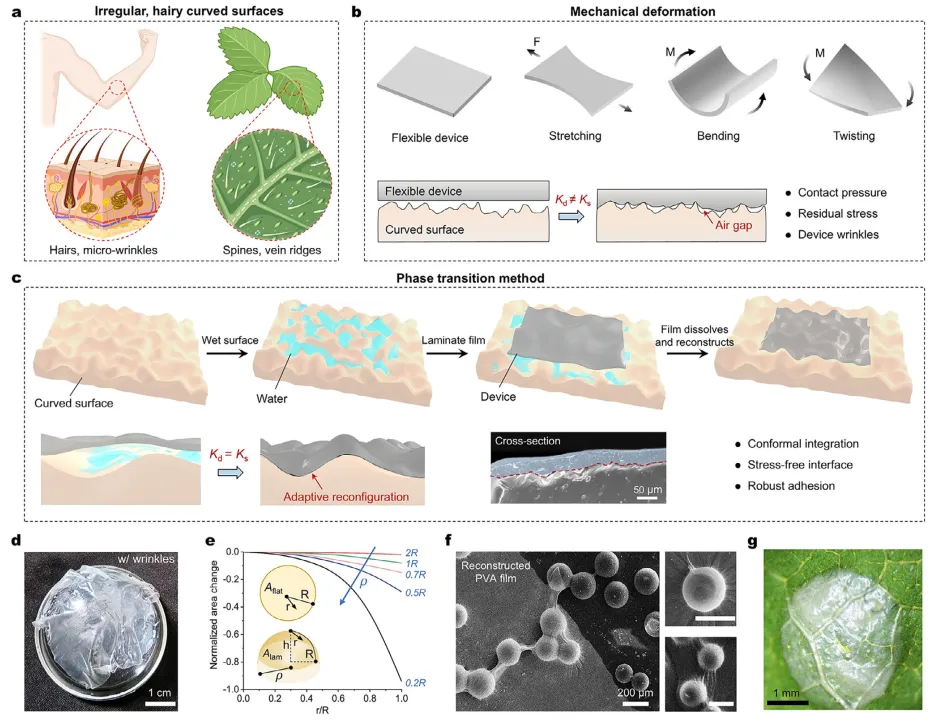
图1 共形紧密生物电子界面的相变构建方法
【重构PVA薄膜的力学性能】
图2a展示了PVA薄膜的固-液-固转变过程。初始状态下,PVA薄膜保持稳定的固态,具有一定弯曲刚度,其最小弯曲半径限制了其对目标微观形貌的适应能力。施加水滴后,PVA薄膜在数秒内从固态转变为液态。该状态赋予PVA储存模量与损耗模量等流变特性,使其能够重新流动并适应目标表面。最终通过水分蒸发,PVA薄膜重新固化并与目标形成牢固粘附。图2b展示了固态PVA薄膜与重构PVA薄膜在曲面上的有限元模拟变形结果:固态薄膜仅在接触峰处形成桥接,产生气隙;而液相PVA均匀铺展,实现>99%的表面接触并消除界面空隙。模拟结果表明,重构薄膜通过利用液态PVA的流变性实现了与结构的高度共形接触。实验集成过程始于商用PVA薄膜,其虽具备足够柔性可贴合人体皮肤,但高弯曲刚度限制了真实共形能力,导致气隙产生并与皮肤形成非共形接触(图2c)。为实现共形集成,本文施加水滴(约50 µL)触发PVA薄膜的固-液转变,赋予其流变特性,使其能自然匹配柔软皮肤(图2d)。干燥后,重构PVA薄膜与前臂皮肤形成无缝接触,即使经过大力拉伸、压缩、扭转和剥离仍无分层现象,证实了其与人体皮肤的强韧粘附。为定量表征表面曲率特性,将PVA薄膜与粗糙砂纸基板形成共形接触,剥离后薄膜保留乳头状微结构形貌,精确复制了目标基板的形貌特征,曲率半径小于2 µm。为验证复制保真度,本文将PVA贴合于皮肤复制模型并触发相变,剥离后的重构PVA薄膜携带负浮雕结构,精准复制了复制模型的微观纹理(图2e),证实了亚微米级的成型精度与一致性。力学表征显示原始PVA薄膜在拉伸应变约157%范围内呈现线性应力-应变关系,杨氏模量约112 MPa(图2f);而重构PVA薄膜的线性区间延伸至约176%拉伸应变,杨氏模量显著降低至约19.5 MPa(图2g)。这些结果表明,在构建的PVA薄膜中引入表面微结构可增强拉伸性,同时大幅降低刚度。
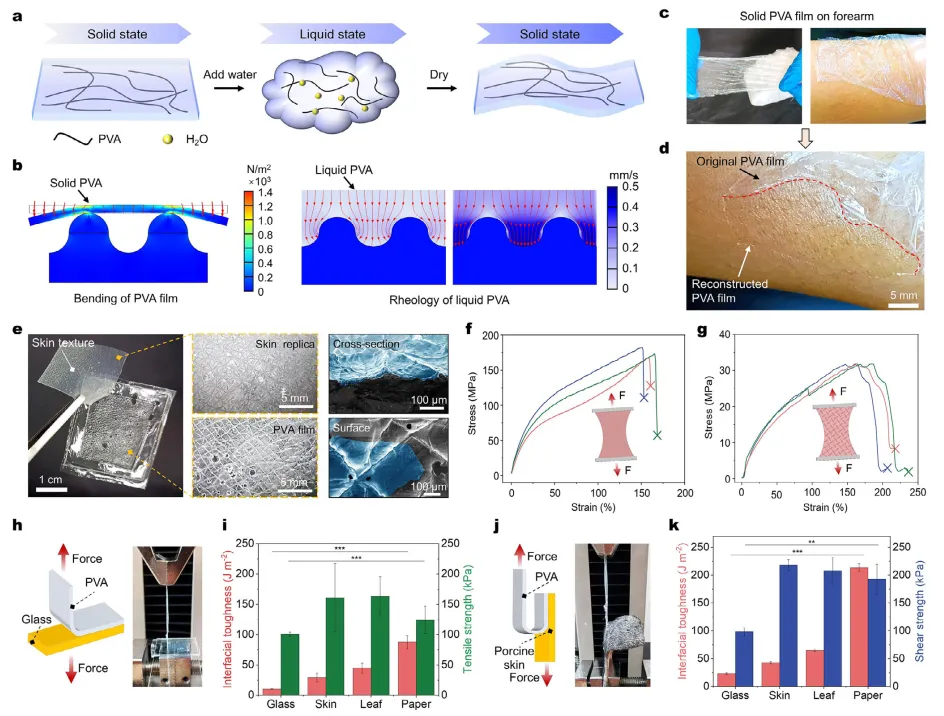
图2 重构PVA基底的相变机理与力学特性
【曲面目标上的共形打印】
为验证共形打印能力,本文通过相变路径将柔性电子器件转移至多种复杂目标表面。图3展示了PVA薄膜及其与目标物集成的表征结果,包括传统制备的柔性电子器件及PVA/纳米材料器件。如图3a示意图所示,首先通过传统光刻技术在刚性硅基底上制备纳米级厚度电极,随后通过溶解水溶性聚丙烯酸牺牲层实现器件剥离。采用牺牲层辅助转移印刷法后,超薄柔性电子器件可悬浮于水面。将PVA溶液涂覆于培养皿并干燥,形成PVA/柔性电子器件复合结构。随后将多层结构剥离并贴合至目标表面。相变驱动的PVA薄膜重构使其能够匹配目标表面形貌,在此过程中固态PVA薄膜转化为液态,实现与局部表面形貌的共形接触。图3b显示100纳米厚聚对二甲苯与50纳米厚金电极构成的柔性电子器件与PVA集成后,从培养皿剥离时无裂纹或褶皱,验证了该温和无损剥离方法的可靠性。此后所有此类基于PVA堆叠结构的电子器件均标准化标注为PVA/柔性电子器件。对于不规则复杂表面,该方法可实现共形接触。图3c展示了器件的多层结构示意图:超薄功能层(金属或纳米线网络)被PVA层包裹,在保持共形能力的同时提供机械保护与结构支撑。图3d展示了金属基(PVA/金)与纳米材料基(PVA/银纳米线)系统与相同PVA支撑层集成的实例,证实了相变转移工艺对不同导体类型与厚度的普适适用性。
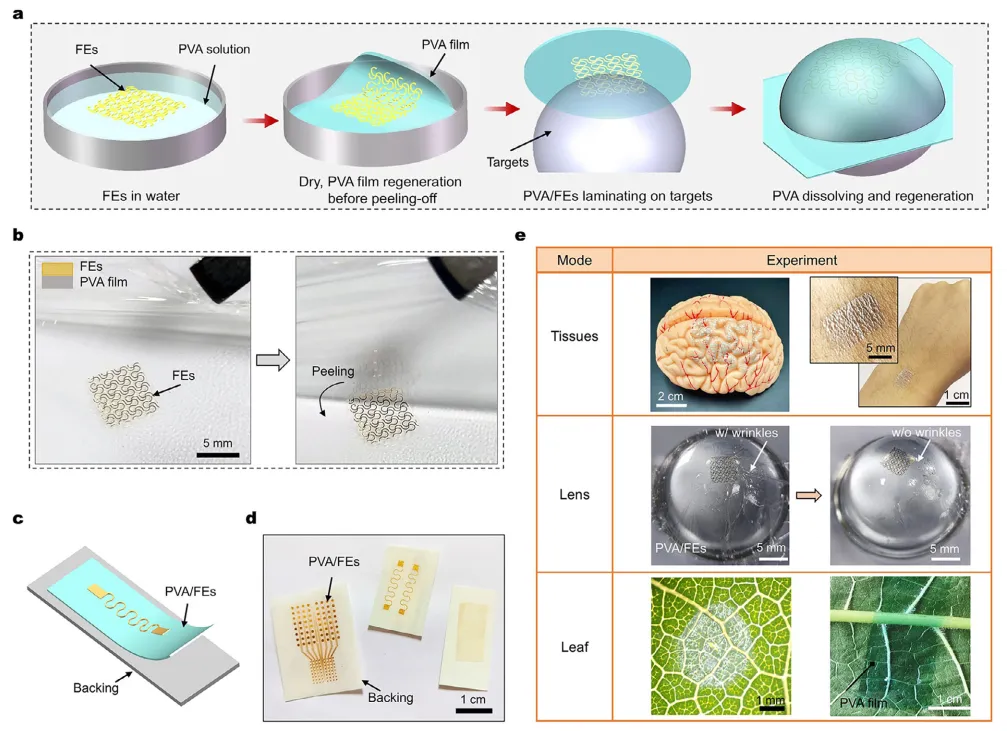
图3 面向监测目标的重构薄膜性能表征
【共形传感器:从蚕体运动追踪到人体运动追踪】
图4a展示了具有高共形性的应变传感器在脆弱且动态的蚕体表面的贴附情况。该器件通过将10 mg/mL银纳米线悬浮液浇铸至培养皿中的PVA溶液制备而成。干燥后获得超薄PVA/银纳米线复合材料(图4b),细节视图显示银纳米线嵌入基底内部(图4c)。柔性应变传感器共形贴附于蚕体表面,器件通过银导线与万用表电连接以读取信号。银纳米线在PVA基体中形成的致密渗透网络既确保了稳定的导电通路,又保持了机械柔性,同时防止了纳米线在拉伸或弯曲过程中脱落。这种可拉伸的共形应变传感器能顺应蚕体轮廓,且不阻碍其自然弯曲与运动。图4d展示了贴附传感器后蚕体的弯曲半径。无论是否贴附传感器,其最小弯曲半径变化趋势基本一致,证实了零机械干扰(图4e)。值得注意的是,蚕体持续佩戴传感器长达5天未出现明显健康异常,展现出优异的生物相容性。此外,在爬行过程中蚕体最大长度与原始状态保持一致,表明其日常活动未受限制(图4f)。与阻碍蚕体运动并干扰其自然功能的刚性绑带或胶带不同,本文的柔性传感器允许其自由活动。实时电阻记录显示清晰、周期性的信号,对应蚕体在每个蠕动爬行周期中表皮的拉伸与压缩,实现了对蚕类自然行为的无创高保真监测(图4g)。
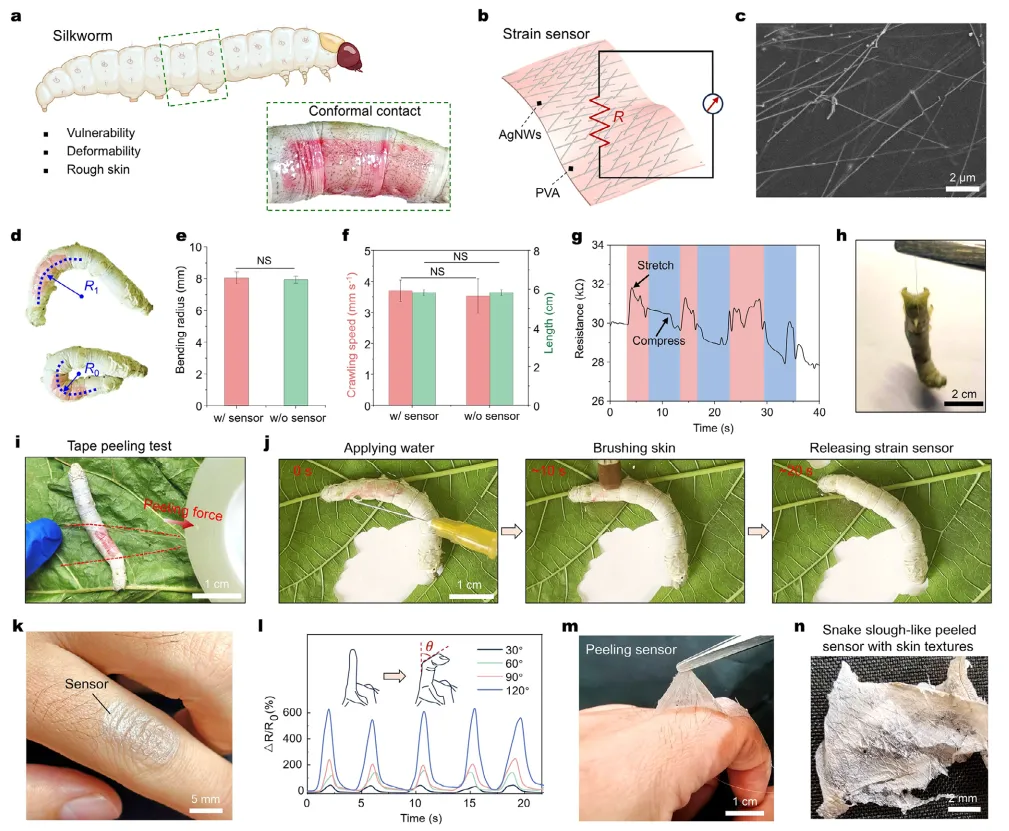
图4 适用于蚕体与人体运动检测的全共形传感器
【共形电极:从含羞草到人体皮肤电监测】
为解析电信号与植物运动的关系,本文在植物叶片上制备了共形PVA/银纳米线电极。图5a展示了含羞草叶片的结构:在膨胀状态下,伸展细胞充盈,小叶保持水平;当受到轻微触碰时,伸展细胞因离子流驱动的快速失水而收缩,导致叶柄下垂(图5b)。此过程中电响应调控着物理活动。为揭示该机制,本文在小叶和叶柄上贴合共形电极,实现了无需穿刺组织的无间隙接触(图5c)。如扫描电镜图像所示(图5d),电极形成了强韧的共形生物电子界面,完整包裹了包括气孔在内的叶片表面。与传统需要穿刺叶柄并必然造成结构损伤的刚性电极不同(图5e),本文的器件仅贴合于表面,完整保持了组织完整性。即使使用镊子刻意拉扯,电极仍能牢固附着于小叶,这证明了其强韧而温和的范德华粘附力,可在植物快速感震反应期间持续记录其电信号指令。共形电极在含羞草上持续贴附10天未引起萎蔫、黄化或任何可观察到的小叶膨压及反应异常,证实了器件的生物相容性及对植物生理的无干扰特性。
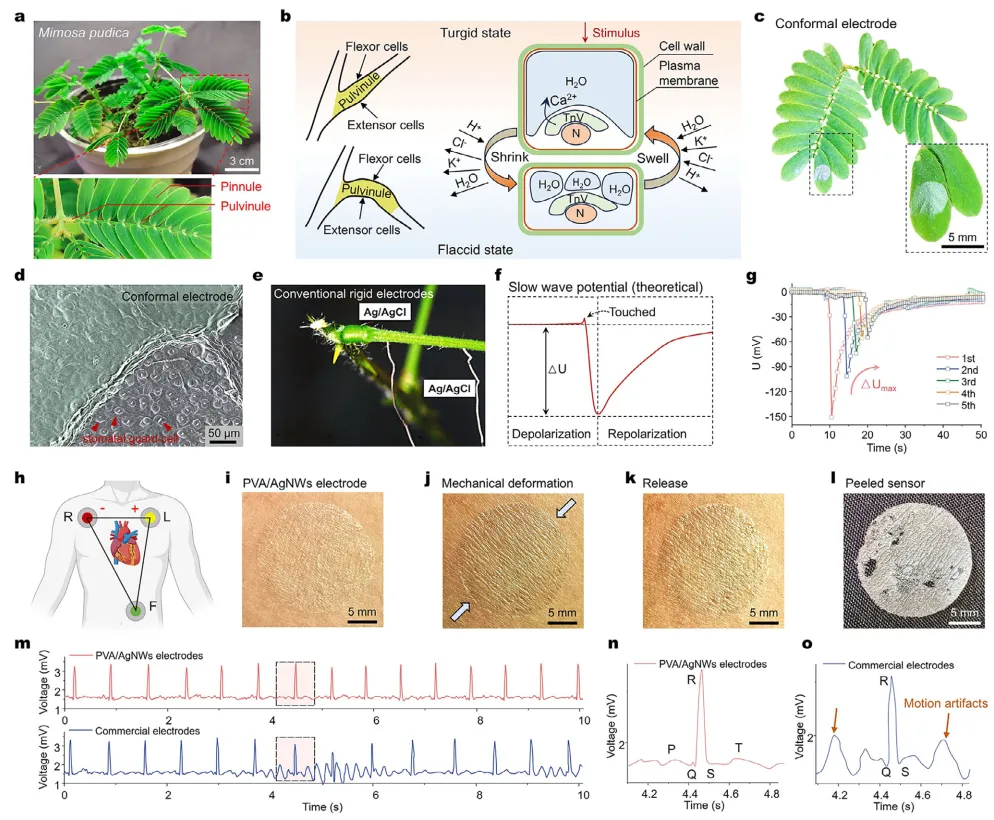
图5 用于植物与人体生理信号监测的共形电极
【总结与展望】
本文提出一种相变策略,可将柔性电子器件转化为瞬态液态表皮,使其能够流动并固化于生命体任意微观/宏观形貌表面。由此形成的范德华键合界面具有共形贴合、可拉伸、强韧且完全无应力的特性,并可按需通过水溶解实现无痛移除。在蚕体、含羞草叶片、人体多毛皮肤及胸部的实验验证表明,该技术能实现连续运动追踪与临床级心电图监测,突破了传统刚性电极、凝胶基电极或缝合固定电极的应用局限。通过将电子器件与最脆弱、最弯曲、最动态的生物表面无扰动融合,这项研究实现了对以往难以监测目标的原位高保真监控,拓展了生物集成器件的前沿疆界。
参考资料:
https://doi.org/10.1002/adma.73074
来源:EngineeringForLife
声明:仅代表作者个人观点,用于研究用途,作者水平有限,如有不科学之处,请在下方留言指正!
