思路可学!南京中医药大学 刘史佳教授:白头翁汤通过 SLC7A11/GPX4/FTH1 通路在溃疡性结肠炎中调节铁死亡介导的线粒体自噬和细胞凋亡
- 2026-05-06 04:32:57

各位热爱科研的小伙伴们,今天为大家推介2026年1月29日发表在 《Phytomedicine》杂志的研究性文章。该文章由南京中医药大学 刘史佳教授团队共同完成,聚焦精准医学与临床实践研究,深入阐明中医药防治溃疡性结肠炎作用机制。文章题为“Baitouweng decoction regulates ferroptosis-mediated mitophagy and apoptosis through the SLC7A11/GPX4/FTH1 pathway in ulcerative colitis”。本文旨在探讨白头翁汤对 DSS 诱导的溃疡性结肠炎的治疗效果及其分子机制,并且围绕白头翁汤、溃疡性结肠炎、铁死亡、线粒体自噬、凋亡、氧化应激关键词展开研究。

背景:溃疡性结肠炎(UC)是一种难治性慢性非特异性炎症性肠病,其患病率不断上升,重症可能进展为结肠癌。白头翁汤(Baitouweng Decoction, BTW)作为经典中药复方,在UC的临床治疗中已有数百年应用历史,但其具体作用机制尚不明确。铁死亡(ferroptosis)作为一种新近发现的程序性细胞死亡方式,被证实参与UC结肠上皮细胞死亡及炎症加剧过程。
SLC7A11/GPX4/FTH1通路是调控铁死亡(Ferroptosis)的核心防御轴。该通路构成了细胞对抗脂质过氧化的“盾牌系统”。SLC7A11 负责原料供应,GPX4 是核心执行器,而 FTH1 则通过管控铁离子源头消除隐患。三者协同运作,将细胞内的氧化应激水平维持在生存阈值之内。
目的:探究白头翁汤对葡聚糖硫酸钠(DSS)诱导的溃疡性结肠炎的治疗效果,并阐明其通过SLC7A11/GPX4/FTH1通路调控铁死亡介导的线粒体自噬(mitophagy)和细胞凋亡(apoptosis)的分子机制。
方法:蛋白质组学与转录组学分析:对UC小鼠结肠组织进行蛋白质组学和转录组学测序,识别差异表达蛋白/基因及富集通路。
动物实验:36只雄性C57BL/6小鼠随机分为6组:对照组、DSS模型组、BTW低/高剂量组(3.4/6.8 g·kg⁻¹·d⁻¹)、柳氮磺吡啶(SASP)阳性药组(200 mg·kg⁻¹·d⁻¹)、铁死亡抑制剂Fer-1组(5 mg·kg⁻¹·d⁻¹)。DSS组及给药组自由饮用3% DSS水溶液7天建立急性UC模型,给药组同时灌胃或腹腔注射相应药物。
细胞实验:TNF-α诱导Caco-2细胞建立体外UC模型,给予不同浓度BTW(15、30、60 μg/ml)干预;并采用铁死亡诱导剂RSL3和抑制剂Fer-1进行验证。
检测指标:疾病活动指数(DAI)、结肠长度、H&E染色组织病理评分;血清炎症因子(IL-1β, IL-6, TNF-α等)流式细胞术检测;氧化应激指标(MDA, SOD, GSH)及Fe²⁺含量;ROS荧光染色;Western blot和qPCR检测SLC7A11、GPX4、FTH1、PINK1、PARKIN、LC3、p62、BAX、BCL2等蛋白及mRNA表达。
结果:蛋白质组学分析显示铁死亡通路是UC的关键致病机制,DSS组TFRC、ACSL4等上调,GPX4等下调。
BTW显著改善UC小鼠体重下降、DAI评分升高、结肠缩短和组织病理损伤;降低血清促炎因子(IL-1β, TNF-α, CXCL1等),升高抗炎因子IL-10;上调肠道紧密连接蛋白Occludin和ZO-1,保护肠屏障。
BTW抑制铁死亡:升高结肠组织SLC7A11、GPX4、FTH1蛋白表达;降低血清MDA和Fe²⁺水平,升高SOD和GSH;减少ROS积累。
体外实验验证:BTW以剂量依赖性抑制TNF-α诱导的Caco-2细胞炎症,上调SLC7A11/GPX4/FTH1,且该作用可被RSL3(GPX4抑制剂)部分逆转,表明BTW通过抑制铁死亡发挥作用。
转录组学揭示凋亡和铁死亡为核心通路,线粒体自噬为连接枢纽。BTW激活PINK1/PARKIN介导的线粒体自噬(上调PINK1、PARKIN、LC3II/LC3I,下调p62和NLRP3),同时调节BCL2/BAX比值抗凋亡。
结论:白头翁汤通过激活SLC7A11/GPX4/FTH1通路抑制铁死亡,并协同调节PINK1/PARKIN介导的线粒体自噬和细胞凋亡,从而减轻溃疡性结肠炎相关的炎症反应和肠屏障损伤,缓解氧化应激。
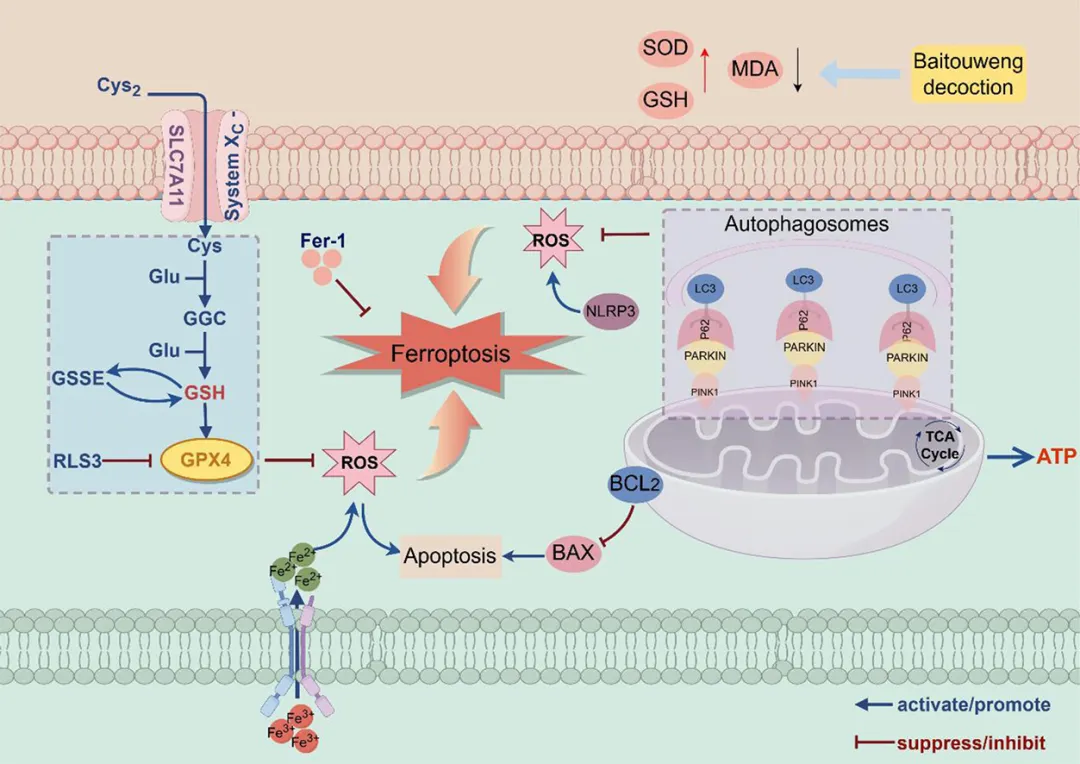
图形摘要
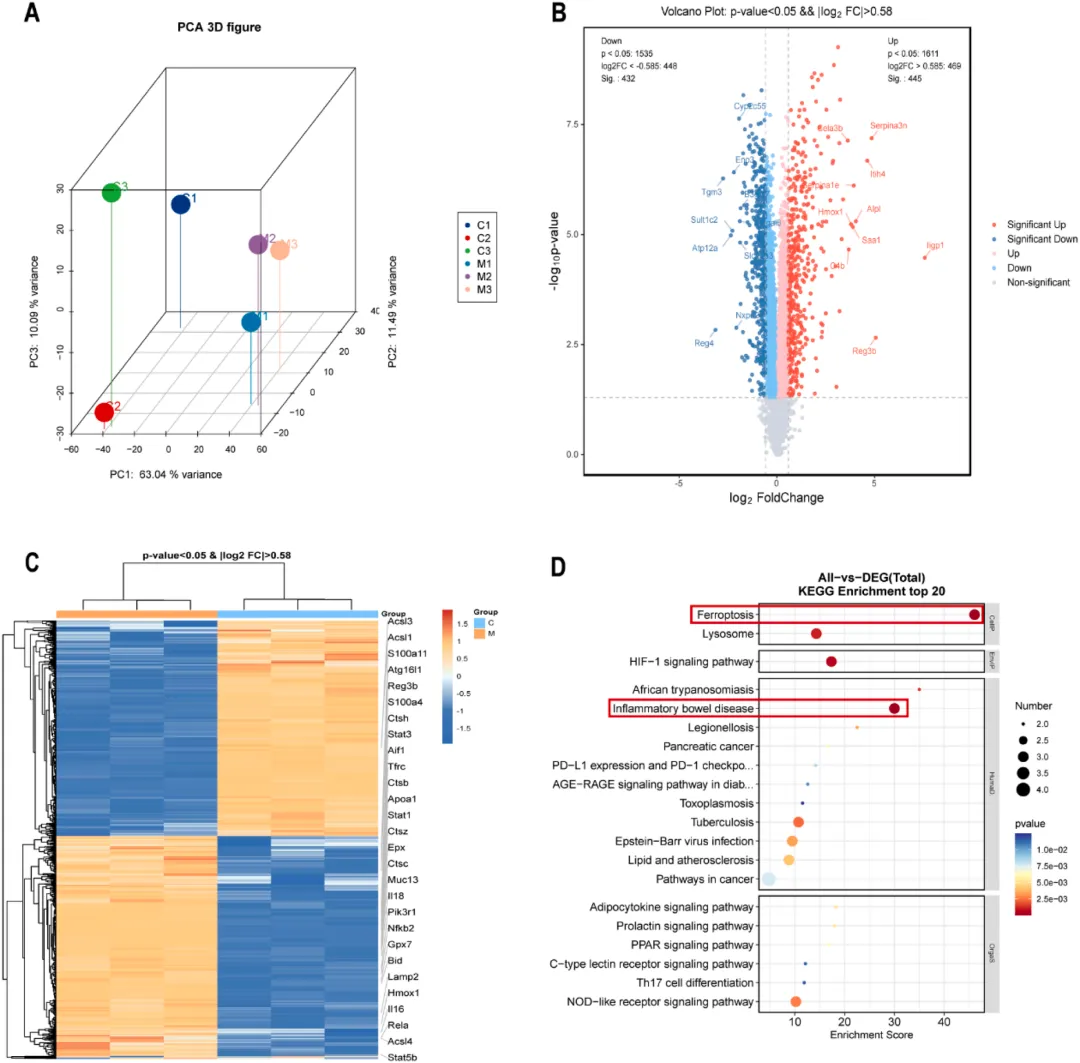
图1 对照组与模型组(DSS 处理)小鼠结肠组织的蛋白质组学分析(n=3)。
(A)主成分分析;(B) 差异表达蛋白(DEPs)火山图;(C) 差异表达蛋白热图;(D) KEGG 通路富集分析。
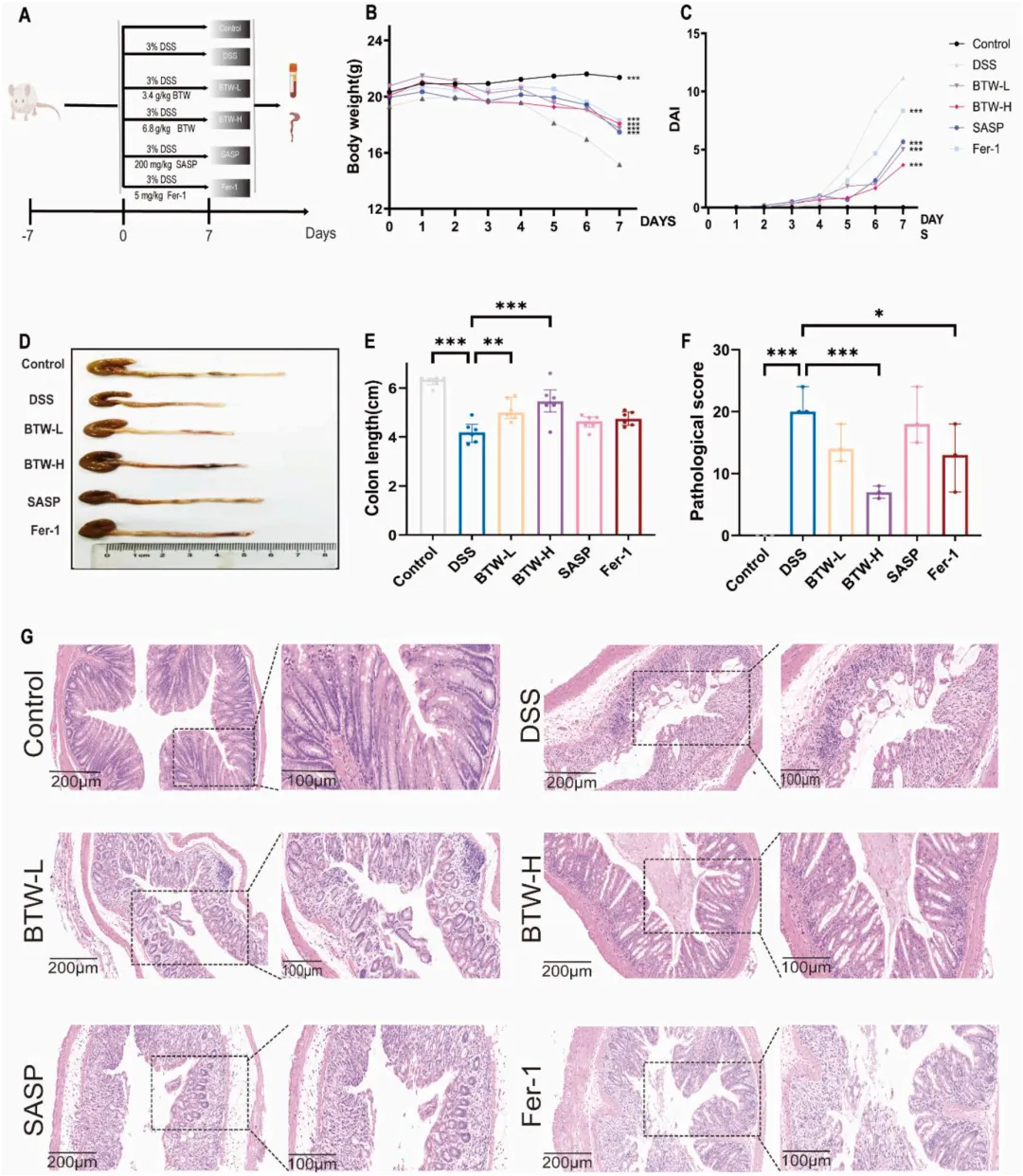
图2 白头翁汤可改善小鼠溃疡性结肠炎相关症状。
(A)动物实验流程图;(B) 体重变化(n=6);(C) 疾病活动指数评分(n=6);(D) 结肠长度对比代表性图像;(E) 结肠长度统计(n=6);(F) 组织学评分(n=3);(G) 结肠组织 H&E 染色代表性图像。
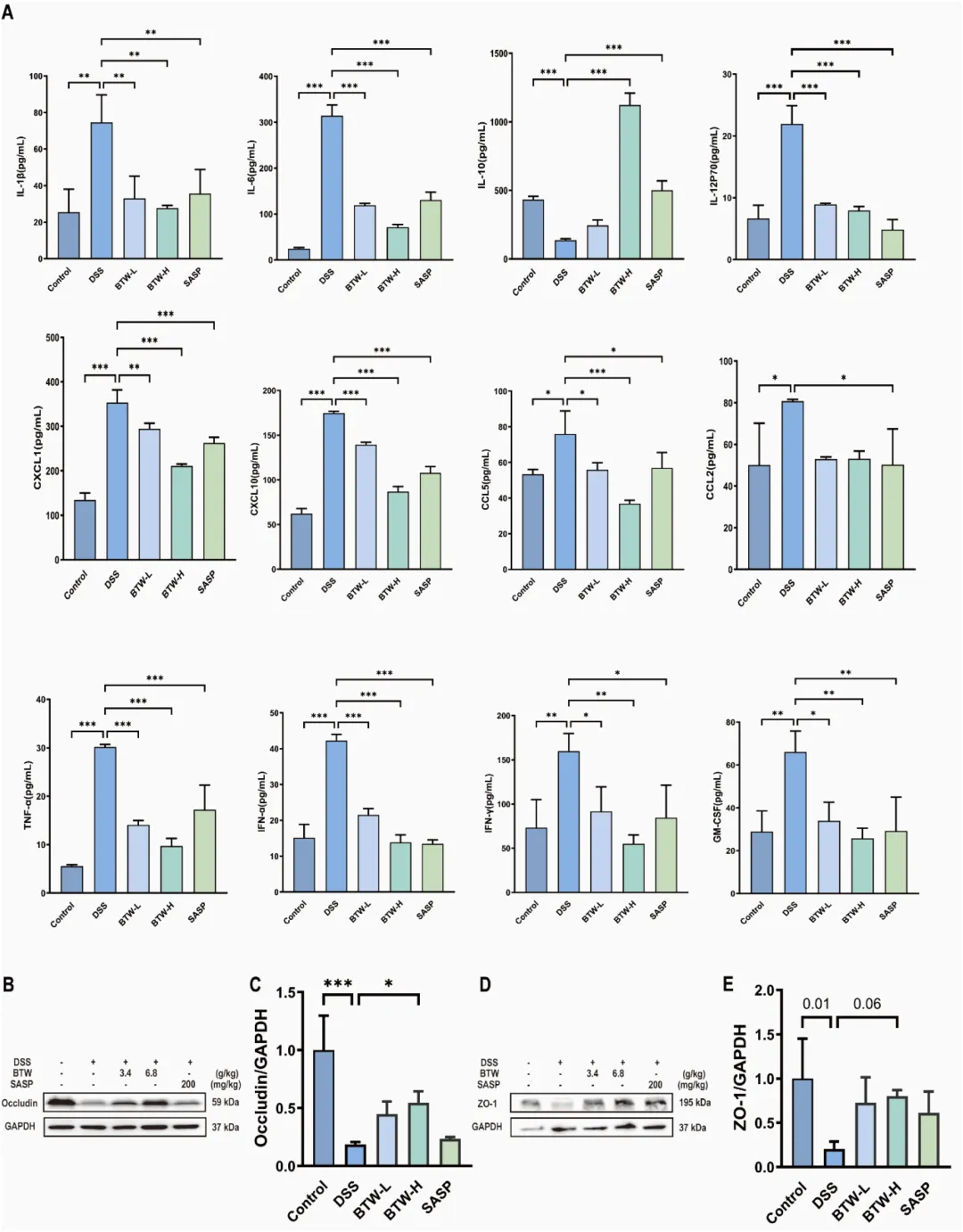
图3 白头翁汤改善溃疡性结肠炎小鼠结肠炎症并保护肠道屏障功能。
(A)血清炎症因子表达(n=3);(B) 蛋白免疫印迹法检测结肠组织中闭合蛋白(Occludin)的表达;(C) 图 B 中闭合蛋白定量分析(n=3);(D) 蛋白免疫印迹法检测结肠组织中紧密连接蛋白 1(ZO-1)的表达;(E) 图 D 中紧密连接蛋白 1 定量分析(n=3)。
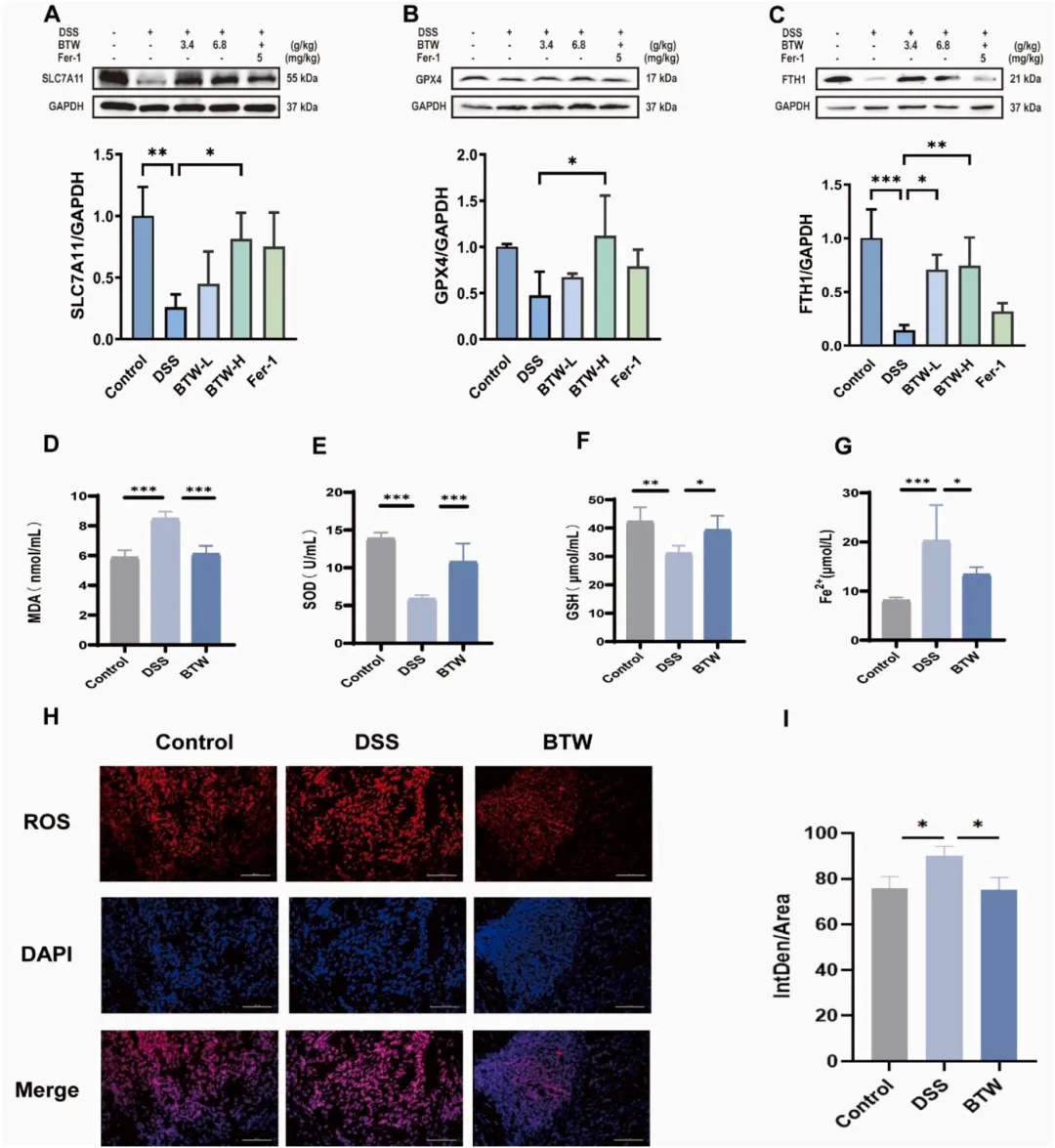
图4 白头翁汤抑制溃疡性结肠炎小鼠铁死亡。
(A–C) 蛋白免疫印迹法定量检测结肠组织中 SLC7A11、GPX4、FTH1 的蛋白表达水平(n=3);(D–F) 血清中丙二醛(MDA)、超氧化物歧化酶(SOD)、谷胱甘肽(GSH)水平(n=6);(G) 结肠组织中 Fe²⁺相对含量(n=6);(H–I) 活性氧(ROS)水平免疫荧光分析(n=3)。
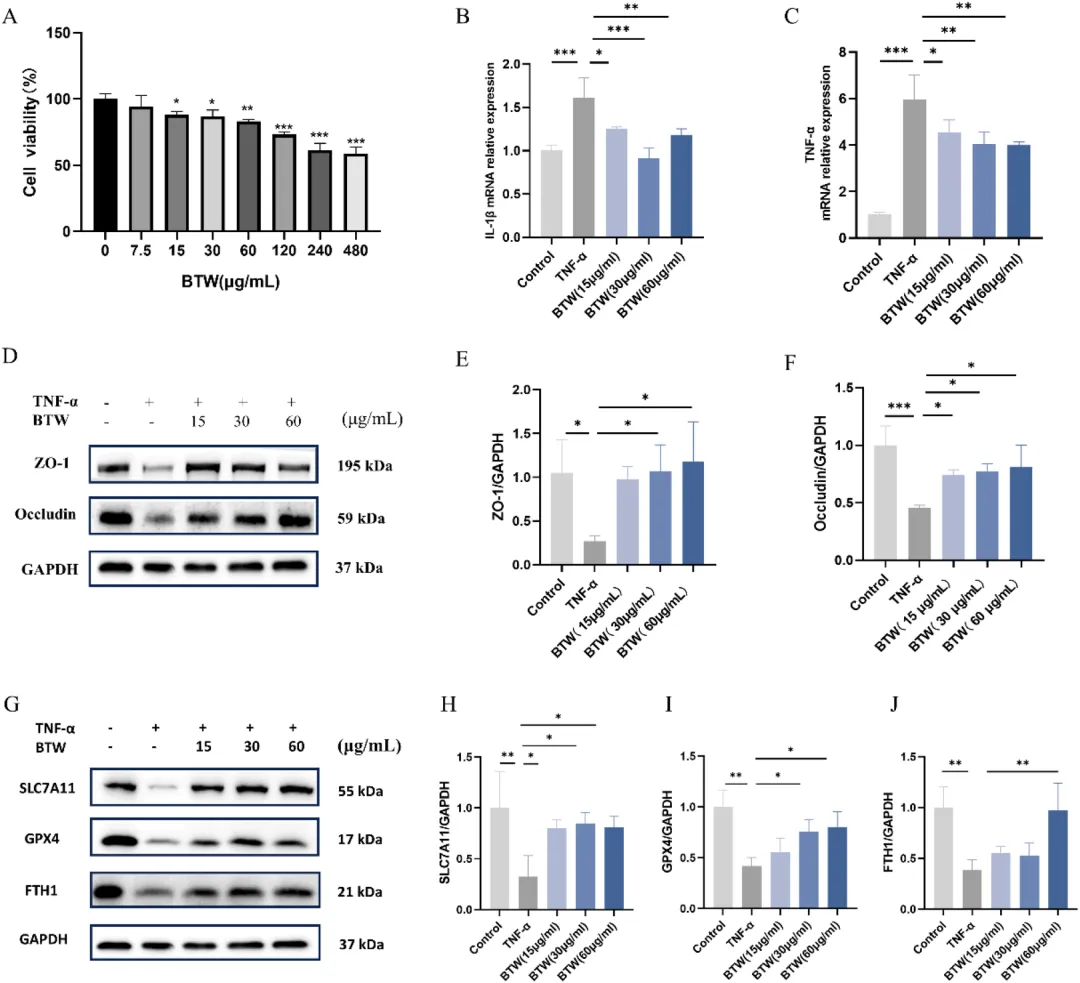
图5 白头翁汤抑制 TNF‑α 诱导的 Caco‑2 细胞铁死亡。
(A)不同浓度白头翁汤(7.5、15、30、60、120、240、480 μg/mL)处理 Caco‑2 细胞 24 h 后的细胞活力;(B–C) IL‑1β 和 TNF‑α 的相对 mRNA 表达(n=3);(D) 蛋白免疫印迹法检测紧密连接蛋白 1(ZO-1)和闭合蛋白(Occludin)的蛋白表达水平;(E–F) 图 D 中闭合蛋白与紧密连接蛋白 1 定量分析(n=3);(G) 蛋白免疫印迹法检测 SLC7A11、GPX4、FTH1 的蛋白表达;(H–J) 图 G 中 SLC7A11、GPX4、FTH1 定量分析(n=3)。
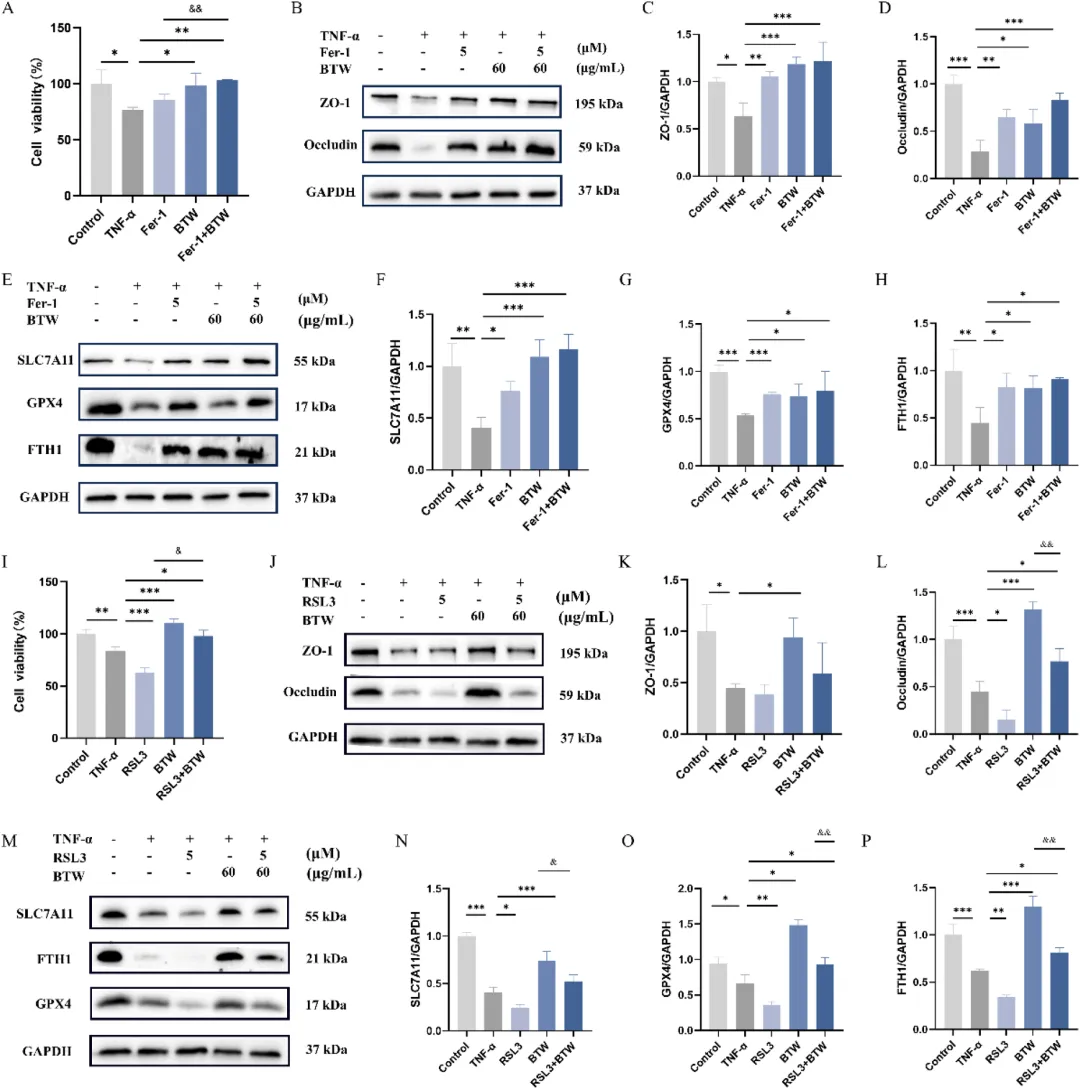
图6 白头翁汤抑制 RSL3 诱导的 Caco‑2 细胞铁死亡。
(A)铁抑素‑1(Ferrostatin‑1)对细胞活力的影响;(B–D) 蛋白免疫印迹法定量检测紧密连接蛋白 1(ZO-1)和闭合蛋白(Occludin)的蛋白表达水平(n=3);(E–H) 蛋白免疫印迹法定量检测 SLC7A11、GPX4、FTH1 的蛋白表达水平(n=3);(I) RSL3 对细胞活力的影响;(J–L) 蛋白免疫印迹法检测紧密连接蛋白 1(ZO-1)和闭合蛋白(Occludin)的蛋白表达(n=3);(M–P) 蛋白免疫印迹法检测 SLC7A11、GPX4、FTH1 的蛋白表达(n=3)。
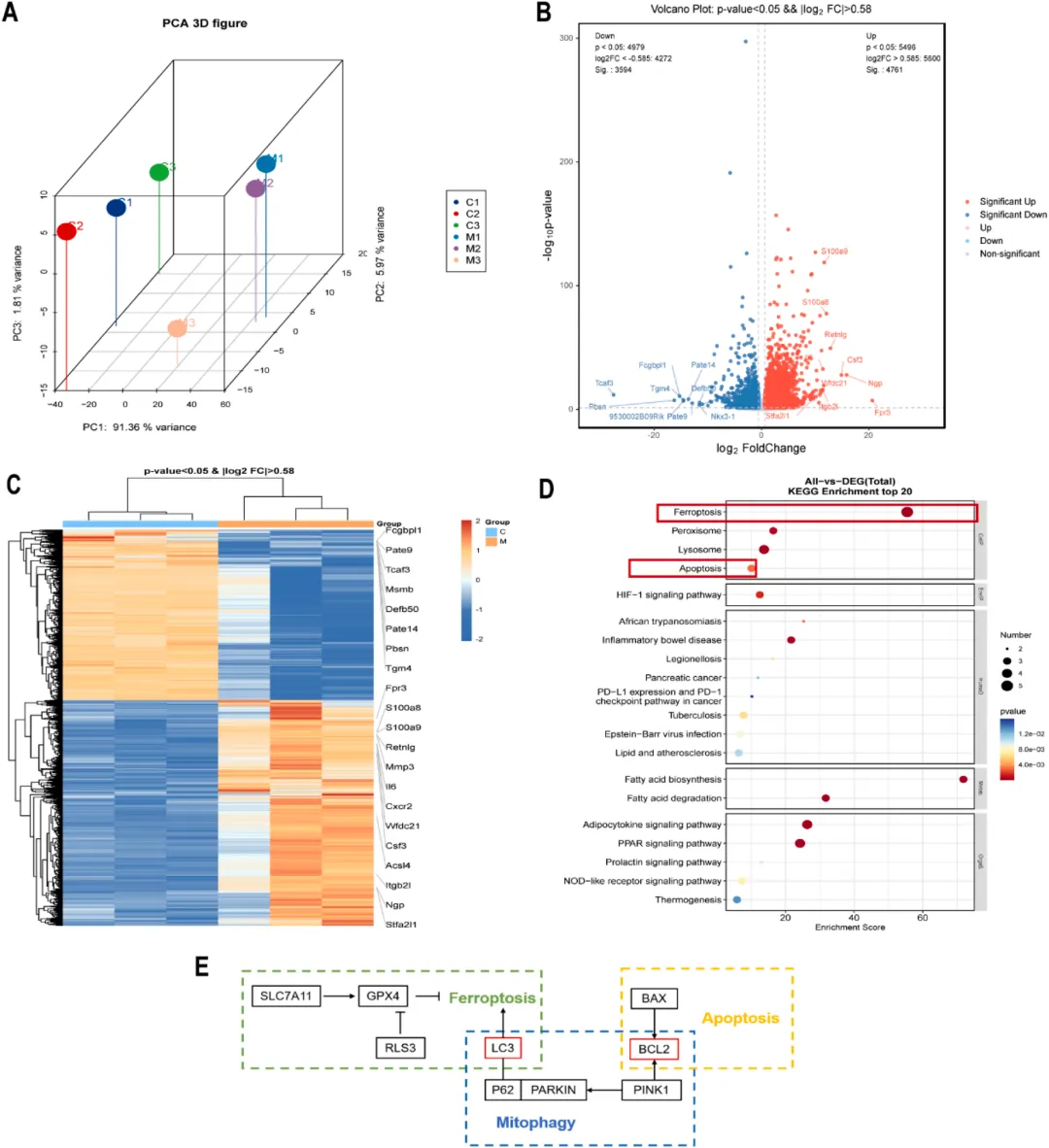
图7 对照组与模型组(DSS 处理)小鼠结肠组织的转录组学分析(n=3)。
(A)主成分分析;(B) 差异表达基因(DEGs)火山图;(C) 差异表达基因热图;(D) KEGG 通路富集分析;(E) 铁死亡、凋亡和线粒体自噬信号通路的 KEGG 分析。
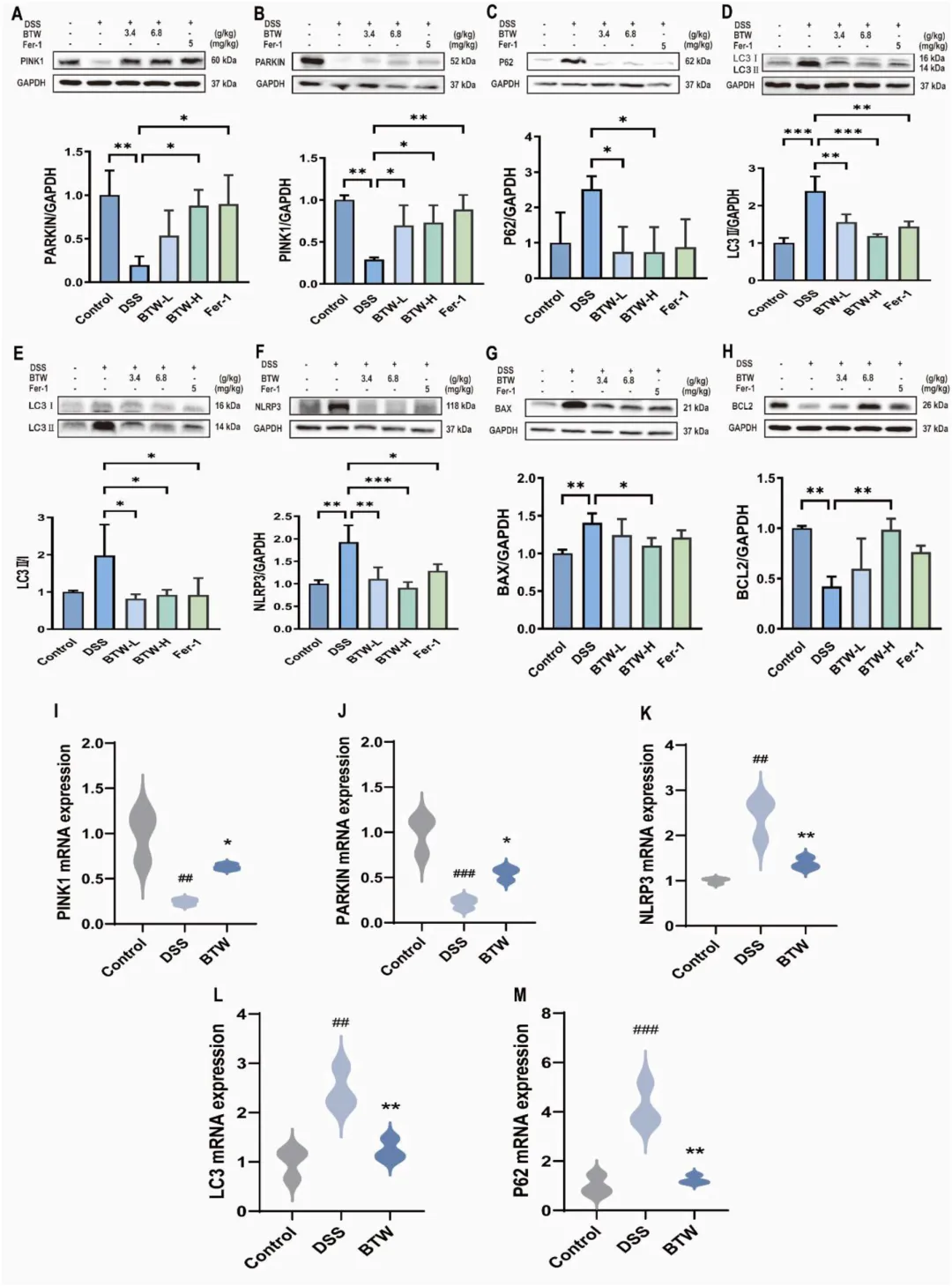
图8 白头翁汤通过激活 PINK1/PARKIN 介导的线粒体自噬改善溃疡性结肠炎。
(A–H) PINK1、PARKIN、P62、LC3、NLRP3、BAX、BCL2 的蛋白表达(n=3);(I–M) PINK1、PARKIN、NLRP3、LC3、P62 的相对 mRNA 表达(n=3)。
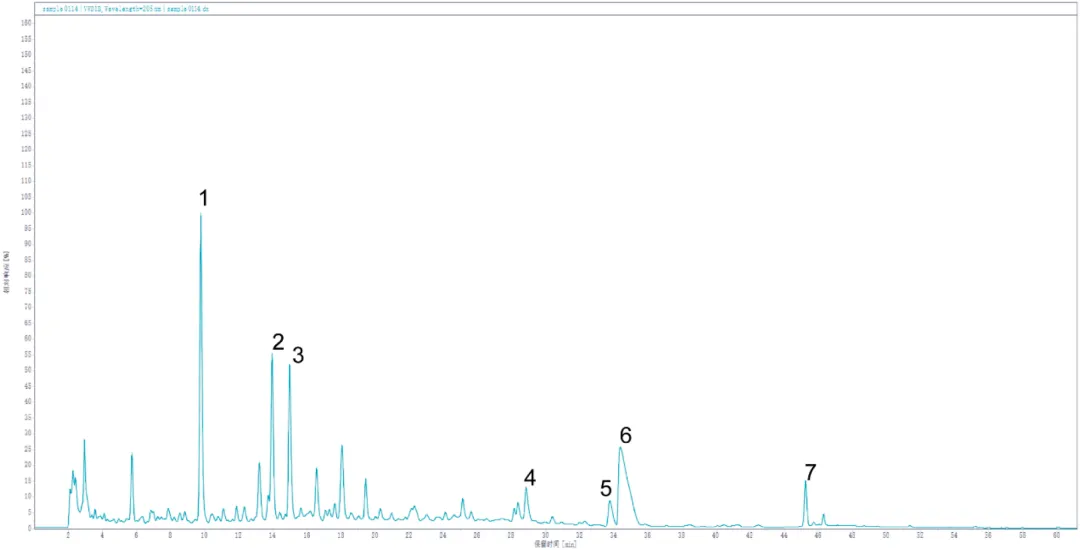
图9 白头翁汤化学成分定性分析。
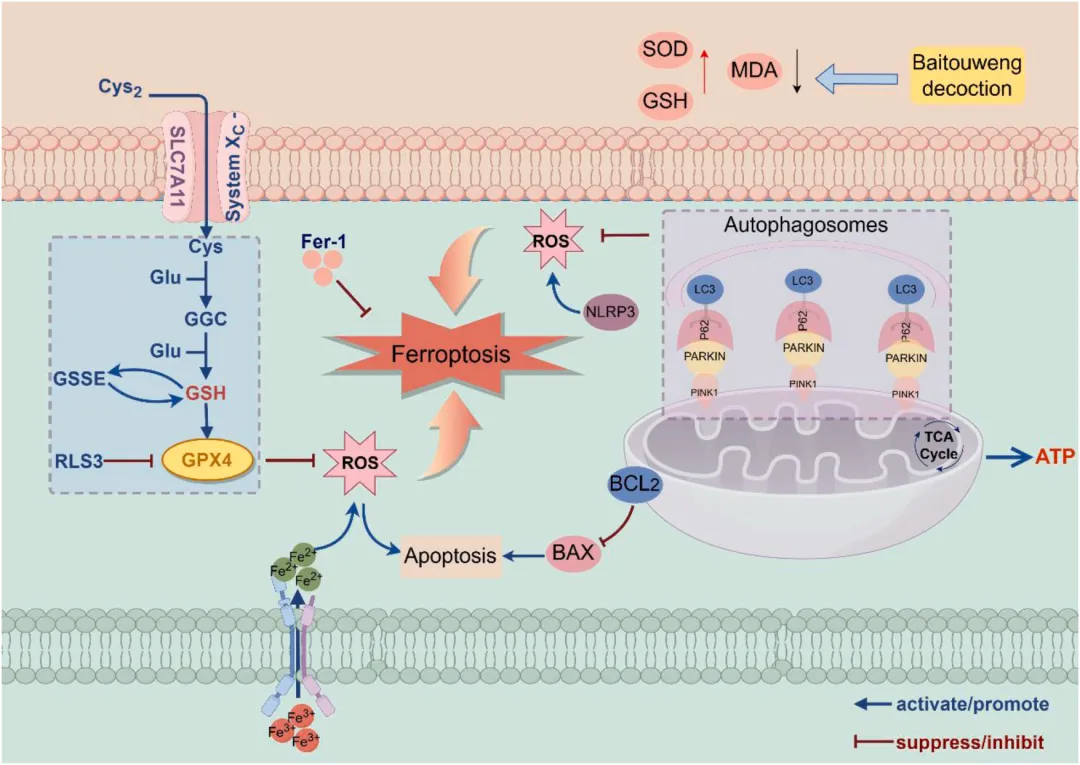
图 10 白头翁汤抗溃疡性结肠炎的作用机制示意图。
综上所述,本研究通过多组学分析、动物实验和细胞实验系统证实:白头翁汤可通过抑制SLC7A11/GPX4/FTH1介导的铁死亡通路来改善溃疡性结肠炎。在抑制铁死亡的同时,BTW还能调节体内线粒体自噬和凋亡水平。具体机制为:UC诱导炎症因子水平升高,损害线粒体自噬功能,导致受损线粒体清除障碍、ROS积累,从而显著增强细胞对铁死亡的易感性;过量的ROS进一步影响细胞增殖、触发脂质过氧化和凋亡,驱动铁死亡发生。BTW通过激活PINK1/PARKIN通路恢复线粒体自噬,上调抗凋亡蛋白BCL2、下调促凋亡蛋白BAX,并增强SLC7A11/GPX4/FTH1抗氧化系统的功能,最终多环节协同缓解UC。本研究为白头翁汤治疗溃疡性结肠炎的临床应用提供了新的机制依据,并提示靶向铁死亡-线粒体自噬-凋亡交叉对话可能是治疗UC的有效策略。未来需要进一步探索这三种过程如何交互调控UC,以及BTW在其他消化道炎症疾病中的适用性。


需要领取文献的同学,后台私信“89”,即可领取!
《医研三人行》公众号推送文章仅为学术交流使用,仅供读者参考。公众号中“原创”标识仅代表原创编译之作,不代表本公众号对文本主张版权。版权归文章作者所有。
1、APSB 综述,青岛大学亓洪昭/孙锦平/姜少燕艳团队:细胞外囊泡穿越血脑屏障的精准打击,是缺血性中风治疗的范式革命还是临床泡沫?
2、肝纤维化又发顶刊 Autophagy!新分子 + 外泌体机制,直接抄思路:UBQLN1的O-GlcNAc糖基化修饰打破磷酸化-泛素化稳态,双重驱动MASH纤维化
3、流行病学研究表明,肥胖会增加乳腺癌的发病率么?西班牙庞培法布拉大学发现:肿瘤细胞与脂肪细胞之间的相互作用促进肿瘤细胞的迁移和侵袭



